Понятие о строении атома. Срстав атомных ядер. презентация
Содержание
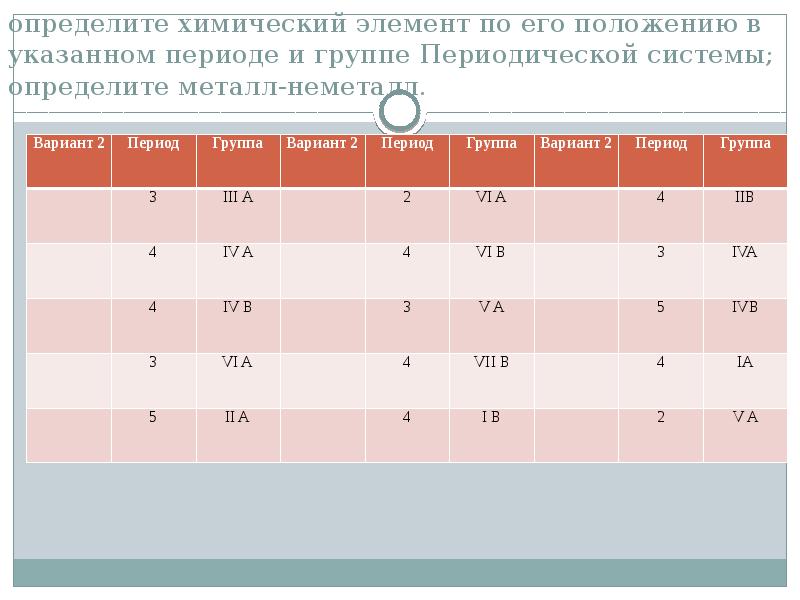
- 2. определите химический элемент по его положению в указанном периоде и группе
- 3. Решите задачи:
- 4. Представление об атоме Атом-мельчайшая частица химического вещества . Размеры атомов ничтожно
- 5. Научные открытия Ирландский физик Стони в1891 году открыл, что электричество переносится
- 6. Антуан Анри Беккерель открыл явление радиоактивности
- 7. Джозеф Джон Томсон
- 8. Эрнст Резерфорд
- 9. Нильс Бор
- 10. Планетарная модель строения атома В Солнечной системе планеты обращаются вокруг
- 11. Каковы размеры ядра? Если представить себе атомное ядро в виде вишни,
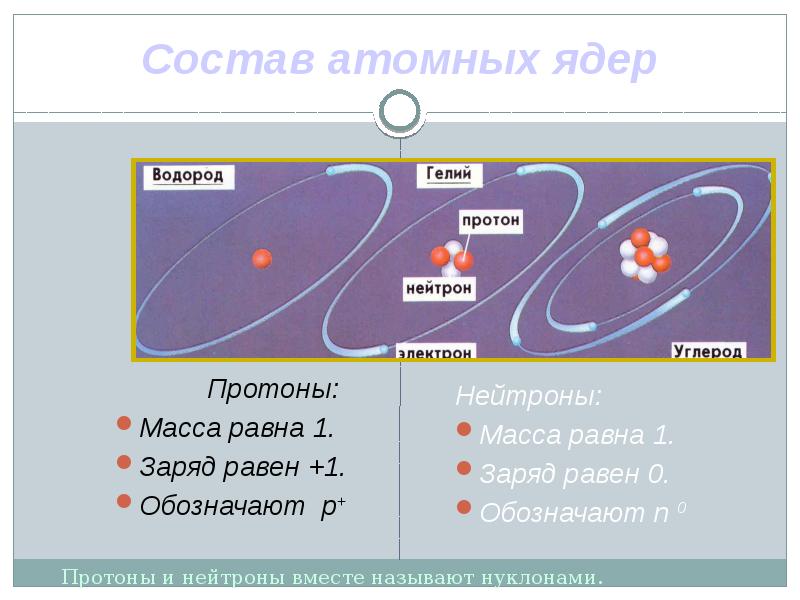
- 12. Состав атомных ядер Протоны: Масса равна 1. Заряд равен +1. Обозначают
- 13. Понятие об электроне Электроны вращаются вокруг ядра со скоростью света
- 14. Строение атома и Периодическая система Число протонов в атоме равно порядковому
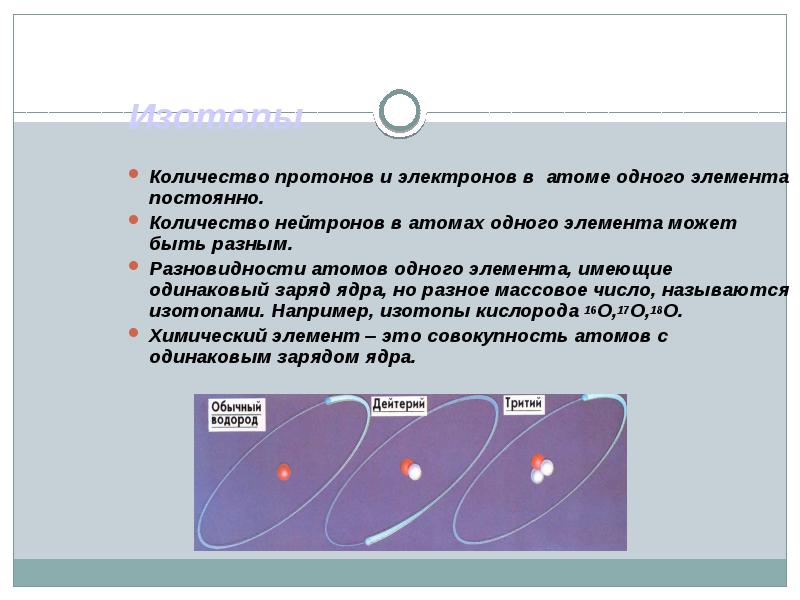
- 15. Изотопы Количество протонов и электронов в атоме одного элемента постоянно. Количество
- 16. Скачать презентацию











Слайды и текст этой презентации
Скачать презентацию на тему Понятие о строении атома. Срстав атомных ядер. можно ниже:
Похожие презентации





























