Различают две основные теории специфичности ферментов: презентация
Содержание
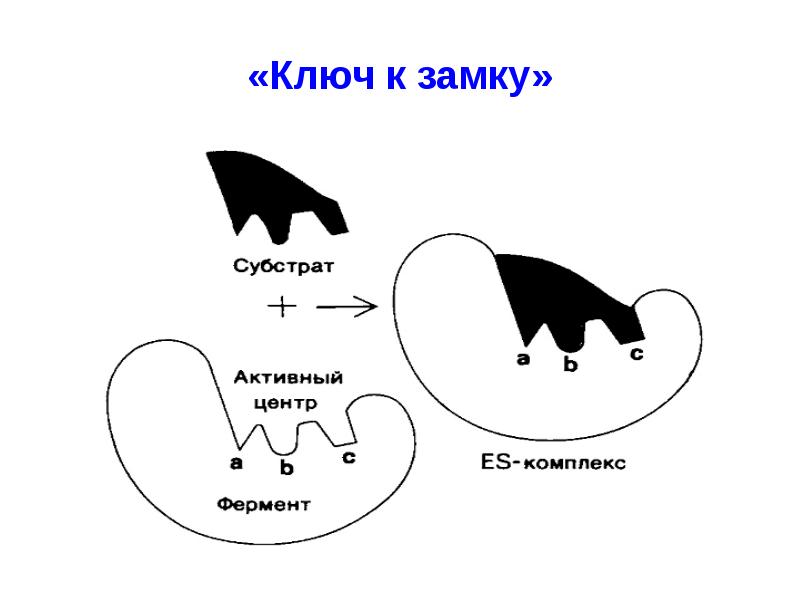
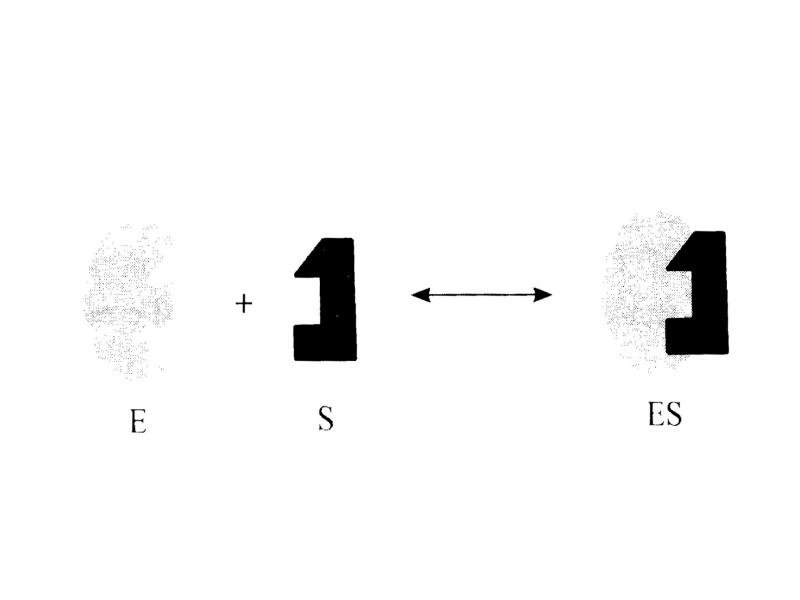
- 2. 1-ая теория предложена Э. Фишером предусматривает наличие
- 3. «Ключ к замку»
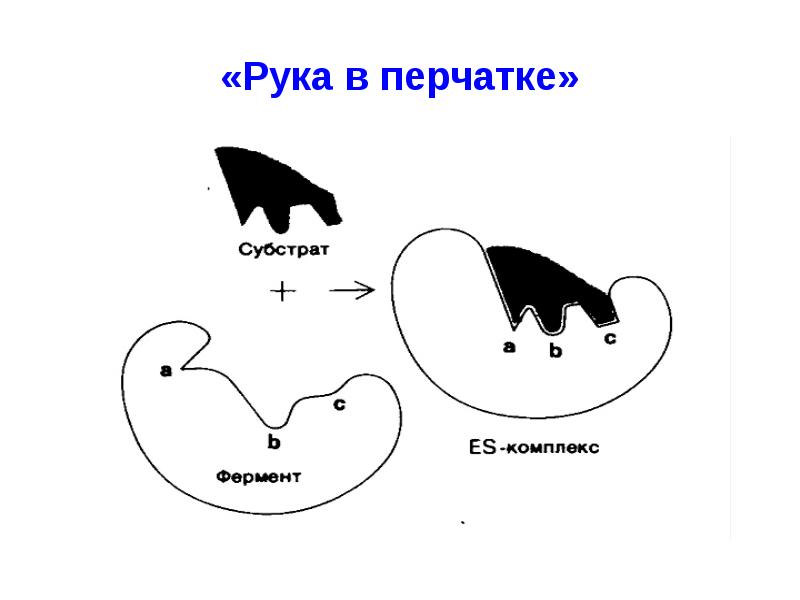
- 5. 2-ую теорию предложил Кошленд По данной теории молекула фермента является гибкой,
- 6. «Рука в перчатке»
- 7. Модуль «Ферменты» Лекция 2 Механизм действия ферментов. Кинетика ферментативных реакций
- 8. Рассмотрим механизм действия ферментов: с точки зрения изменения энергетики химических
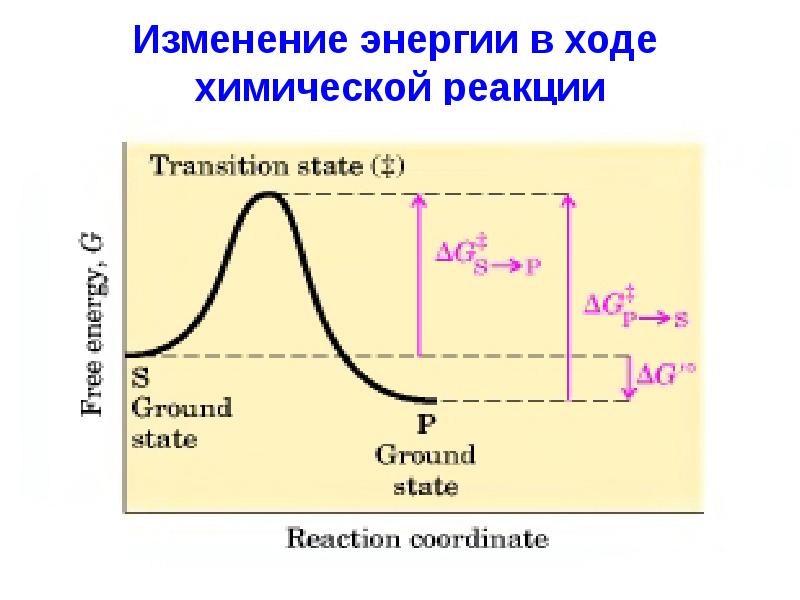
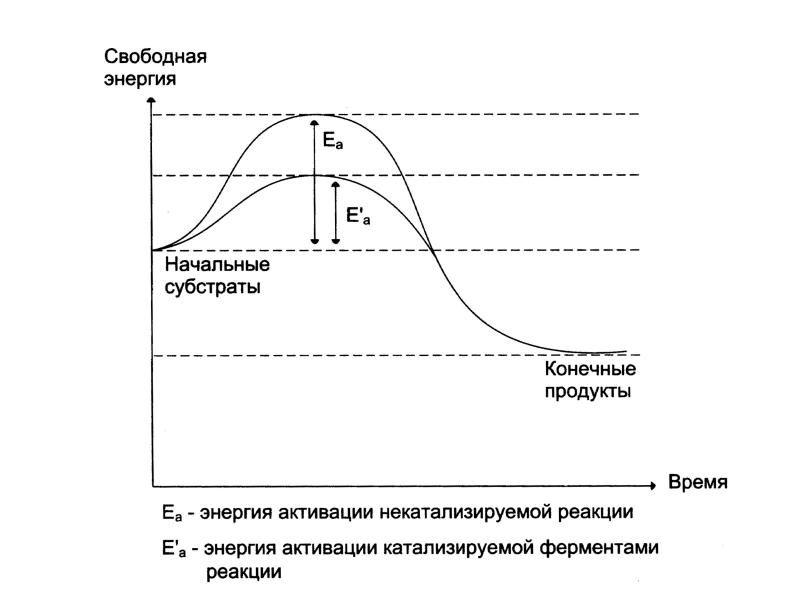
- 9. Изменение энергии в ходе химической реакции
- 10. Ферменты, как истинные катализаторы значительно повышают V определенных химических реакций, которые
- 11. Диаграмма изменения свободной энергии реакции без и с Е
- 13. V реакции зависит от энергетического барьера, который реагирующим веществам нужно преодолеть.
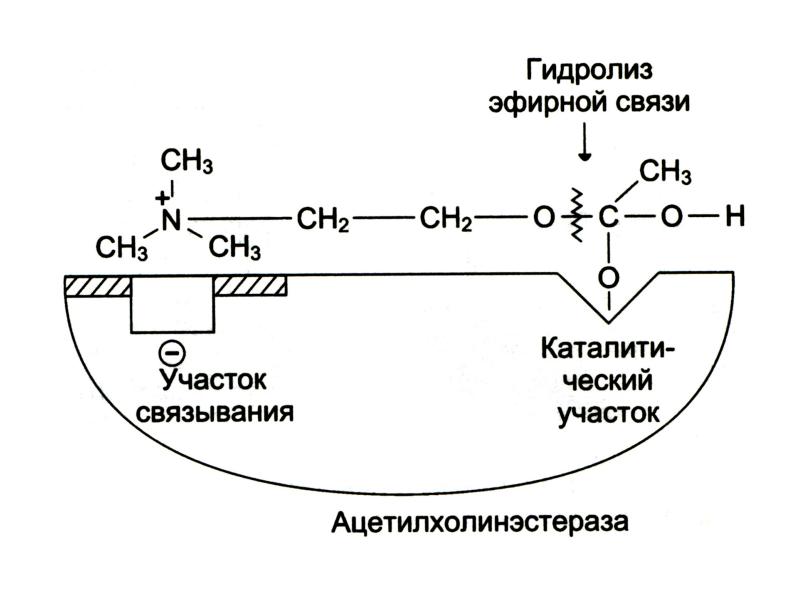
- 14. При образовании [E-S] комплекса происходит перераспределение электронной плотности в S и
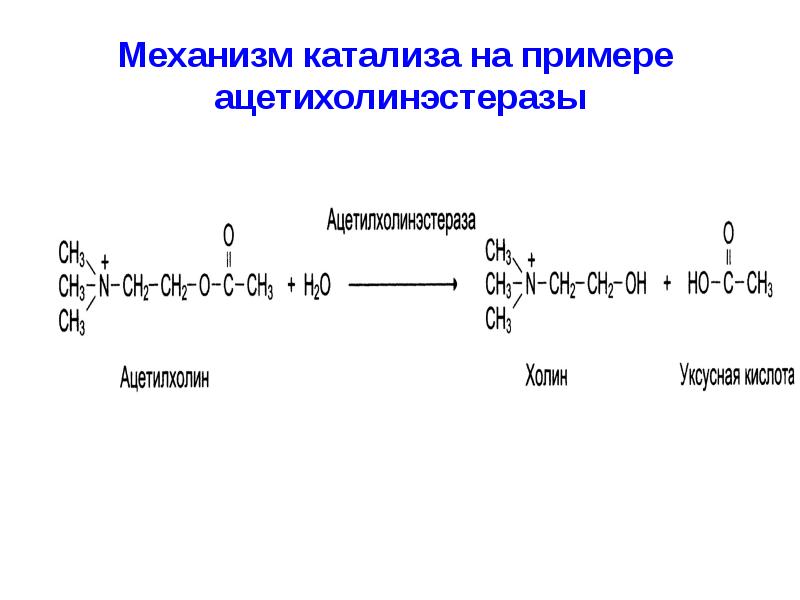
- 15. Механизм катализа на примере ацетихолинэстеразы
- 17. Для выражения активности ферментов используют: международную единицу, катал, удельную активность, молярную
- 18. Единицы ферментативной активности Международная единица – это такое количество Е, которое
- 19. В системе СИ выражение активности фермента в каталах 1 катал (кат)
- 20. 1 кат = 1 М/сек = 60 М /мин = 60∙106
- 21. Удельная активность – ферментативная активность на единицу массы белка:
- 22. Молярная активность (число оборотов фермента) –
- 23. Ферментативная кинетика Основы кинетики
- 24. Ферментативная кинетика k1 k3 E + S ↔
- 25. В момент наступления равновесия:
- 26. Кm – основная характеристика ферментативной реакции, характеризует сродство E к S.
- 27. Бриггс и Холдейн вывели математическое выражение зависимости V реакции от [S]:
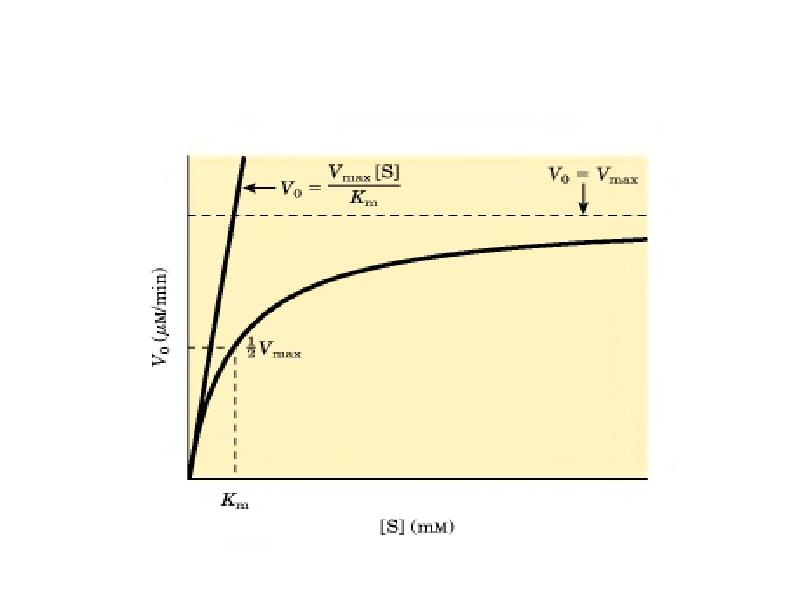
- 28. Графическая зависимость V от [S]
- 29. Возможно 3 варианта решения уравнения Михаэлиса: 1. [S] > Кm
- 31. Физический смысл Кm заключается в том, что Кm численно равна [S],
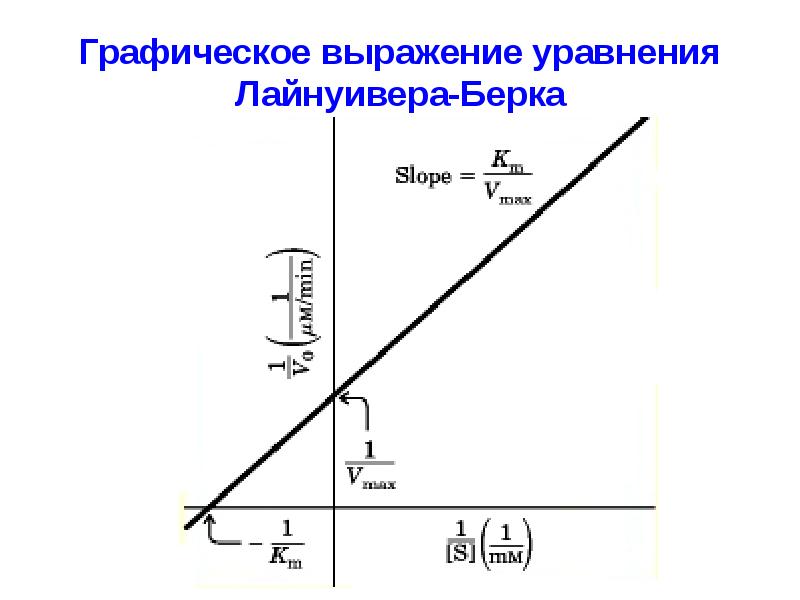
- 32. Г. Лайнуивер и Д. Берк преобразовали уравнение Михаэлиса-Ментен, выразив обе части
- 33. Графическое выражение уравнения Лайнуивера-Берка
- 34. Зависимость скорости реакции от концентрации фермента
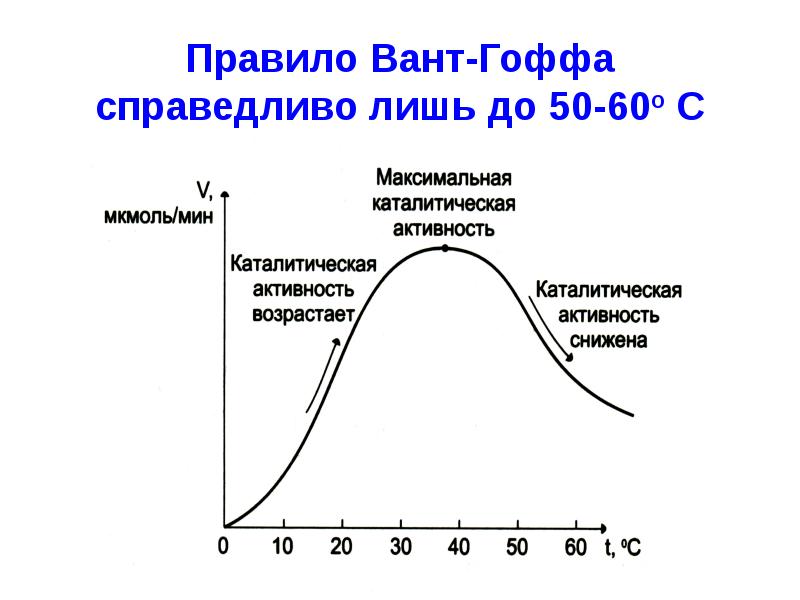
- 35. Зависимость скорости реакции от температуры
- 36. Правило Вант-Гоффа справедливо лишь до 50-60о С
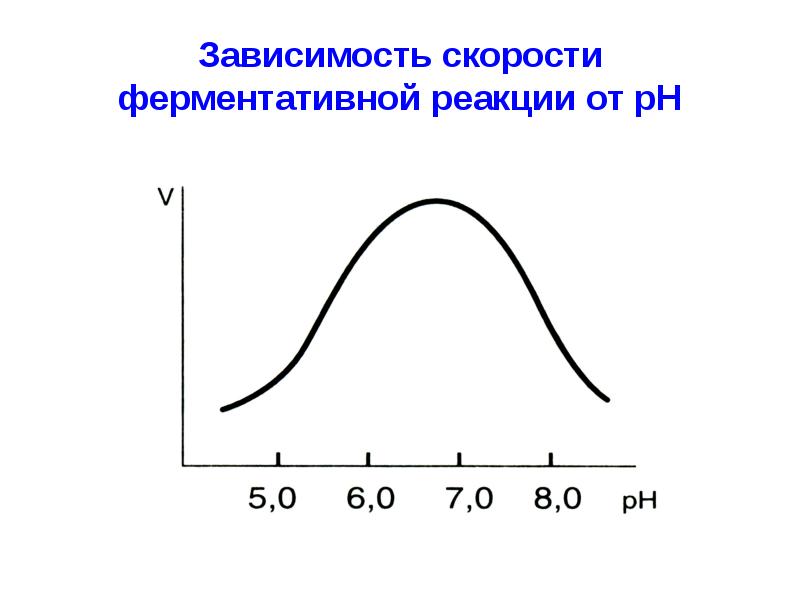
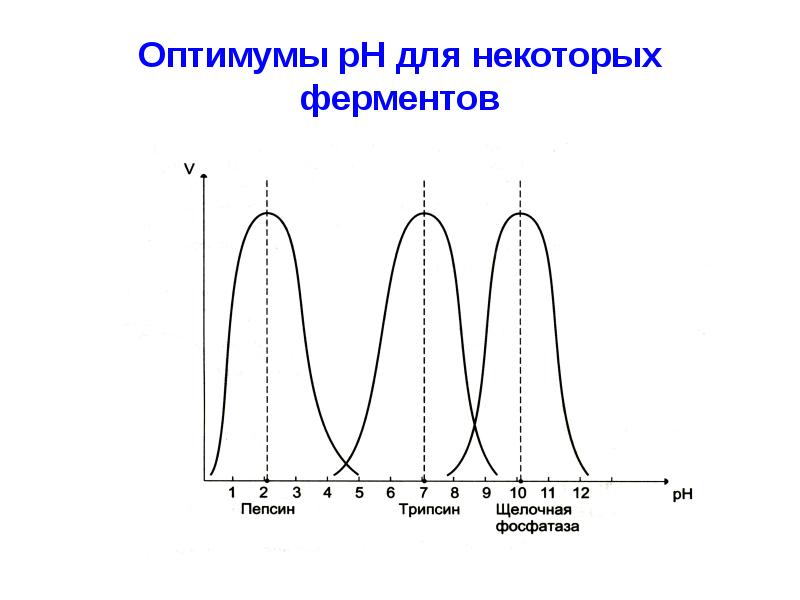
- 37. Зависимость скорости ферментативной реакции от рН
- 38. pH среды влияет на скорость диссоциации различных функциональных группировок, входящих в
- 39. При изменении pH изменяется количество ионных связей в молекуле, а, значит,
- 40. Оптимумы рН для некоторых ферментов
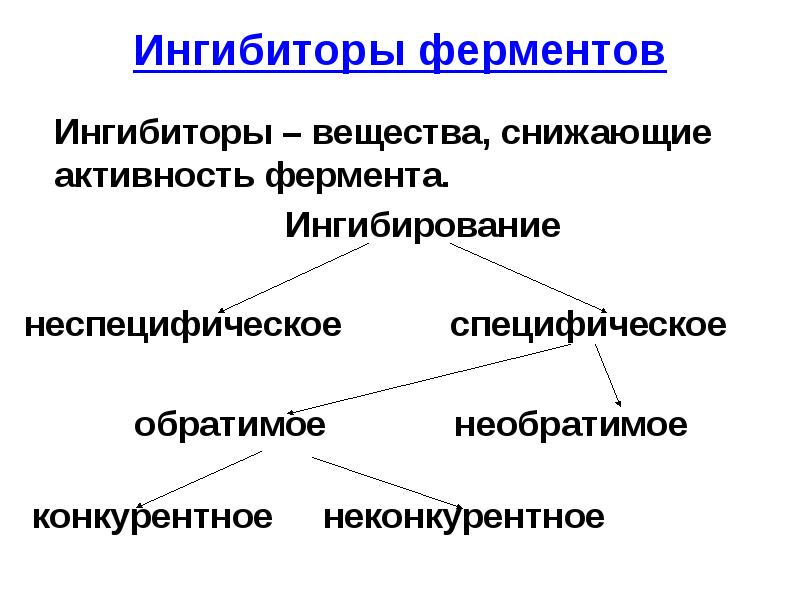
- 41. Ингибиторы ферментов Ингибиторы – вещества, снижающие активность фермента. Ингибирование
- 42. Неспецифическое Обусловлено денатурацией фермента под влиянием физических и химических факторов: to,
- 43. Специфическое Избирательный процесс, при котором I действует только на определенный фермент
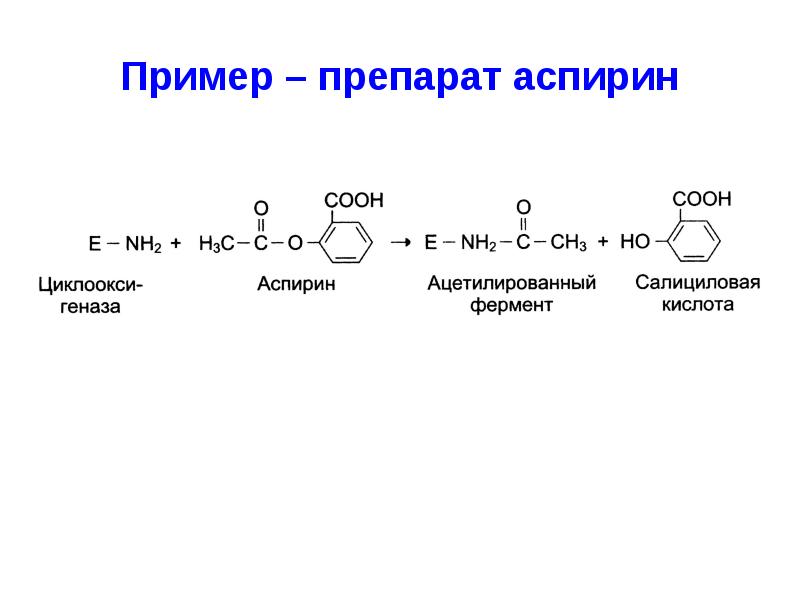
- 44. Пример – препарат аспирин
- 45. Обратимое I связывается с E нековалентными связями → [IE] легко
- 46. Конкурентное (изостерическое) I - структурный аналог S I связывается
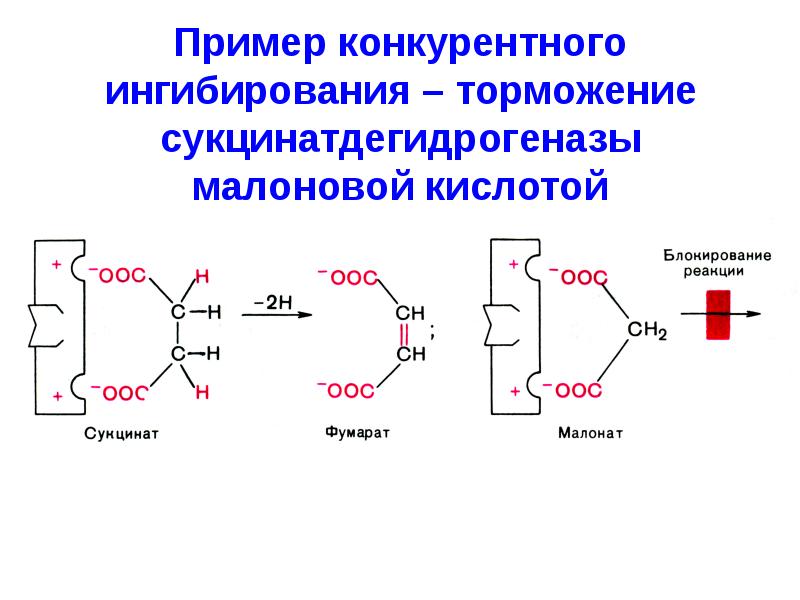
- 47. Пример конкурентного ингибирования – торможение сукцинатдегидрогеназы малоновой кислотой
- 48. Для устранения действия конкурентного I необходимо увеличить концентрацию S
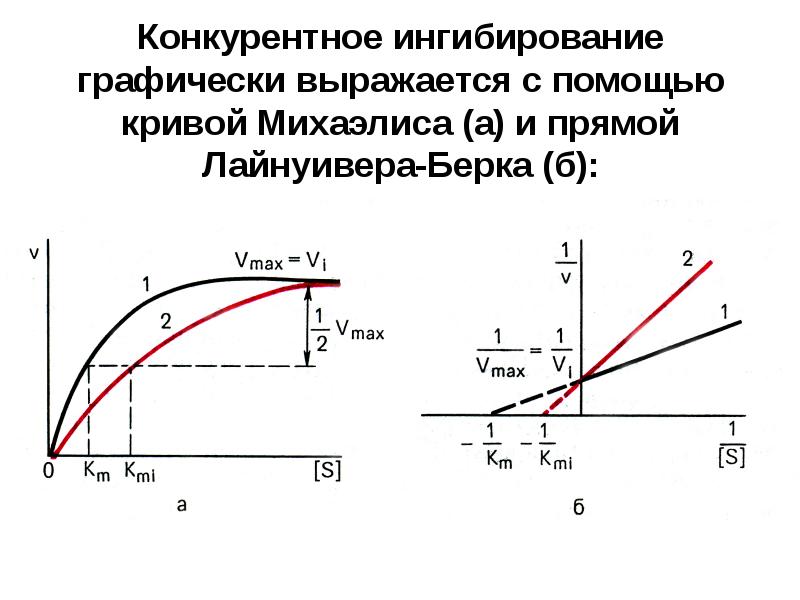
- 49. Конкурентное ингибирование графически выражается с помощью кривой Михаэлиса (а) и прямой
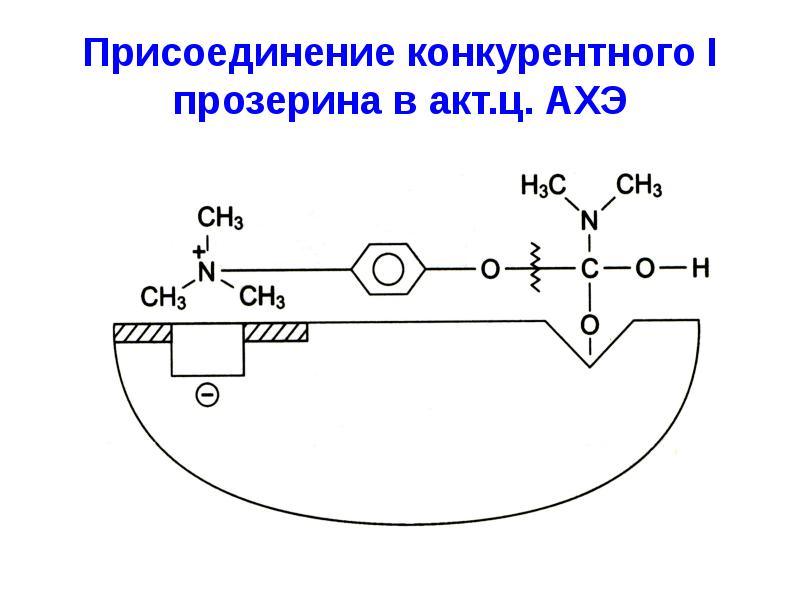
- 50. На принципе конкурентного ингибирования основано действие многих ЛВ, например, группа ацетилхолинэстеразных
- 51. Присоединение конкурентного I прозерина в акт.ц. АХЭ
- 52. Скачать презентацию








![При образовании [E-S] комплекса происходит перераспределение электронной плотности в S и При образовании [E-S] комплекса происходит перераспределение электронной плотности в S и](/documents_7/587c2cc00ba214820d3d8aac6ddc4455/img13.jpg)



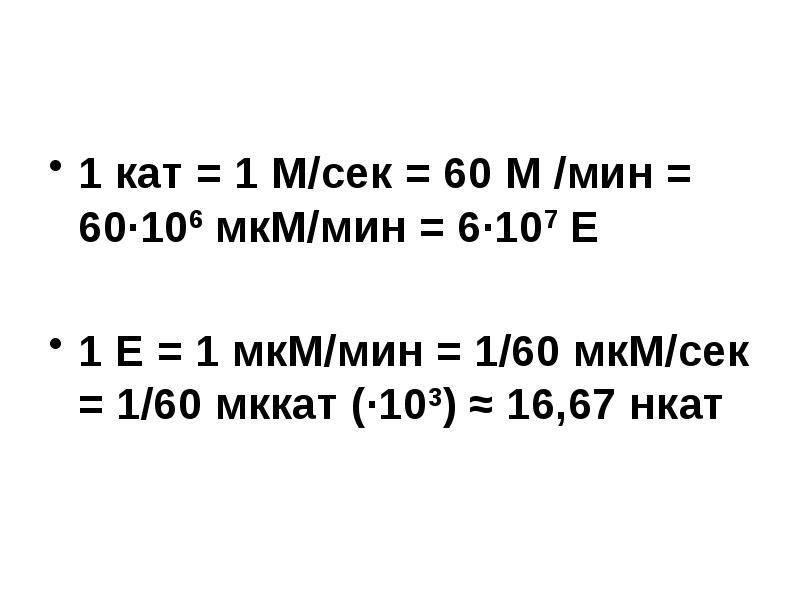






![Бриггс и Холдейн вывели математическое выражение зависимости V реакции от [S]:
Бриггс и Холдейн вывели математическое выражение зависимости V реакции от [S]:](/documents_7/587c2cc00ba214820d3d8aac6ddc4455/img26.jpg)
![Графическая зависимость V от [S] Графическая зависимость V от [S]](/documents_7/587c2cc00ba214820d3d8aac6ddc4455/img27.jpg)
![Возможно 3 варианта решения уравнения Михаэлиса:
1. [S] > Кm Возможно 3 варианта решения уравнения Михаэлиса:
1. [S] > Кm](/documents_7/587c2cc00ba214820d3d8aac6ddc4455/img28.jpg)
![Физический смысл Кm заключается в том, что Кm численно равна [S], Физический смысл Кm заключается в том, что Кm численно равна [S],](/documents_7/587c2cc00ba214820d3d8aac6ddc4455/img30.jpg)







![Обратимое
I связывается с E нековалентными связями → [IE] легко Обратимое
I связывается с E нековалентными связями → [IE] легко](/documents_7/587c2cc00ba214820d3d8aac6ddc4455/img44.jpg)



Слайды и текст этой презентации
Скачать презентацию на тему Различают две основные теории специфичности ферментов: можно ниже:
Похожие презентации





























