Ауыр металдар презентация
Содержание
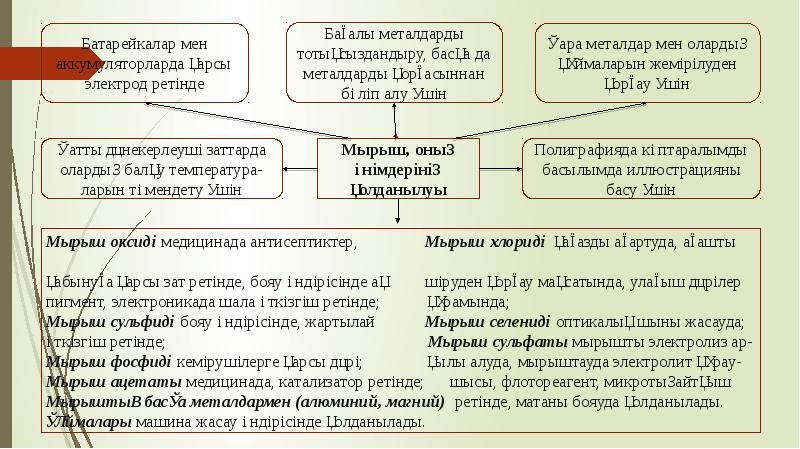
- 2. Мырыш Zn – химиялық элементтердің периодтық жүйесінде IІ топта, ІV периодта
- 3. Қорғасын Pb – химиялық элементтердің периодтық жүйесінде VI периодта, IV топта
- 4. Минералдары галенит PbS
- 5. Минералдары борнит Cu5FeS4 англезит
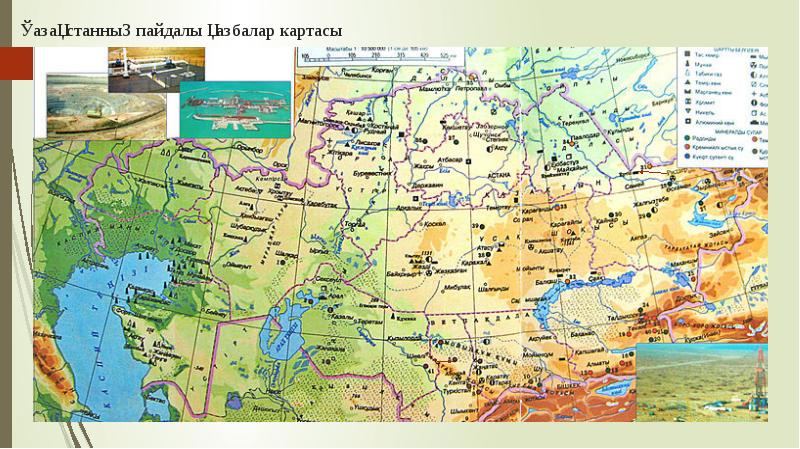
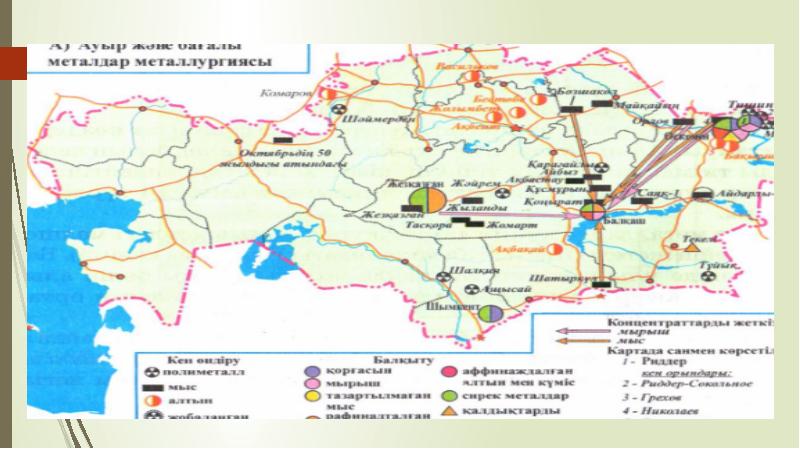
- 6. Қазақстанның пайдалы қазбалар картасы
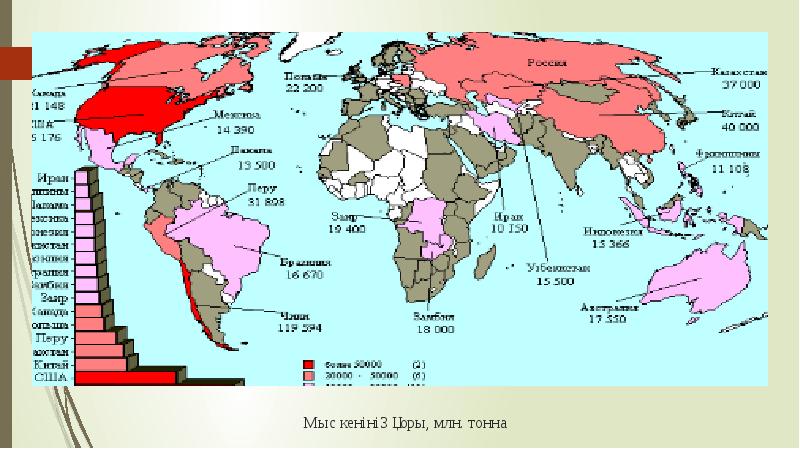
- 7. Мыс кенінің қоры, млн. тонна
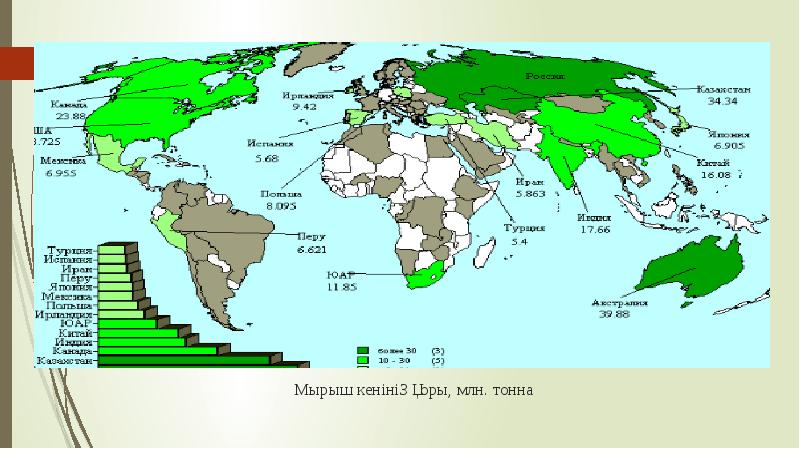
- 8. эээ
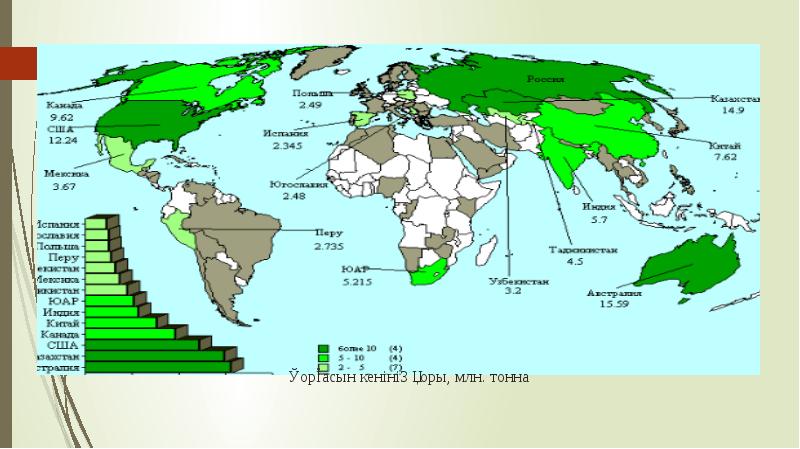
- 9. Қорғасын кенінің қоры, млн. тонна
- 10. Физикалық қасиеттері Мыс – алтын қызыл металл, ауада тез оксидті
- 11. Химиялық қасиеттері Мыс қосылыстарда +1, +2 тотығу дәрежелерін көрсетеді. +1
- 12. 3) Концентрлі ыстық күкірт қышқылымен әрекеттеседі:
- 13. 9) Сұйытылған тұз қышқылымен оттек қатысында әрекеттеседі:
- 14. Кен орындары Мыс-қорғасын-мырыш кендері Қазақстанда мына аумақтарда шоғырланған: 1)Шығыс Қазақстан
- 16. Мыс көптеген өндірістік, шаруашылық саларында қолданылады: 1) Электротехникада мыс сымдары энергия
- 19. Скачать презентацию












Слайды и текст этой презентации
Похожие презентации





























