Биологическое окисление презентация
Содержание
- 3. Биологическое окисление Биологическое окисление – это совокупность реакций окисления,
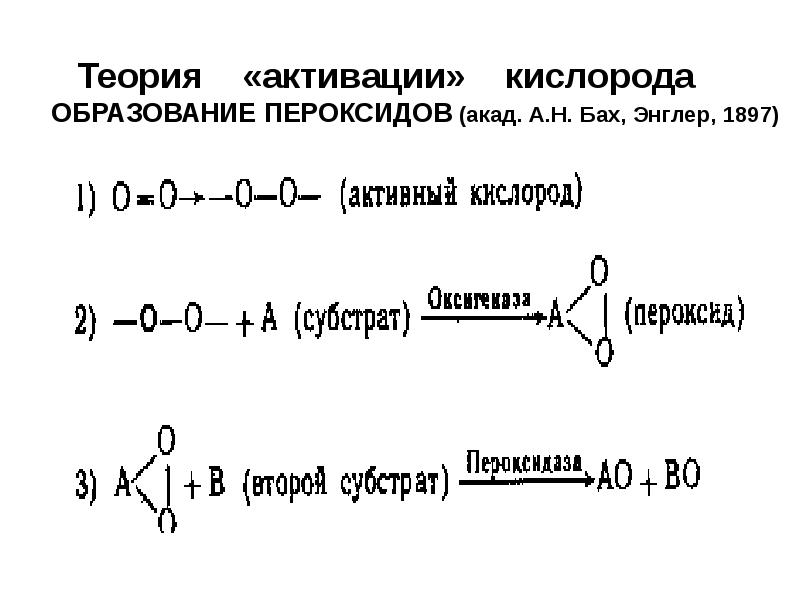
- 4. Теория «активации» кислорода ОБРАЗОВАНИЕ ПЕРОКСИДОВ (акад. А.Н. Бах, Энглер, 1897)
- 5. Варбург Варбург Активирование кислорода – ключевой процесс в тканевом дыхании 1912г
- 6. Теория активирования водорода Теория активирования водорода (акад. В.И. Палладин, 1912)
- 7. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ
- 8. Биологическое окисление Процесс транспорта электронов Процесс многоступенчатый Процесс
- 10. ФЕРМЕНТЫ И КОФЕРМЕНТЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ ФЕРМЕНТЫ И КОФЕРМЕНТЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- 11. Этап осуществляется с помощью: Этап осуществляется с помощью: НАД – зависимые
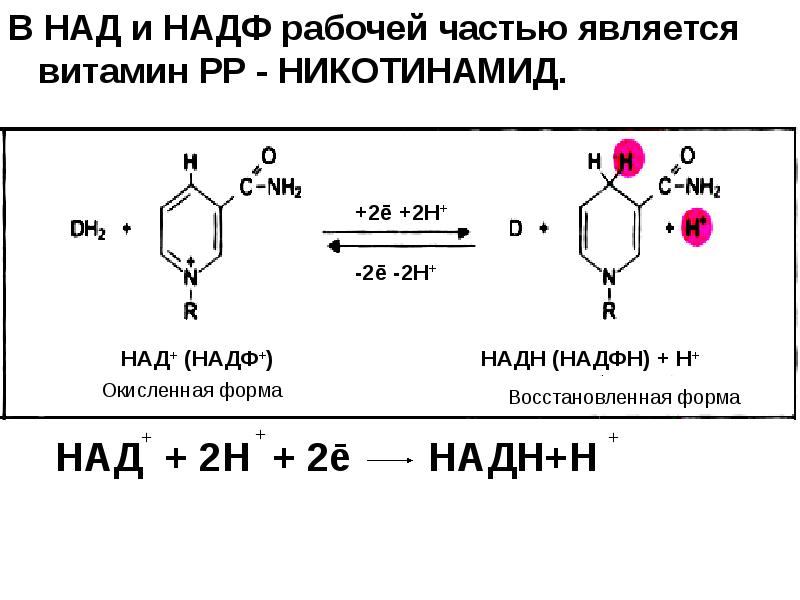
- 12. В НАД и НАДФ рабочей частью является витамин РР - НИКОТИНАМИД.
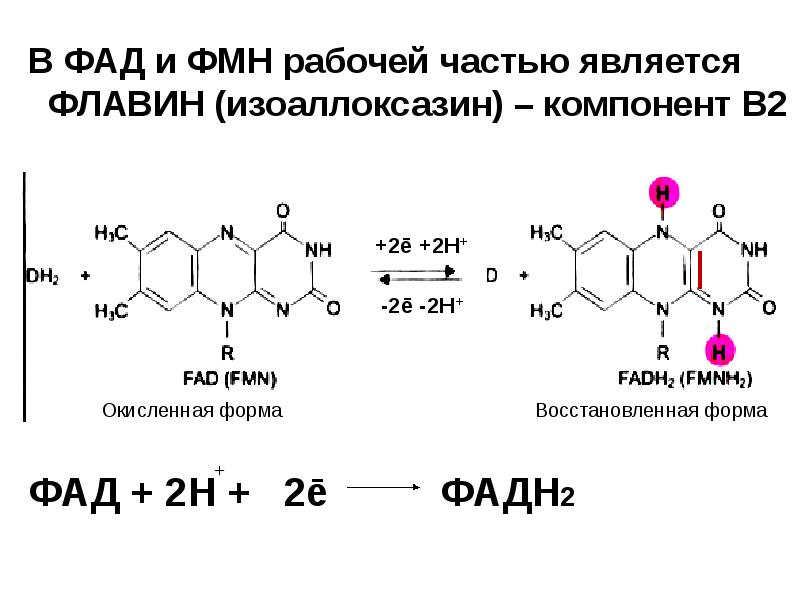
- 13. В ФАД и ФМН рабочей частью является ФЛАВИН (изоаллоксазин) –
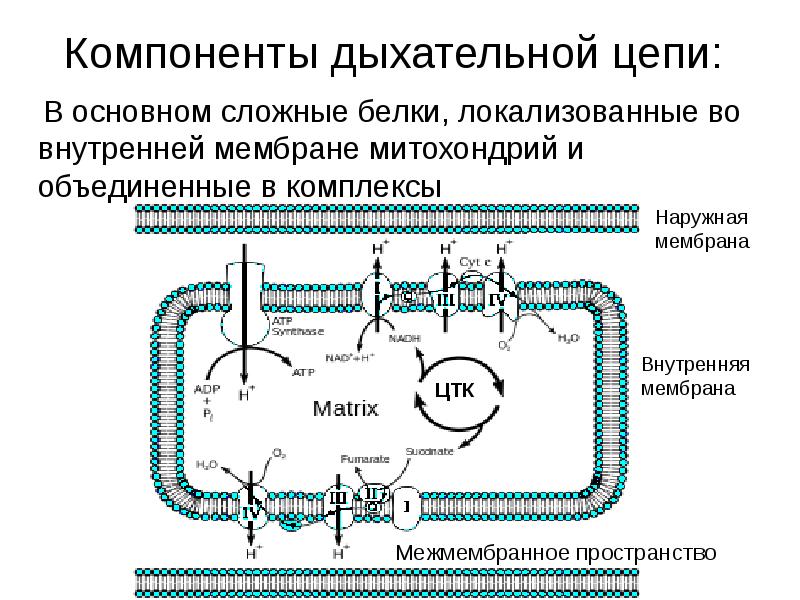
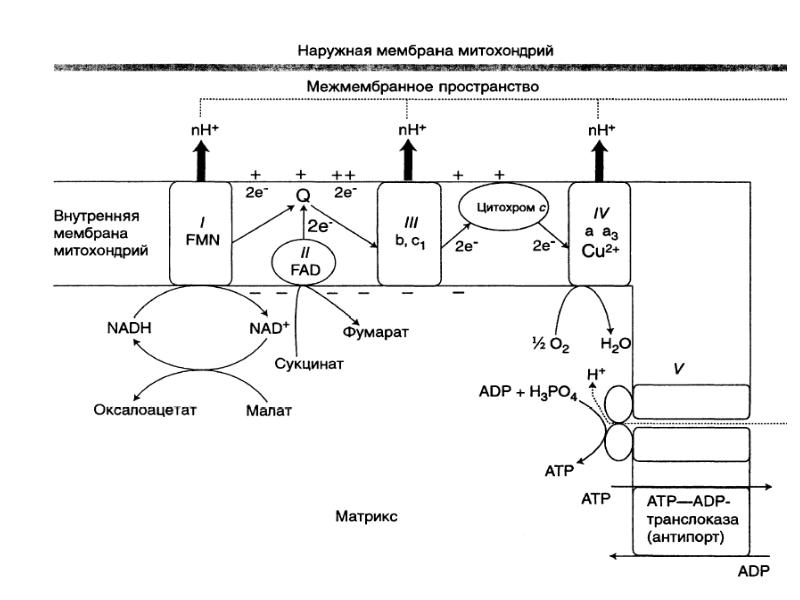
- 14. Компоненты дыхательной цепи: В основном сложные белки, локализованные во внутренней
- 15. Комплекс ферментов переноса электронов и протонов от субстрата к кислороду называется
- 16. Компоненты дыхательной цепи: В основном сложные белки, локализованные во внутренней мембране
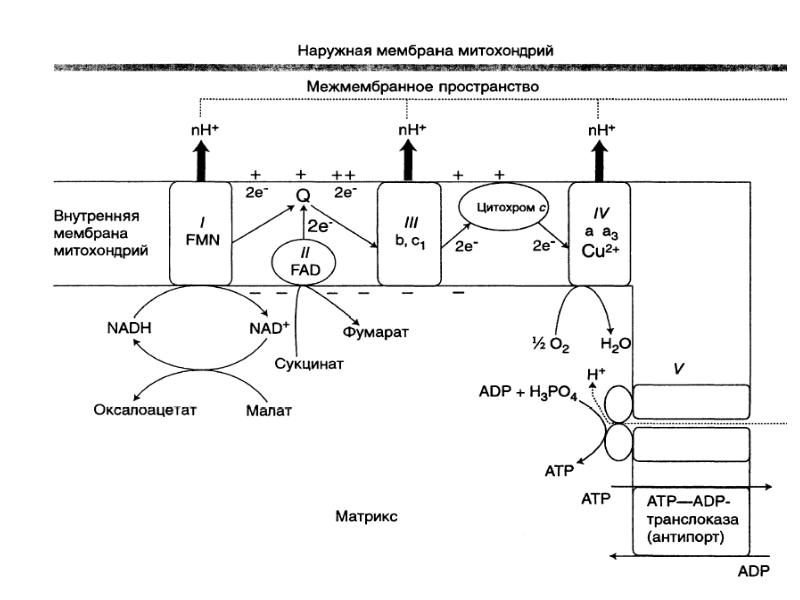
- 17. КОМПОНЕНТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ: Комплекс I (НАДН-дегидрогеназа) Комплекс II (СДГ)
- 18. Комплекс I (НАДН-дегидрогеназа) Флавинзависимый фермент (кофермент ФМН) Единственный Субстрат – кофермент
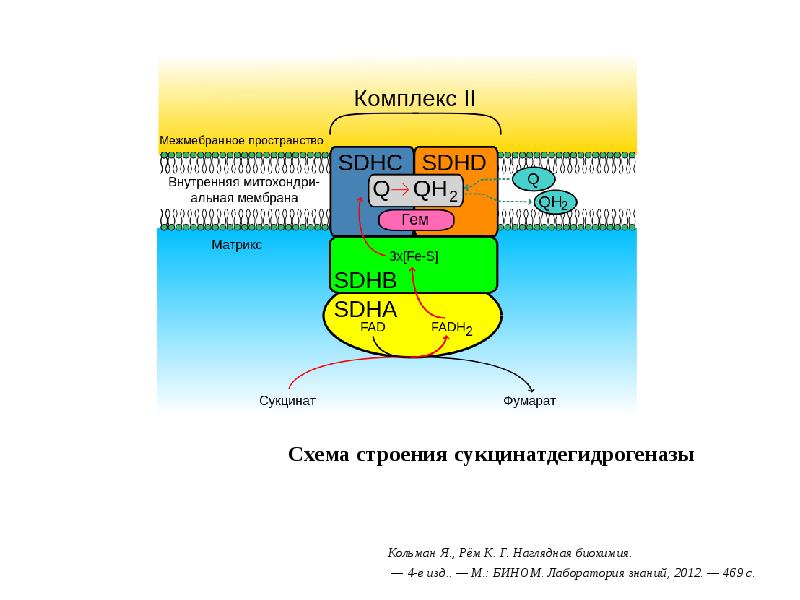
- 19. Комплекс II (СДГ) Флавинзависимый фермент (кофермент ФАД) Донор протонов и электронов
- 20. Схема строения сукцинатдегидрогеназы Кольман Я., Рём К. Г. Наглядная биохимия. — 4-е
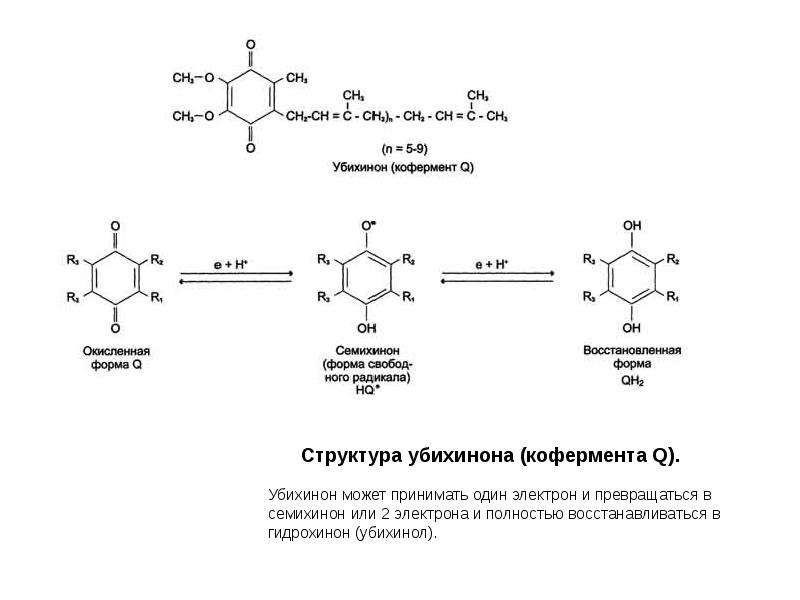
- 21. Убихинон (кофермент Q) Quinone – хинон Ubiquitos – вездесущий У млекопитающих
- 22. Структура убихинона (кофермента Q). Убихинон может принимать один электрон и превращаться
- 23. Цитохромы – сложные белки, небелковая часть – гем Цитохромы – сложные
- 24. Комплекс III (коэнзим Q – дегидрогеназа) В составе цитохромы b, с1
- 25. Цитохром с Не объединяется в комплекс Акцептор электронов от комплекса III
- 26. Комплекс IV (цитохромоксидаза) Содержит цитохромы а, а3, ионы меди Акцептор электронов
- 28. Полная ЭТЦ - взаимодействие субстрата с НАД. Укороченная ЭТЦ -
- 29. Окислительно-восстановительный потенциал *Выражается в вольтах; *Чем отрицательнее E0´, тем меньше сродство
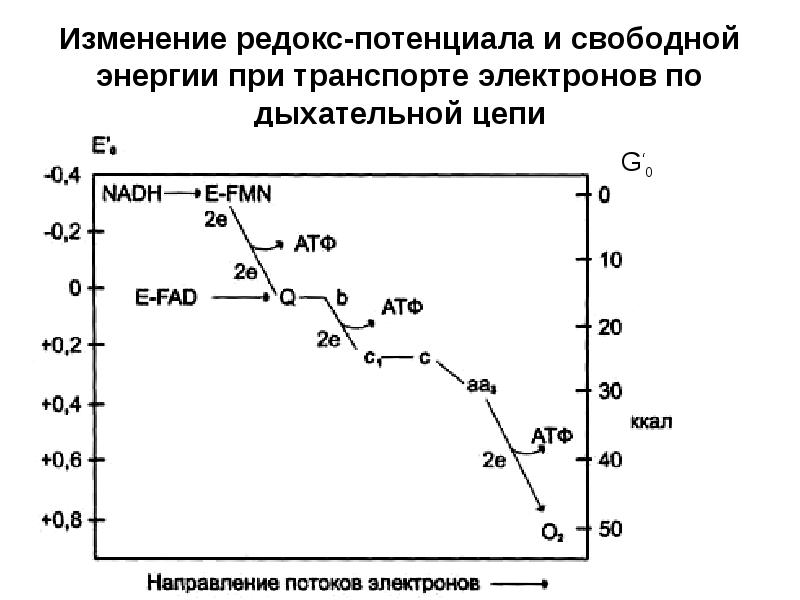
- 30. Изменение редокс-потенциала и свободной энергии при транспорте электронов по дыхательной цепи
- 31. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ. Процесс образования АТФ из АДФ и Н3РО4
- 32. В дыхательной цепи выделяются 3 пункта, где может образоваться АТФ: 1.НАД
- 33. МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Теория ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
- 34. Основные положения теории: Основные положения теории: 1.Мембрана МИТОХОНДРИЙ непроницаема для
- 35. Процесс транспорта электронов происходит во внутренней мембране. Процесс транспорта электронов
- 37. Во время дыхания создаётся ЭЛЕКТРО-ХИМИЧЕСКИЙ потенциал:
- 38. Электрический и концентрационный потенциал составляют ПРОТОНДВИЖУЩУЮ силу, которая перемещает протоны обратно
- 39. УСЛОВИЯ ОБРАЗОВАНИЯ АТФ: УСЛОВИЯ ОБРАЗОВАНИЯ АТФ: 1. Целостность мембраны -
- 40. СОПРЯЖЕНИЕ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ. разобщение ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ (свободное окисление)
- 41. Разобщение ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Разобщение ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ (свободное окисление)
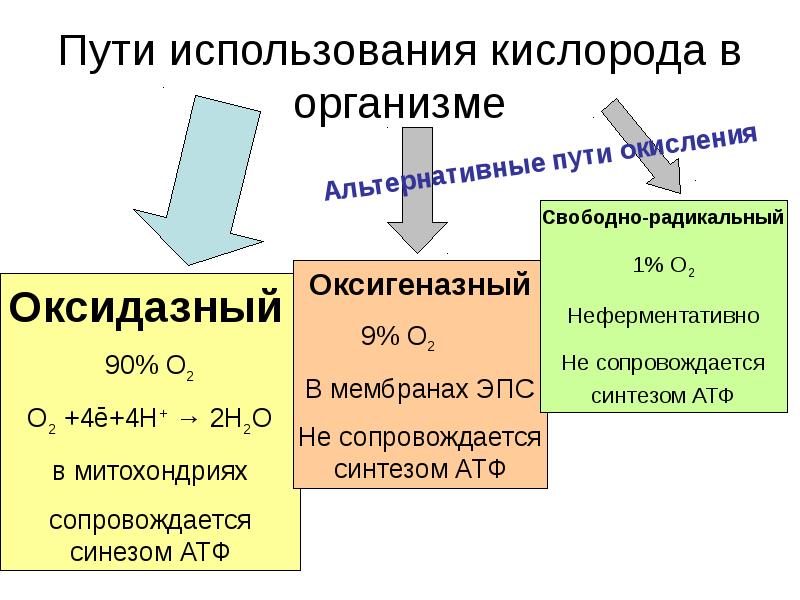
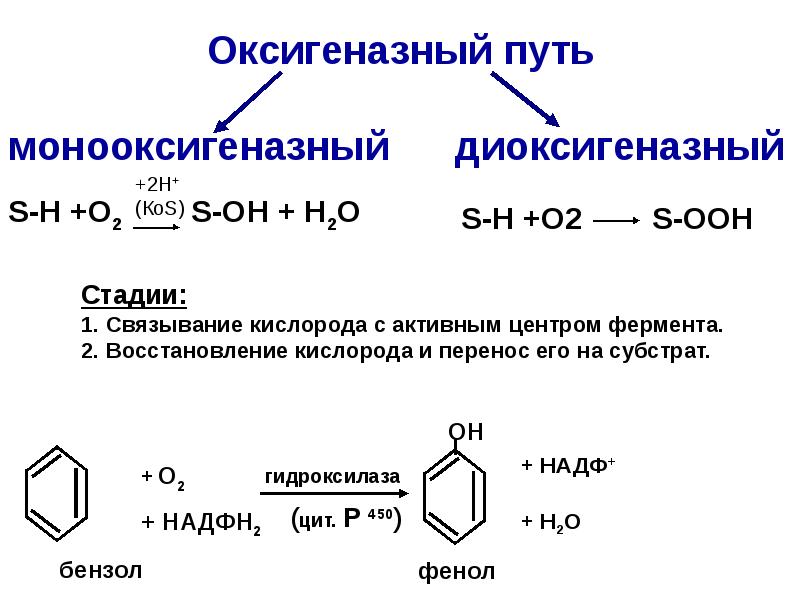
- 42. Пути использования кислорода в организме
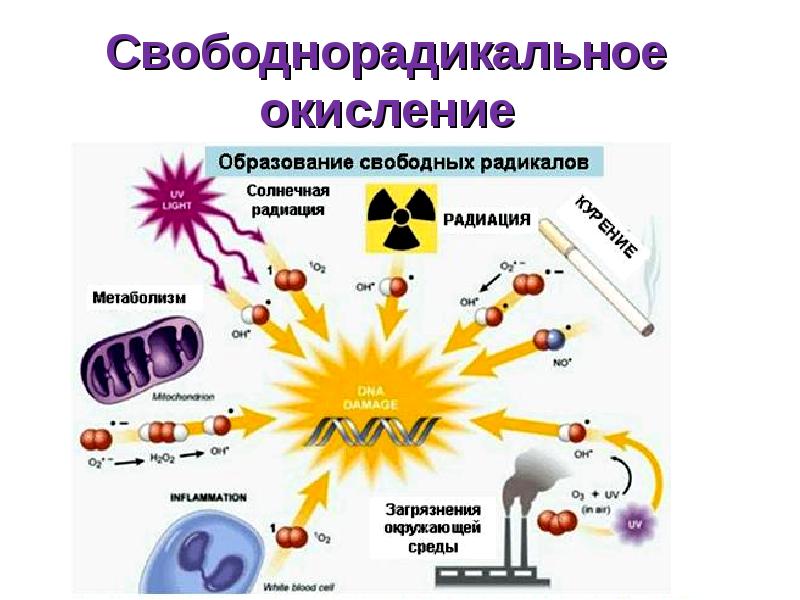
- 44. Свободнорадикальное окисление
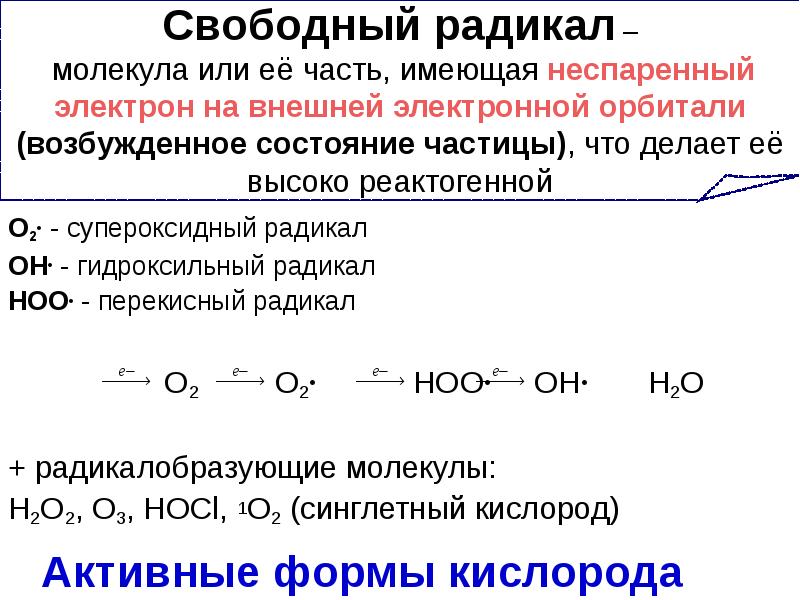
- 45. Свободный радикал – молекула или её часть, имеющая неспаренный электрон на
- 46. Источники свободных радикалов микросомальное окисление, окисление аминокислот, нуклеотидов оксидазами, неполное
- 47. Свойства свободных радикалов Являются нестабильными, короткоживущими молекулами Обладают очень высокой
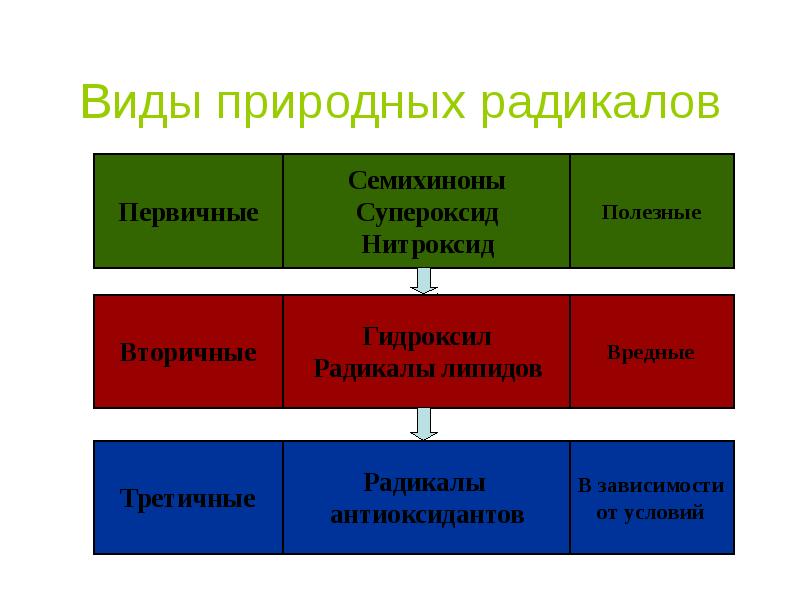
- 48. Виды природных радикалов
- 49. Значение процессов свободно-радикального окисления В НОРМЕ изменение свойств мембран; Фагоцитоз;
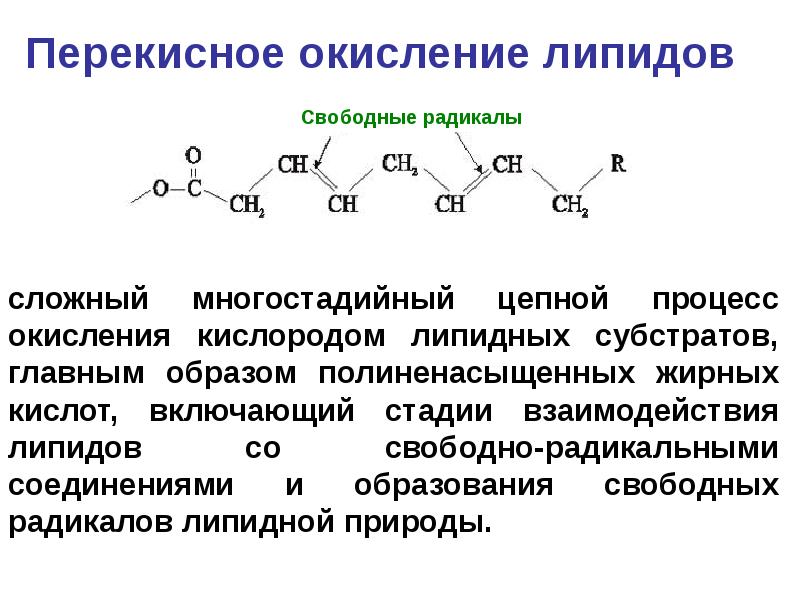
- 50. Перекисное окисление липидов
- 51. Основные стадии перекисного окисления липидов (ПОЛ) инициирование цепной реакции; развитие и
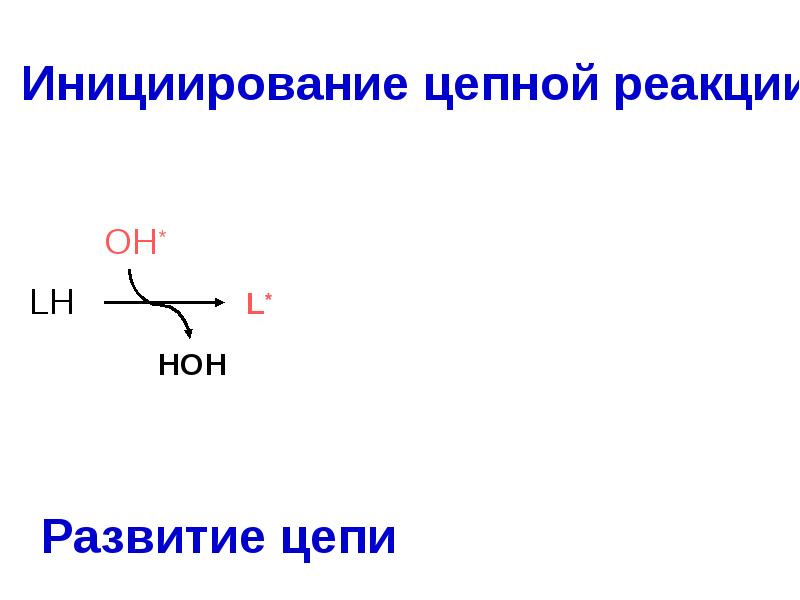
- 52. Инициирование цепной реакции
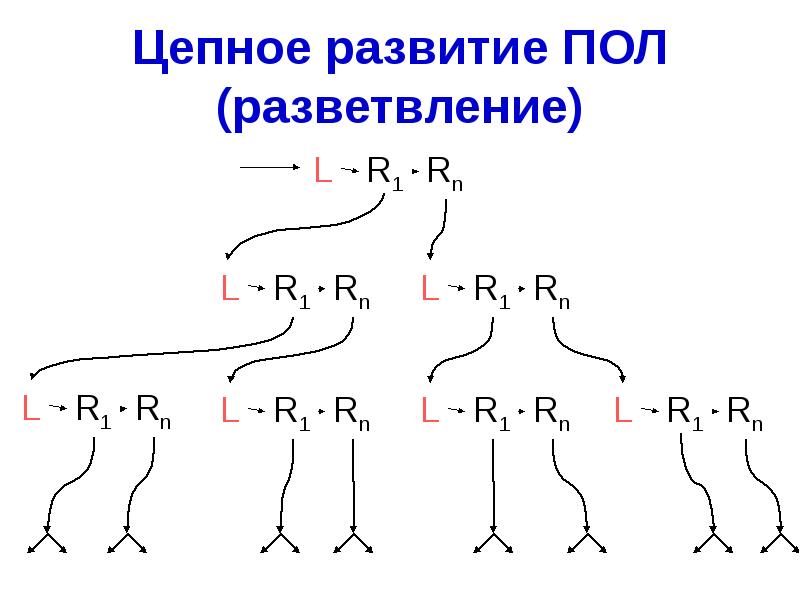
- 53. Цепное развитие ПОЛ (разветвление)
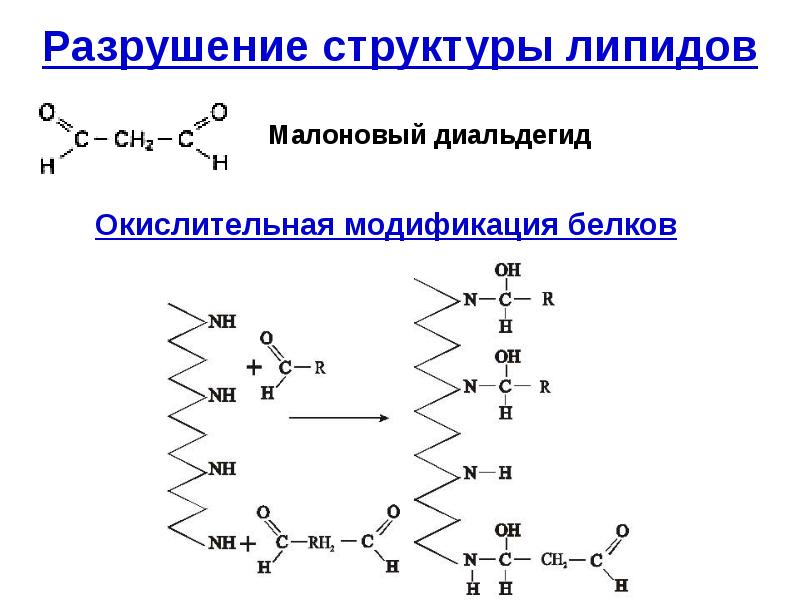
- 54. Разрушение структуры липидов
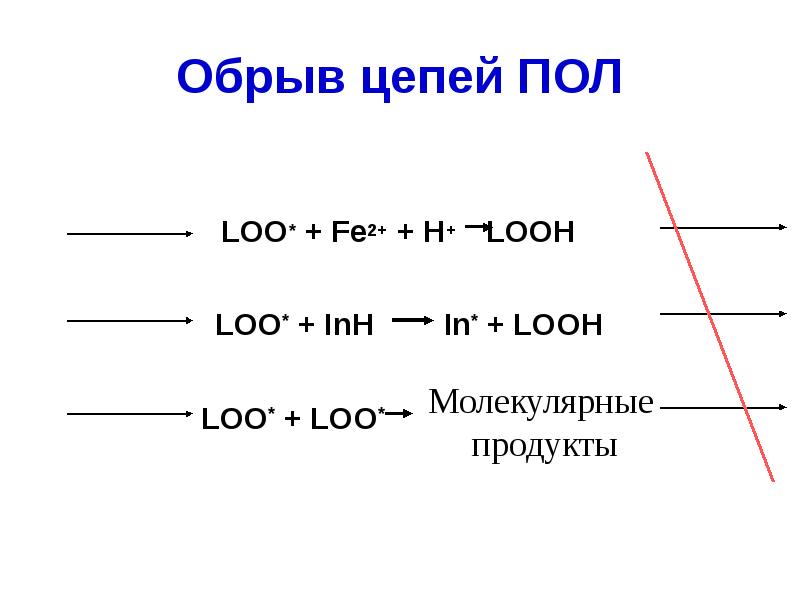
- 55. Обрыв цепей ПОЛ LOO* + Fe2+ + H+ LOOH
- 56. Механизмы защиты от свободных радикалов Предусматривают наличие в клетках антиоксидантной
- 57. Ферментативная антиоксидантная система Супероксиддисмутаза Каталаза Глутатионзависимые ферменты: Глутатионпероксидаза Глутатионредуктаза
- 58. Неферментативная антиоксидантная система Витамины: Е (токоферол), С (аскорбат),биофлавоноиды Пептиды и
- 60. Выдвигается теория Q-цикла транспорта протонов. Выдвигается теория Q-цикла транспорта протонов.
- 61. Скачать презентацию









































Слайды и текст этой презентации
Похожие презентации





























