Дисперсные системы. Способы получения и очистки коллоидных систем. (Лекция 5) презентация
Содержание
- 2. 1. Основные понятия. Классификация дисперсных систем. Дисперсной системой называется система,
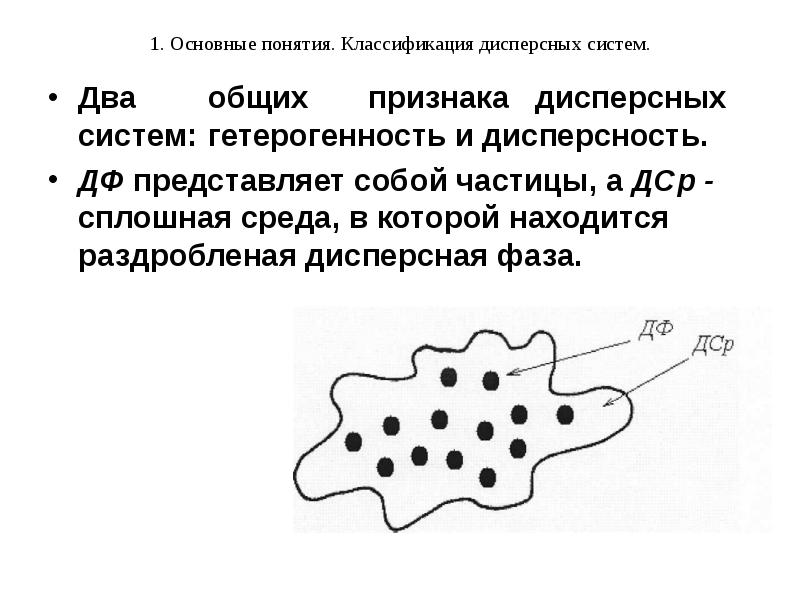
- 3. 1. Основные понятия. Классификация дисперсных систем. Два общих признака дисперсных систем: гетерогенность и дисперсность.
- 4. 1. Основные понятия. Классификация дисперсных систем. Количественные характеристики ДФ Поперечный размер
- 5. 1. Основные понятия. Классификация дисперсных систем. Удельная поверхность Удельная поверхность для
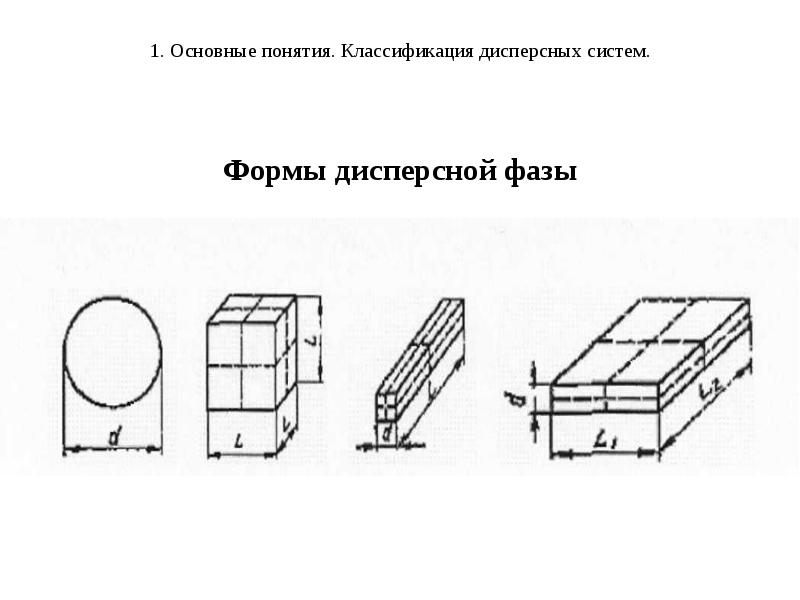
- 6. 1. Основные понятия. Классификация дисперсных систем. Формы дисперсной фазы
- 7. 1. Основные понятия. Классификация дисперсных систем. Важным свойством ДС является наличие
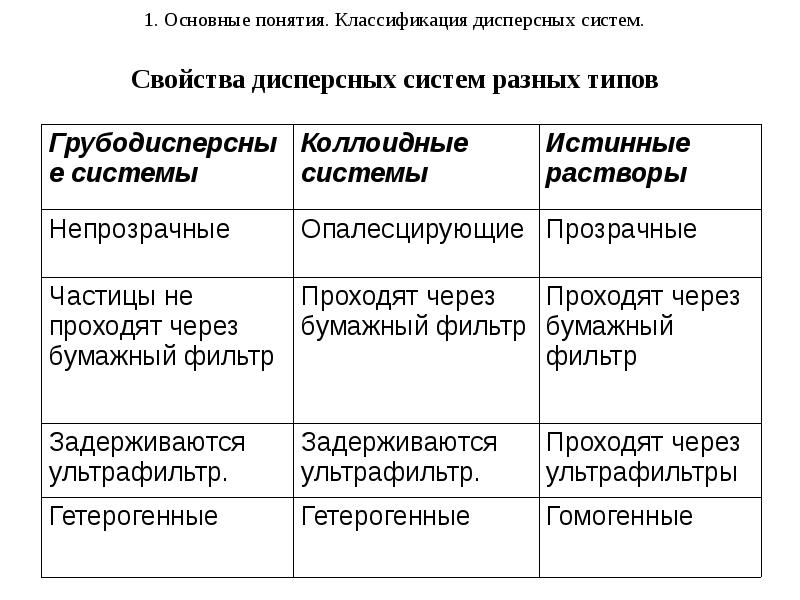
- 8. 1. Основные понятия. Классификация дисперсных систем. Свойства дисперсных систем разных типов
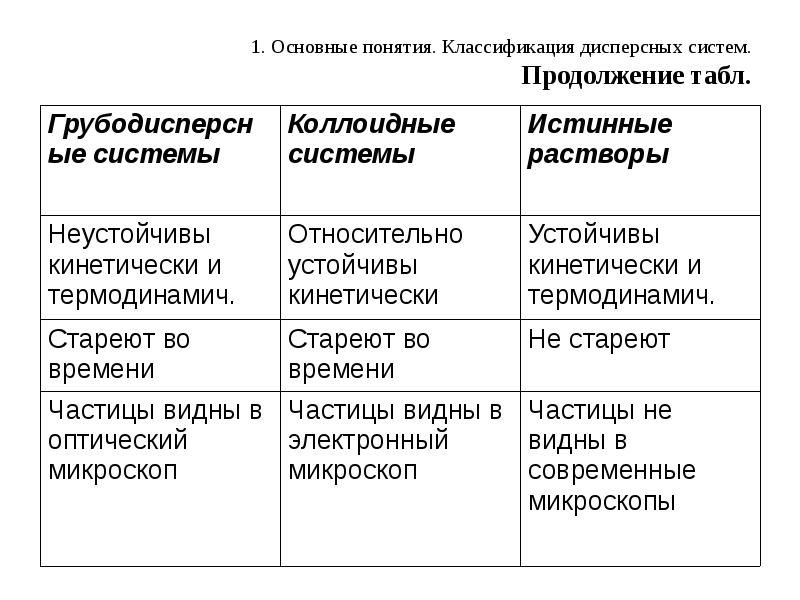
- 9. 1. Основные понятия. Классификация дисперсных систем. Продолжение табл.
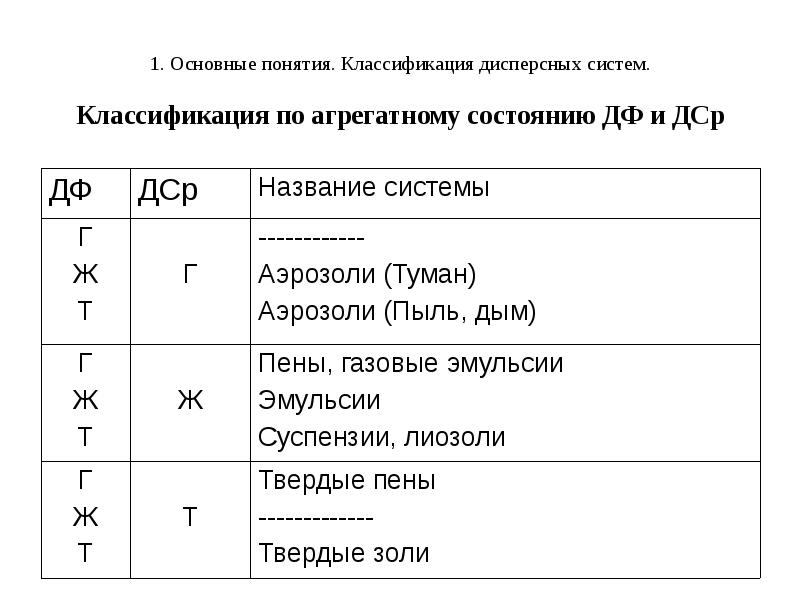
- 10. 1. Основные понятия. Классификация дисперсных систем. Классификация по агрегатному состоянию ДФ
- 11. 1. Основные понятия. Классификация дисперсных систем. Классификация по степени связи ДС
- 12. 1. Основные понятия. Классификация дисперсных систем. Лиофильные системы образуются самопроизвольно, следовательно,
- 13. 1. Основные понятия. Классификация дисперсных систем. Классификация по взаимодействию частиц:
- 14. 1. Основные понятия. Классификация дисперсных систем. Гель – структурированный коллоидный
- 15. 1. Основные понятия. Классификация дисперсных систем. Особое место в классификации
- 16. 2. Коллоидные растворы: строение мицеллы золя Согласно общепринятой мицеллярной
- 17. 2. Коллоидные растворы: строение мицеллы золя Рассмотрим строение мицеллы на примере
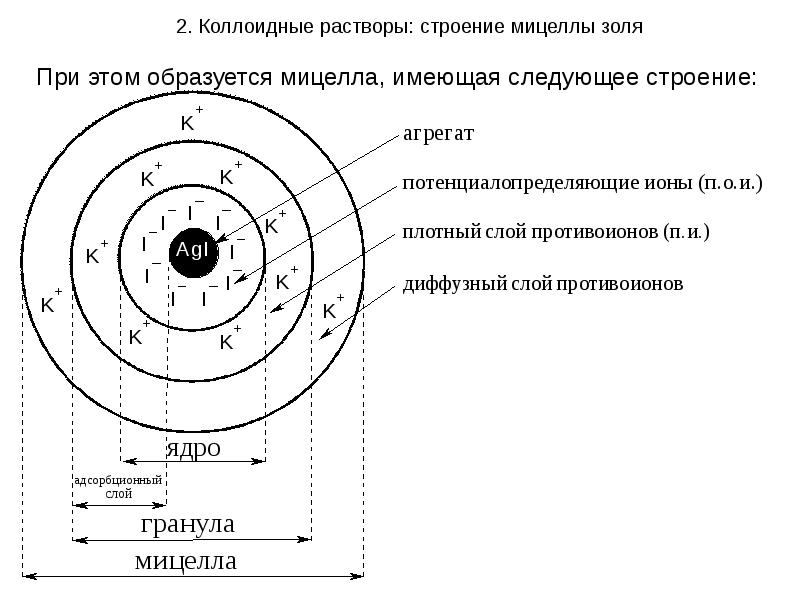
- 18. 2. Коллоидные растворы: строение мицеллы золя При этом образуется мицелла, имеющая
- 19. 2. Коллоидные растворы: строение мицеллы золя Осадок AgI является агрегатом мицеллы.
- 20. 2. Коллоидные растворы: строение мицеллы золя Потенциалопределяющие ионы и противоионы плотного
- 21. 2. Коллоидные растворы: строение мицеллы золя Составим формулу мицеллы AgI в
- 22. 3. Методы получения коллоидных растворов Коллоидные системы занимают промежуточное положение
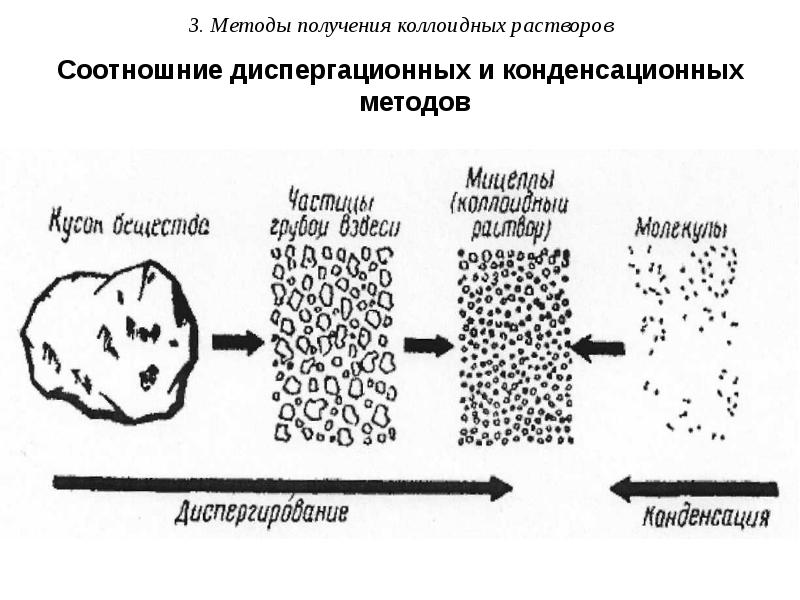
- 23. 3. Методы получения коллоидных растворов Соотношние диспергационных и конденсационных методов
- 24. 3. Методы получения коллоидных растворов Методы диспергирования (от лат. –
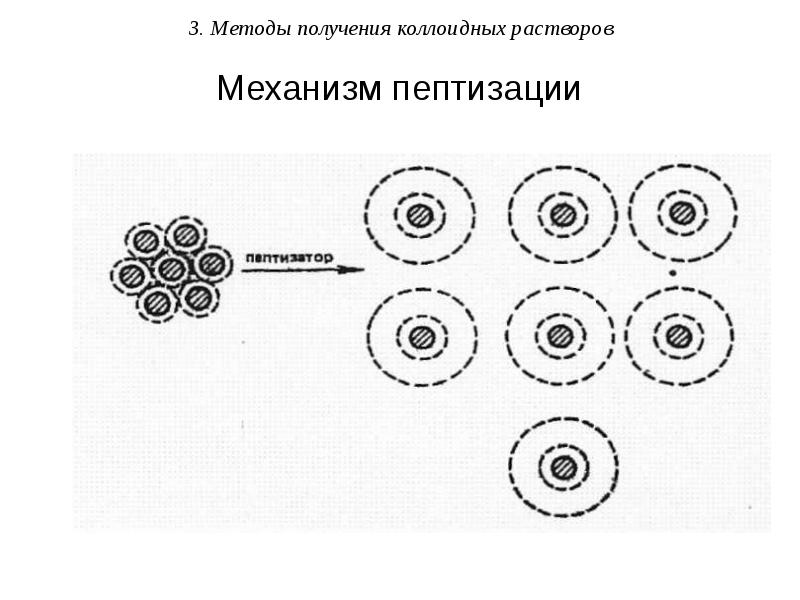
- 25. 3. Методы получения коллоидных растворов Механизм пептизации
- 26. 3. Методы получения коллоидных растворов Примером пептизации может служить переход
- 27. 3. Методы получения коллоидных растворов Строение мицеллы полученного золя
- 28. 3. Методы получения коллоидных растворов Конденсационные методы (от лат. – укрупнять)
- 29. 3. Методы получения коллоидных растворов Химическая конденсация – для получения
- 30. 3. Методы получения коллоидных растворов чтобы вещество ДФ было нерастворимо в
- 31. 3. Методы получения коллоидных растворов Примеры реакций химической конденсации
- 32. 4. Методы очистки коллоидных растворов Коллоидные растворы, как и истинные, хорошо
- 33. 4. Методы очистки коллоидных растворов Диализ проводят с помощью прибора -
- 34. 4. Методы очистки коллоидных растворов
- 35. 4. Методы очистки коллоидных растворов С помощью компенсационного диализа можно количественно
- 36. 4. Методы очистки коллоидных растворов По принципу компенсационного диализа работает аппарат
- 37. 4. Методы очистки коллоидных растворов Для очистки коллоидных растворов от грубодисперсных
- 38. 4. Методы очистки коллоидных растворов Прибор для ультрафильтрации: 1 -
- 39. 4. Методы очистки коллоидных растворов Для разделения частиц ДФ, имеющих различную
- 40. Скачать презентацию































Слайды и текст этой презентации
Скачать презентацию на тему Дисперсные системы. Способы получения и очистки коллоидных систем. (Лекция 5) можно ниже:
Похожие презентации





























