Элементы физической кинетики презентация
Содержание
- 2. 1. Явления переноса в газах 1. Явления переноса в газах
- 8. 2. Число столкновений и средняя длина свободного пробега молекул в газах
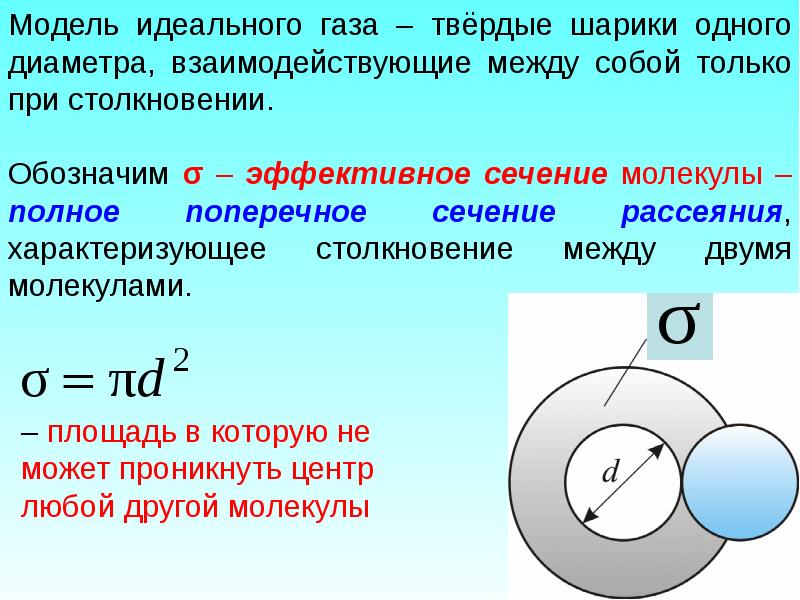
- 9. Расстояние, проходимое молекулой в среднем без столкновений, называется средней длиной свободного
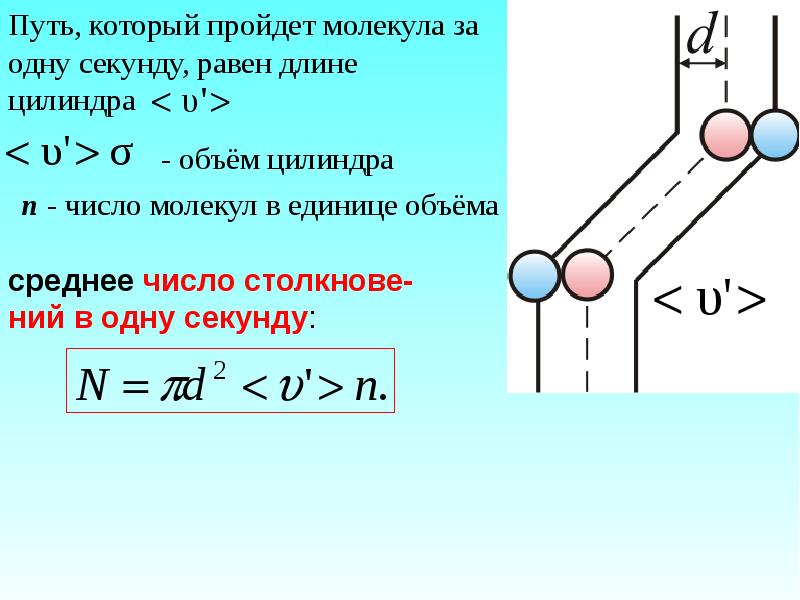
- 11. За одну секунду молекула проходит путь, равный средней арифметической скорости
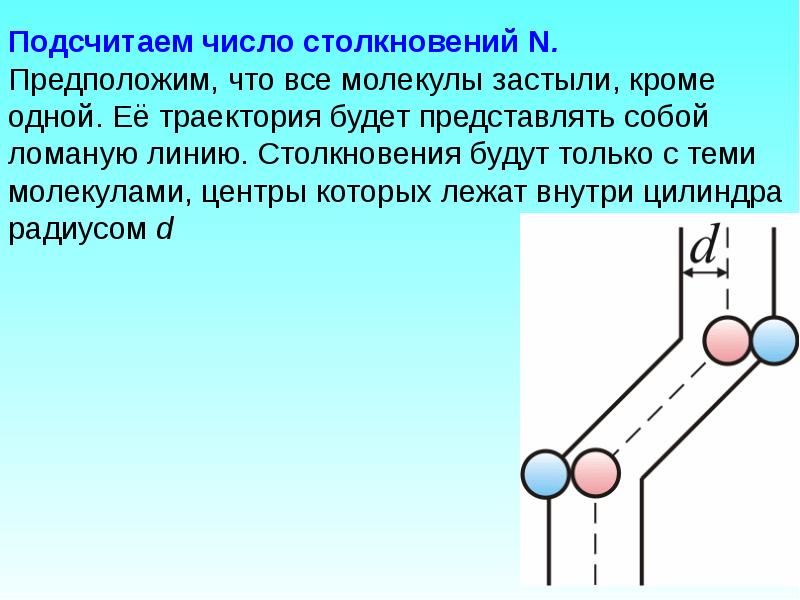
- 12. Подсчитаем число столкновений N. Предположим, что все молекулы застыли, кроме одной.
- 14. Все молекулы движутся, поэтому число соударений определяется средней скоростью движения молекул
- 15. Из уравнения состояния идеального газа выразим n через давление P и
- 16. Таким образом, при заданной температуре, средняя длина свободного пробега обратно пропорциональна
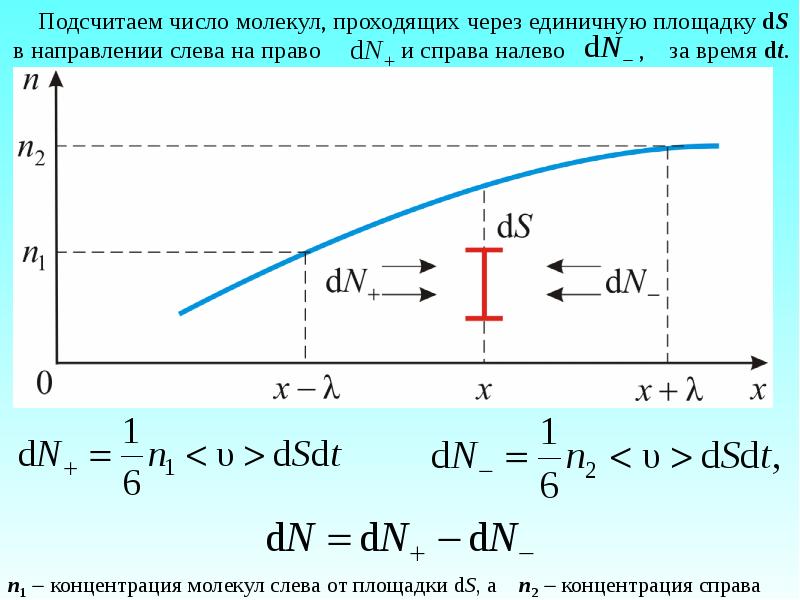
- 17. 3. Диффузия газов 3. Диффузия газов Диффузия
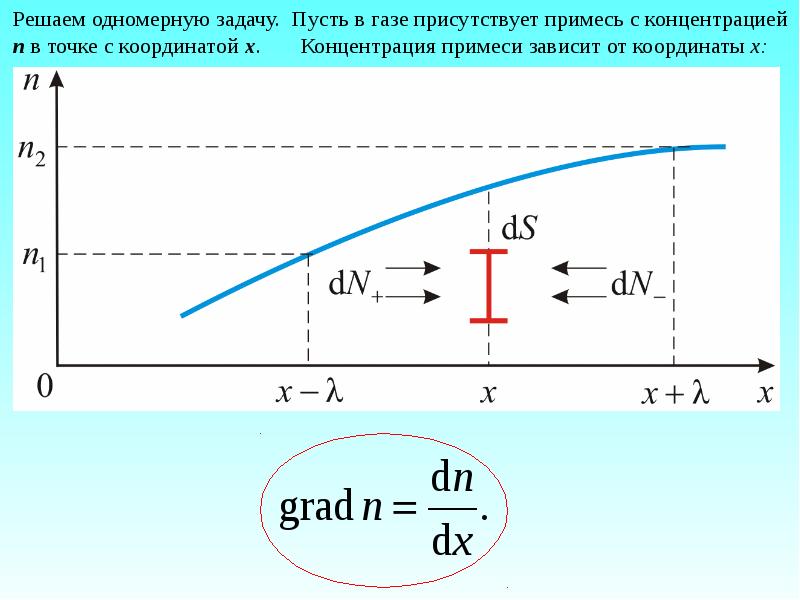
- 20. Градиент концентрации, в общем случае равен
- 22. Результирующий диффузионный поток через единицу площади в единицу времени:
- 23. Обозначим: – коэффициент диффузии. Тогда
- 24. Из уравнения Фика видно, что
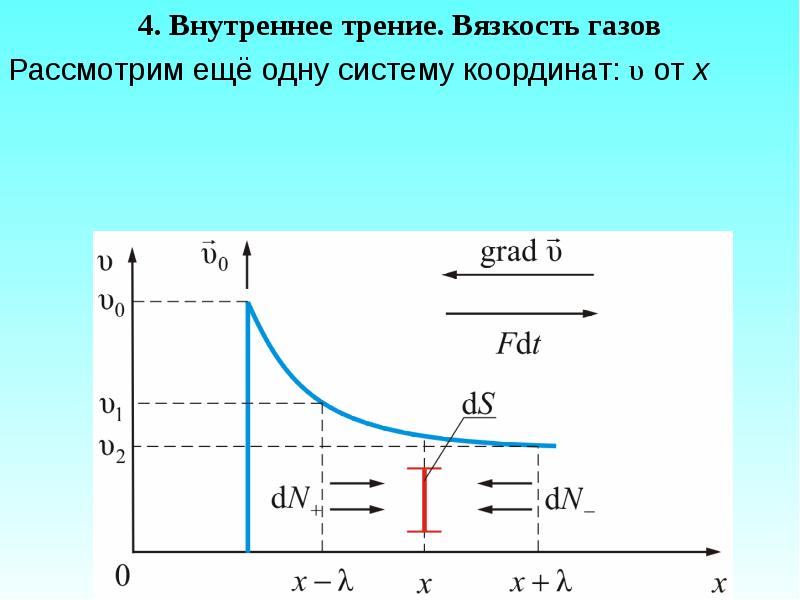
- 25. 4. Внутреннее трение. Вязкость газов 4. Внутреннее трение. Вязкость газов Рассмотрим
- 26. Пусть в покоящемся газе вверх, перпендикулярно оси х движется пластинка со
- 27. Каждая молекула газа в слое принимает участие в двух движениях: тепловом
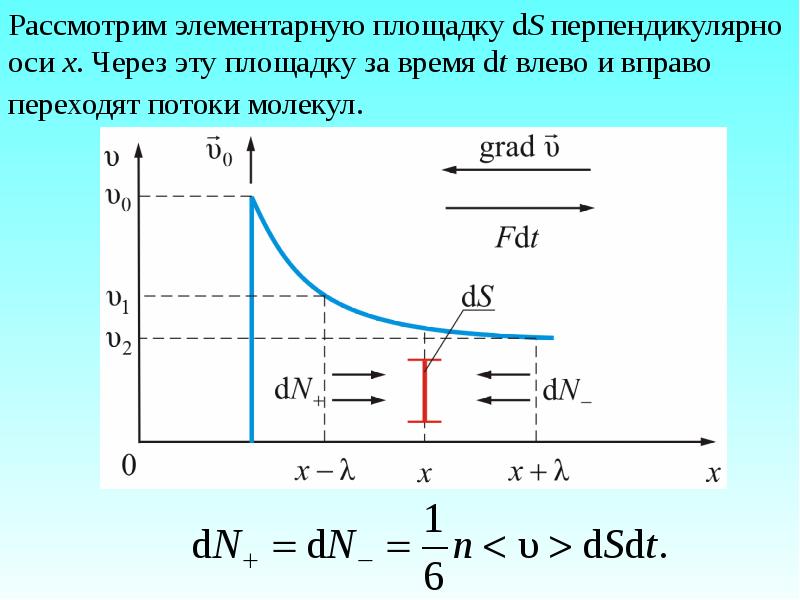
- 29. Рассмотрим элементарную площадку dS перпендикулярно оси х. Через эту площадку за
- 30. Но эти потоки переносят разный импульс:
- 31. Закон вязкости был открыт И. Ньютоном в 1687 г. Переносимый за
- 32. Сила, действующая на единицу площади поверхности, разделяющей два соседних слоя газа:
- 33. Физический смысл коэффициента вязкости η в том, что он численно равен
- 34. 5. Теплопроводность газов 5. Теплопроводность газов Учение о теплопроводности начало развиваться
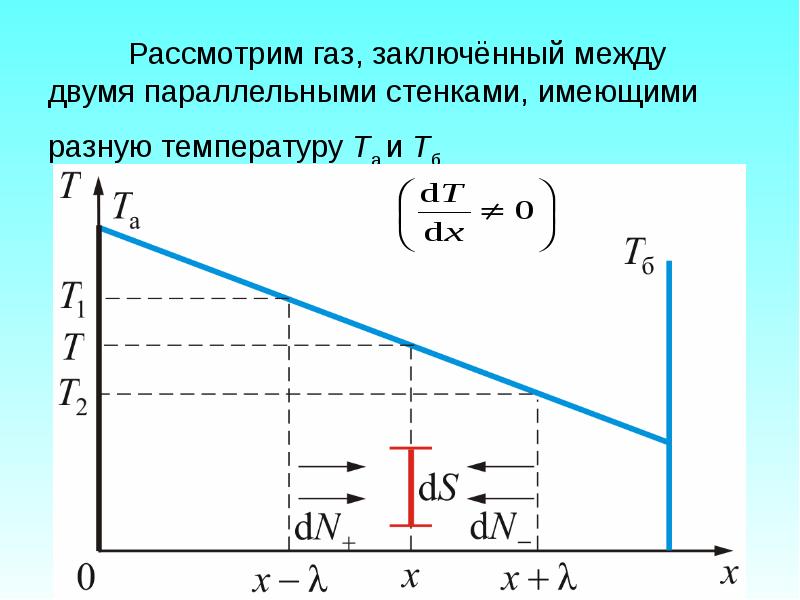
- 35. Рассмотрим газ, заключённый между двумя параллельными стенками, имеющими разную температуру Та
- 36. Итак, у нас имеется градиент температуры
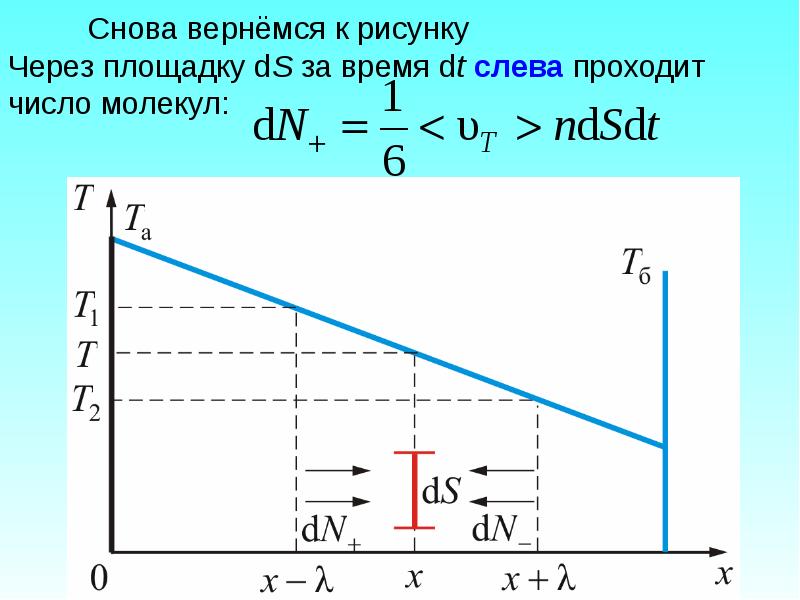
- 38. Снова вернёмся к рисунку Через площадку dS за время dt слева
- 39. Средняя энергия этих молекул К – соответствует значению энергии в том
- 40. Результирующий поток энергии через dS равен разности потоков и
- 41. или
- 42. υТ – тепловая скорость молекул; – удельная
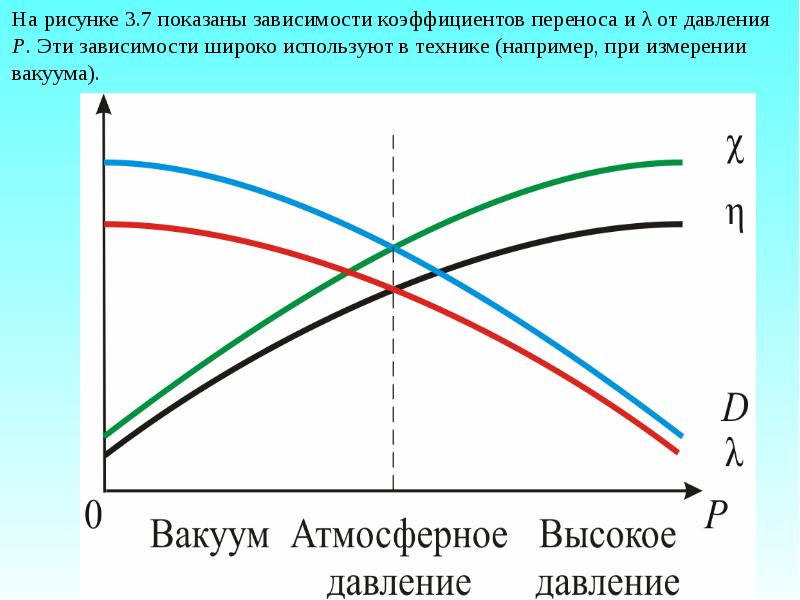
- 46. Так как скорость теплового движения молекул и
- 47. С ростом давления λ уменьшается и затрудняется диффузия (
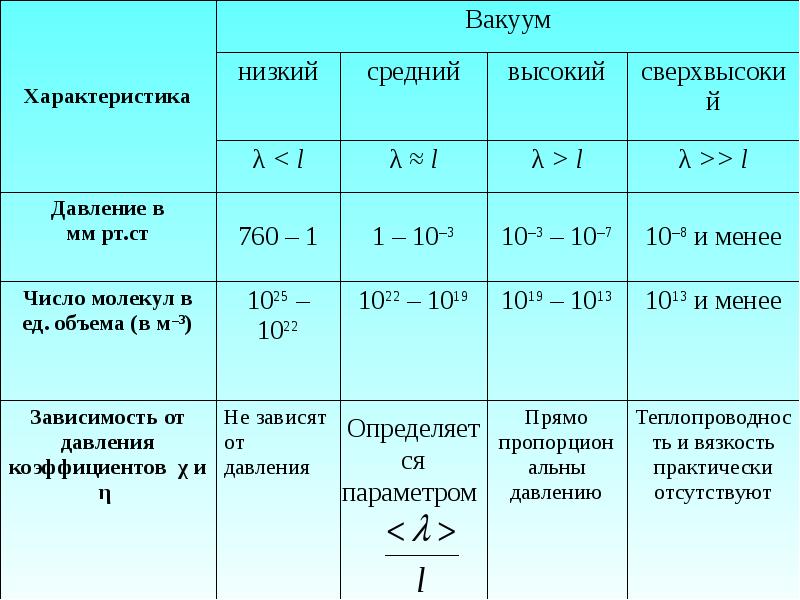
- 49. Молекулярное течение – течение газов в условиях вакуума, то есть когда
- 50. Как при молекулярном течении, как и при эффузии, количество протекающего в
- 51. Газ называется разреженным, если его плотность столь мала, что средняя длина
- 54. Удельный тепловой поток в сильно разряженных газах пропорционален разности температур и
- 55. Если Т1 и Т2 – температуры газа в сосудах, то предыдущее
- 56. Скачать презентацию












































Слайды и текст этой презентации
Похожие презентации





























