Физическая химия дисперсных систем презентация
Содержание
- 2. План лекции Оптические свойства коллоидных растворов Строение коллоидной частицы Условия получения
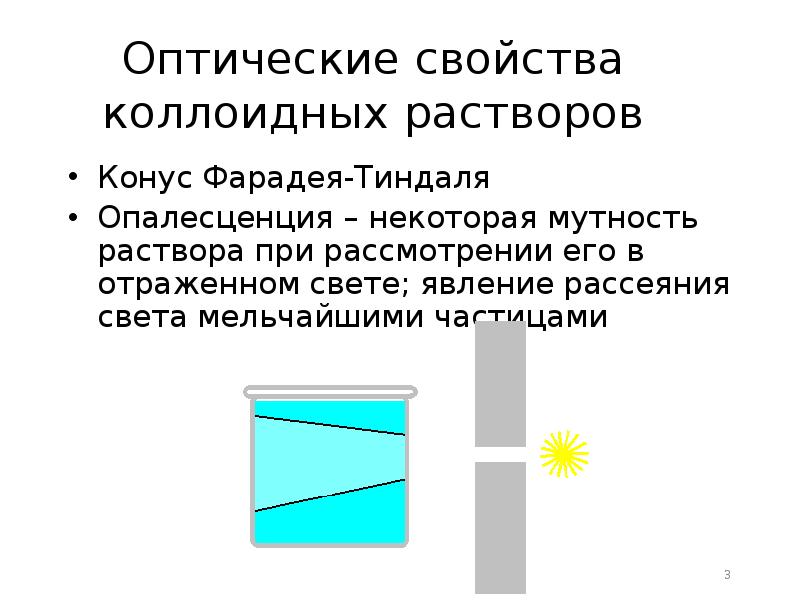
- 3. Оптические свойства коллоидных растворов Конус Фарадея-Тиндаля Опалесценция – некоторая мутность
- 4. Дихроизм Дихроизм Зависит: От природы вещества (поглощение света) От
- 5. Интенсивность рассеянного света I Закон Релея С · V2
- 6. Значение волны видимого света Значение волны видимого света Цвет сигнальных огней
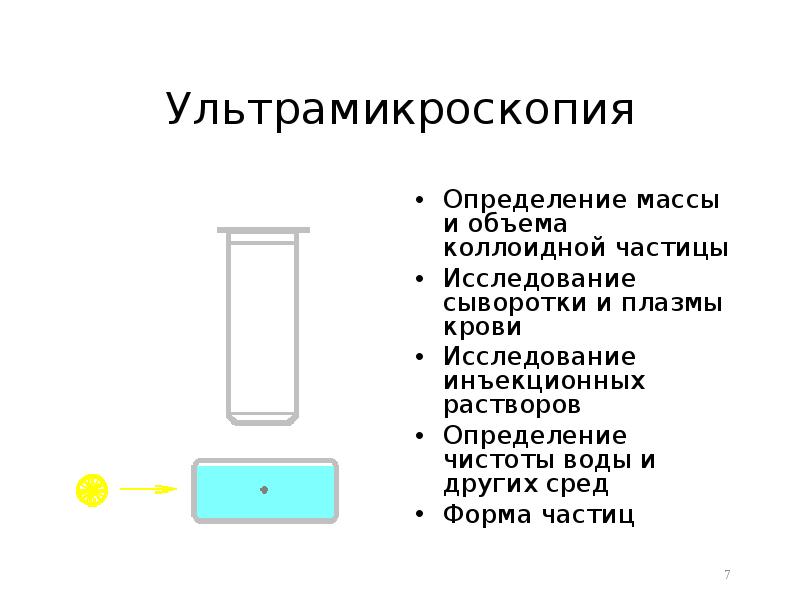
- 7. Ультрамикроскопия Определение массы и объема коллоидной частицы Исследование сыворотки и плазмы
- 8. Строение коллоидной частицы Внутренняя нейтральная часть, содержащая большую часть массы частицы
- 9. Получение коллоидного раствора реакцией осаждения KJ + AgNO3 = AgJ
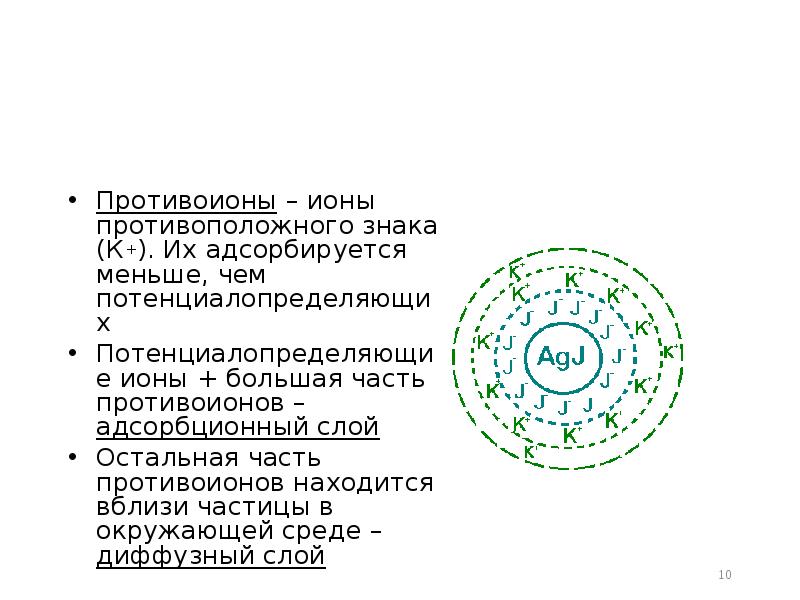
- 10. Противоионы – ионы противоположного знака (К+). Их адсорбируется меньше, чем потенциалопределяющих
- 11. Агрегат + адсорбционный слой – гранула (имеет заряд) Агрегат + адсорбционный
- 12. Строение коллоидной частицы Можно изображать мицеллярными формулами
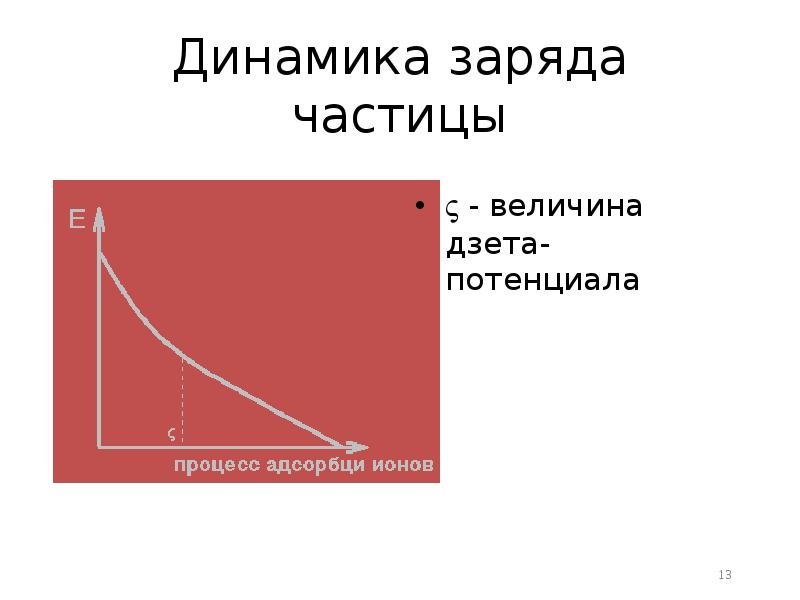
- 13. Динамика заряда частицы - величина дзета-потенциала
- 14. На величину -потенциала влияют Добавление к коллоидному раствору электролитов (сжимают диффузный
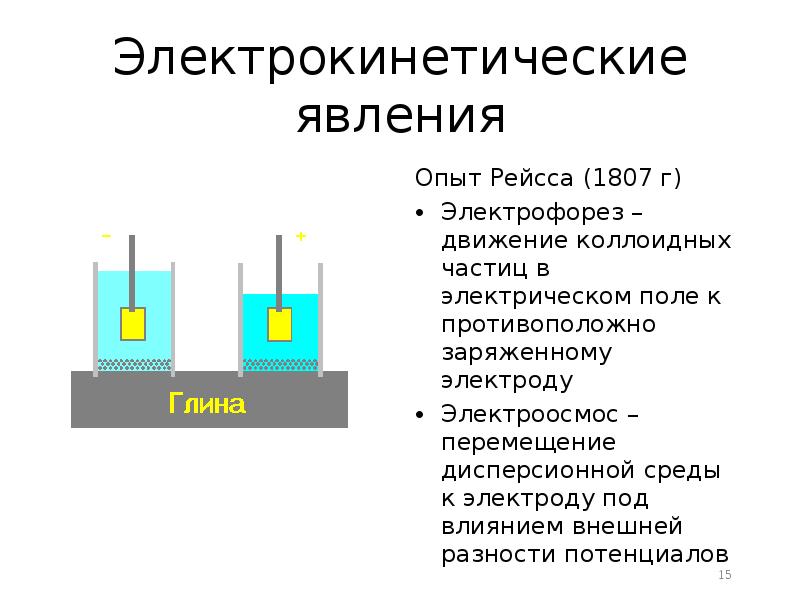
- 15. Электрокинетические явления Опыт Рейсса (1807 г) Электрофорез – движение коллоидных частиц
- 16. Применение электрофореза и электроосмоса В технике и различных производствах: Фарфоровое дело
- 17. Уравнение Гельмгольца-Смолуховского Расчет скорости движения коллоидных частиц в электрическом поле (U):
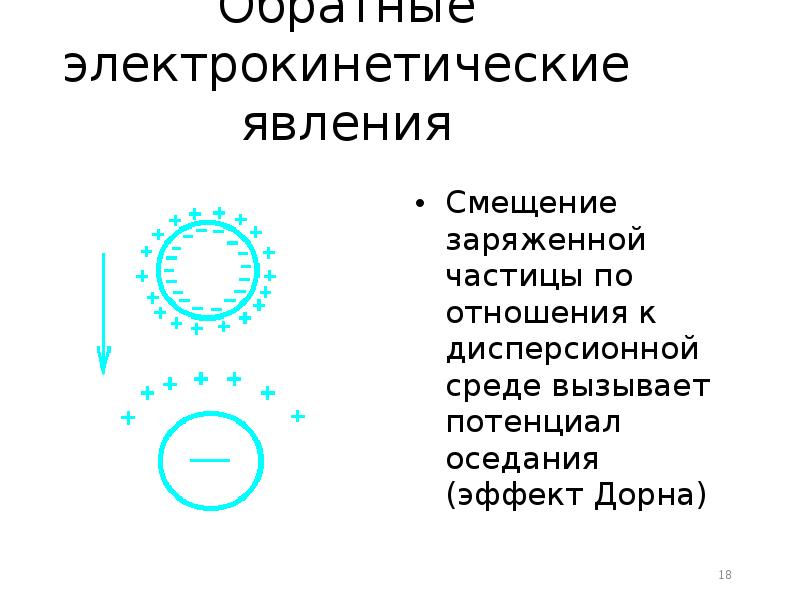
- 18. Обратные электрокинетические явления Смещение заряженной частицы по отношения к дисперсионной среде
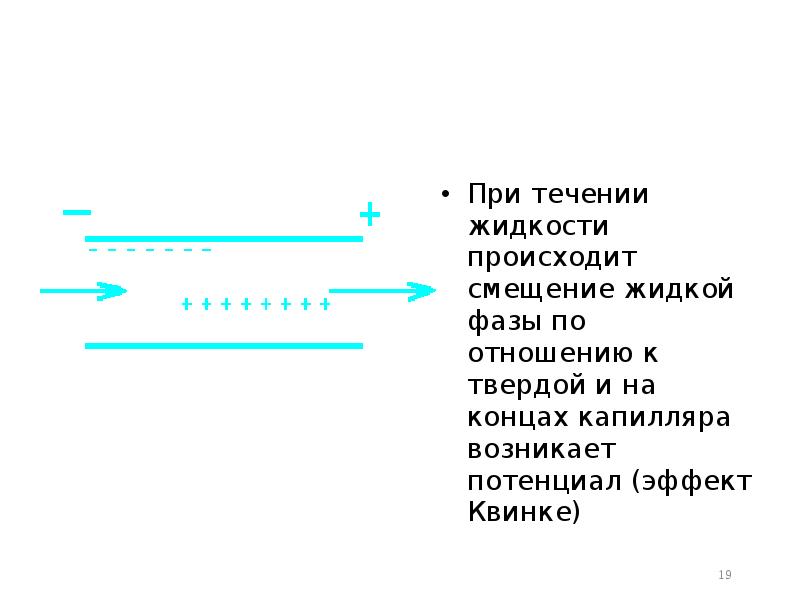
- 19. При течении жидкости происходит смещение жидкой фазы по отношению к твердой
- 20. Скачать презентацию












Слайды и текст этой презентации
Скачать презентацию на тему Физическая химия дисперсных систем можно ниже:
Похожие презентации





























