Кислая, нейтральная и щелочная среда. (Лекция 2) презентация
Содержание
- 5. Интервал значений квантовых чисел
- 6. «Проскок» или «провал» электронов - это переход электронов с подуровня с
- 7. Пример: Для элемента селена 34Se: 1) Символическая электронная формула:
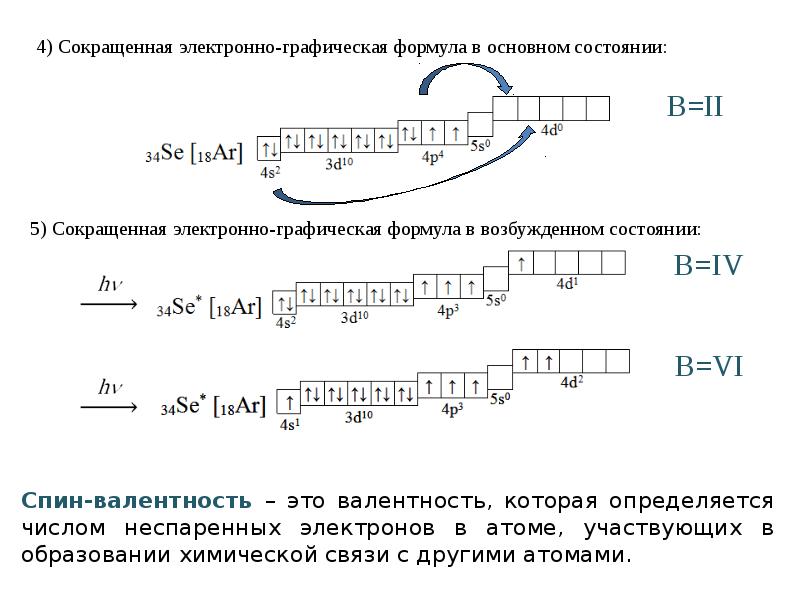
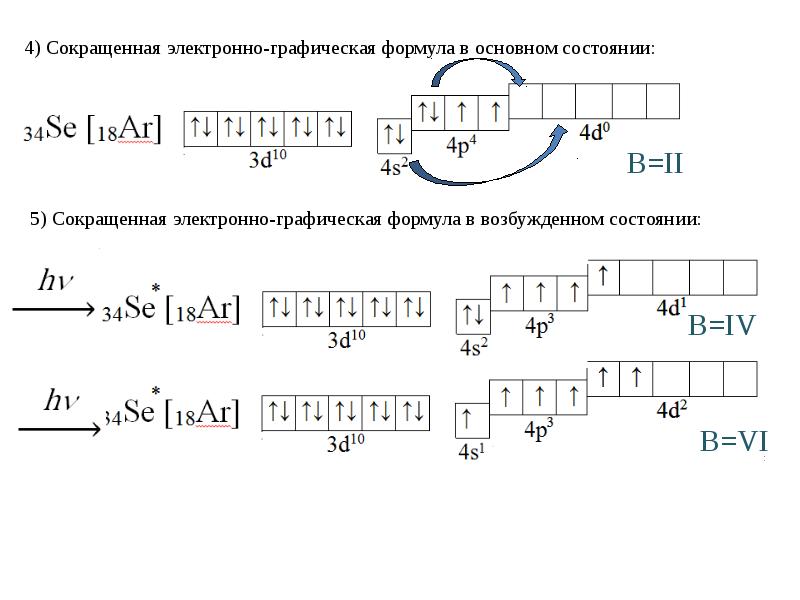
- 8. 3) Электронно-графическая формула:
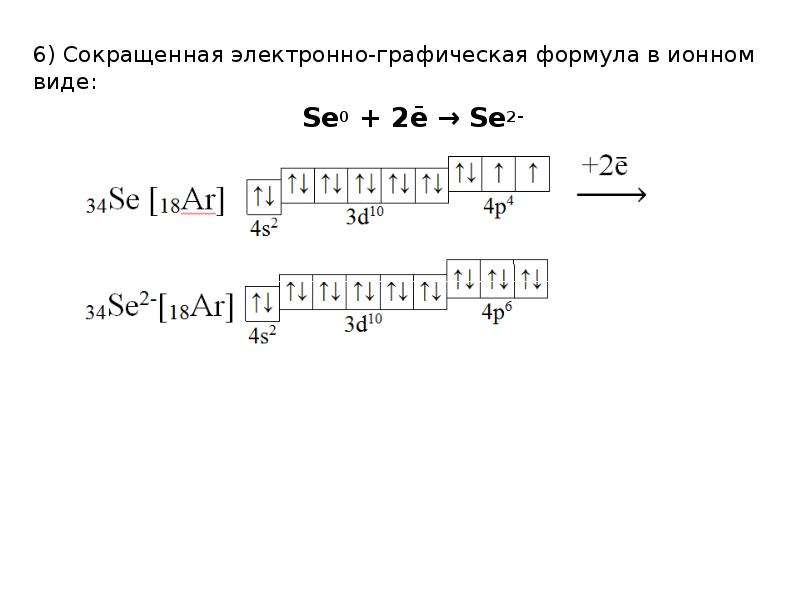
- 11. 6) Сокращенная электронно-графическая формула в ионном виде: 6) Сокращенная электронно-графическая формула
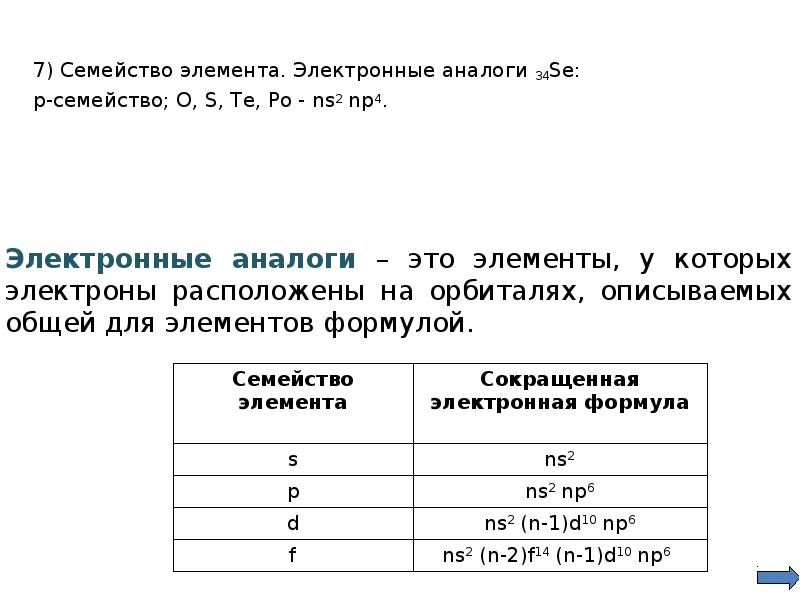
- 12. 7) Семейство элемента. Электронные аналоги 34Se: 7) Семейство элемента. Электронные аналоги
- 13. Скачать презентацию
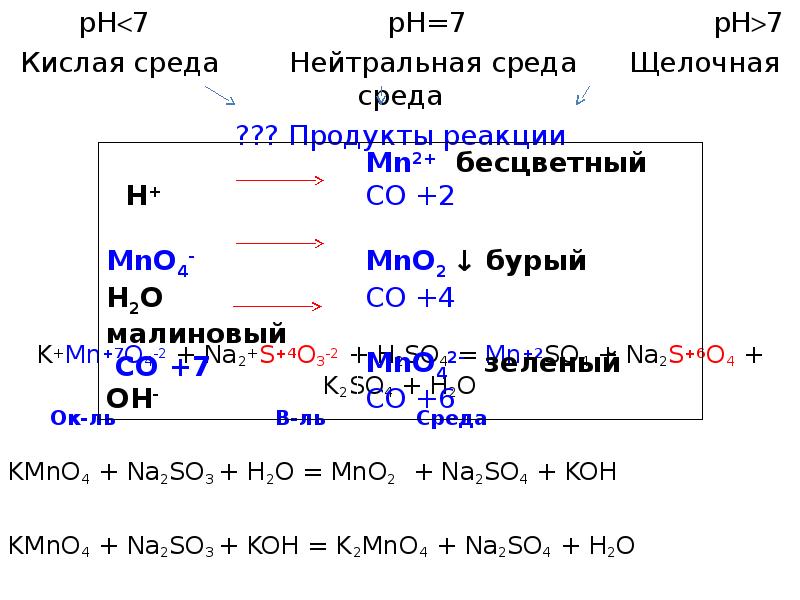
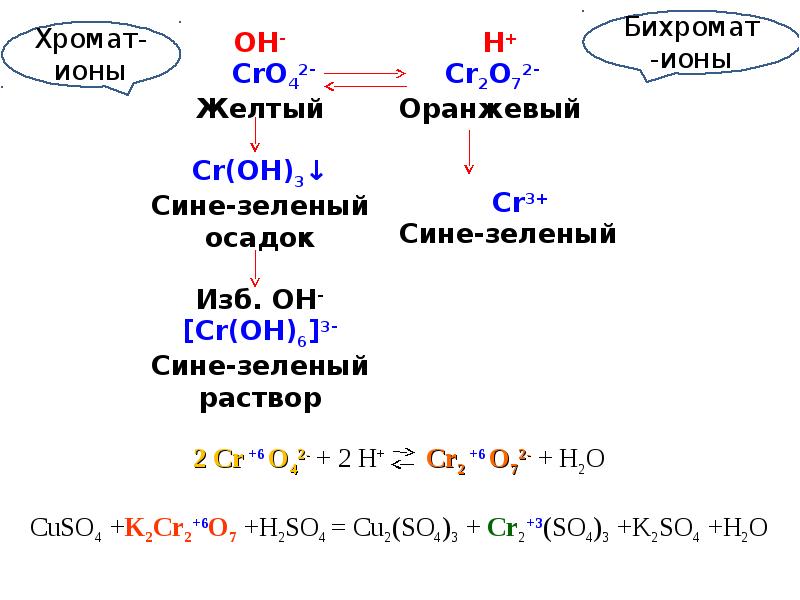
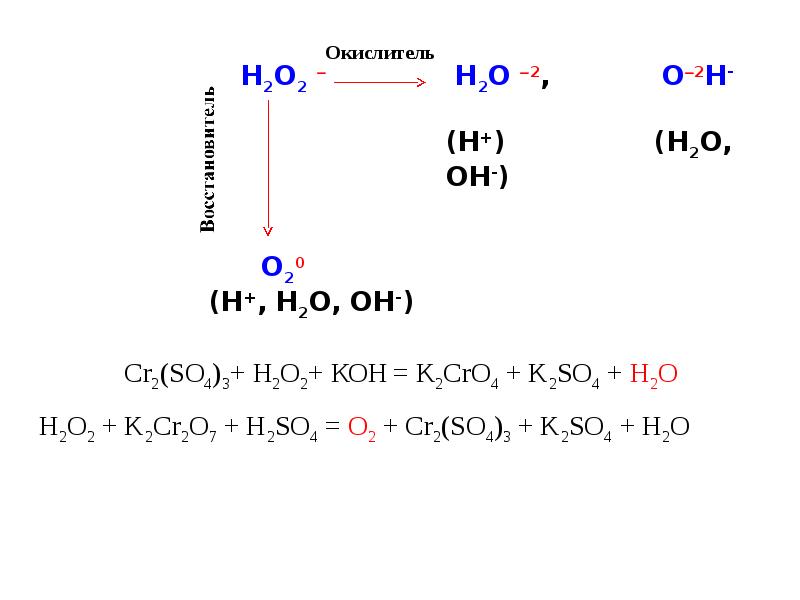

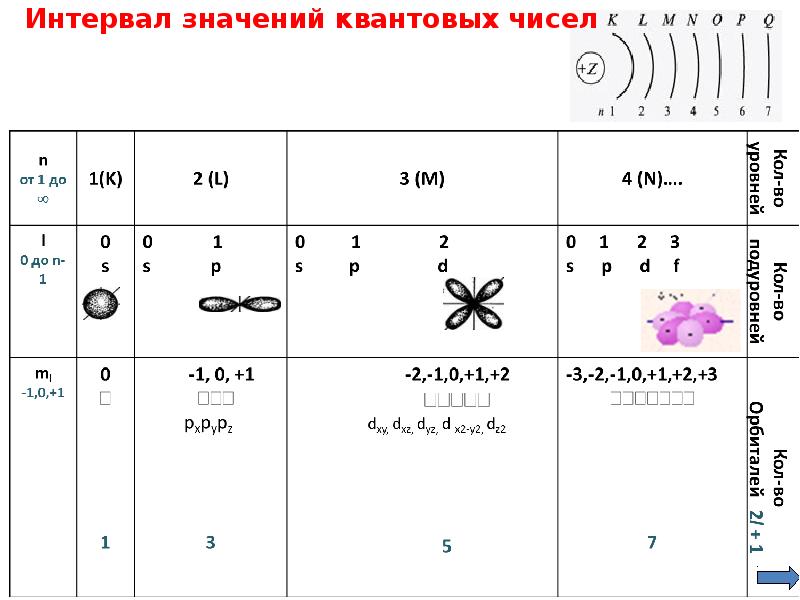



Слайды и текст этой презентации
Скачать презентацию на тему Кислая, нейтральная и щелочная среда. (Лекция 2) можно ниже:
Похожие презентации





























