Кислородные соединения азота. Азотная кислота презентация
Содержание
- 2. ПРОВЕРКА ЗНАНИЙ
- 3. 1.Определите, о каком веществе идёт речь I вариант
- 4. I вариант I вариант
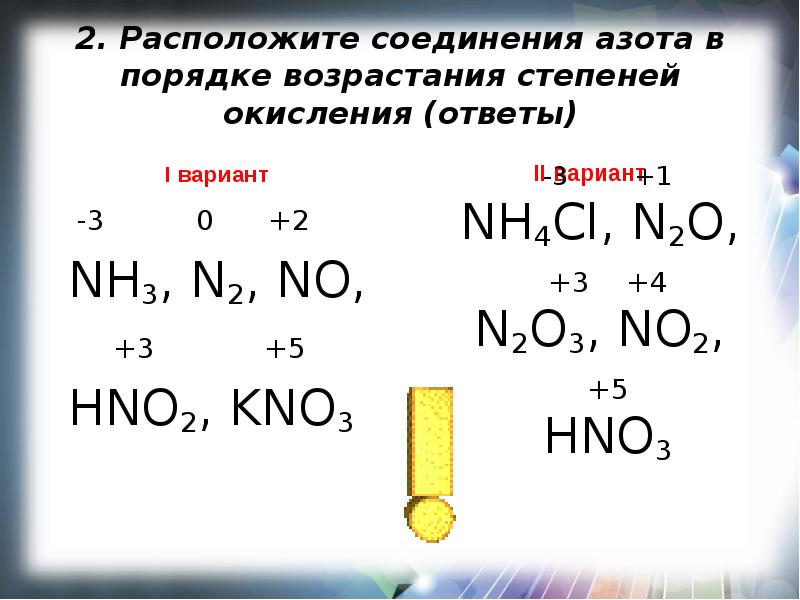
- 5. 2. Расположите соединения азота в порядке возрастания степеней окисления I вариант
- 6. 2. Расположите соединения азота в порядке возрастания степеней окисления (ответы) I
- 7. 3. Составьте уравнения реакций по схеме. Назовите вещество Х I вариант
- 8. 3. Составьте уравнения реакций по схеме. Назовите вещество Х (ответы) I
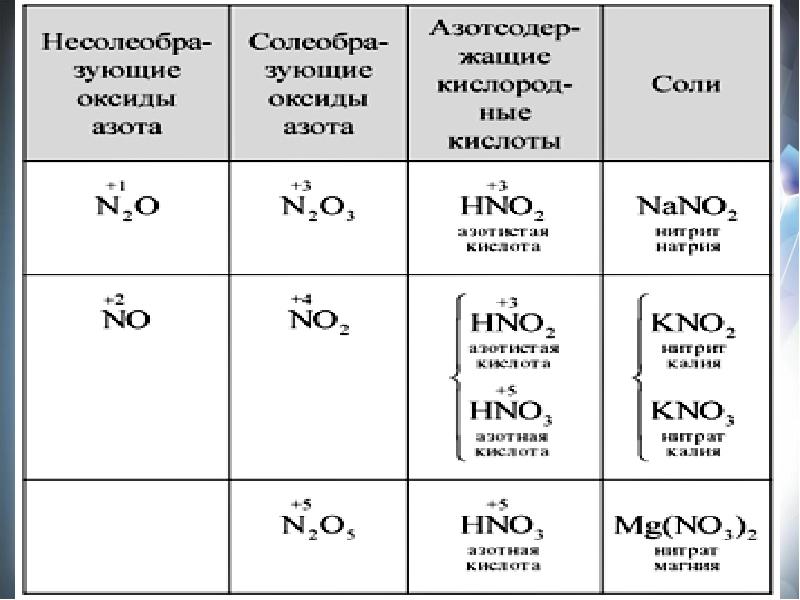
- 9. Кислородные соединения азота. Азотная кислота План изучения: I. Оксиды азота. Физические
- 11. I. Физические свойства азотной кислоты Агрегатное состояние – жидкость;
- 12. II. Характеристика HNO3 По основности: одноосновная 2. По содержанию
- 13. III. Химические свойства HNO3 Свойства HNO3 как электролита Диссоциация: HNO3 =
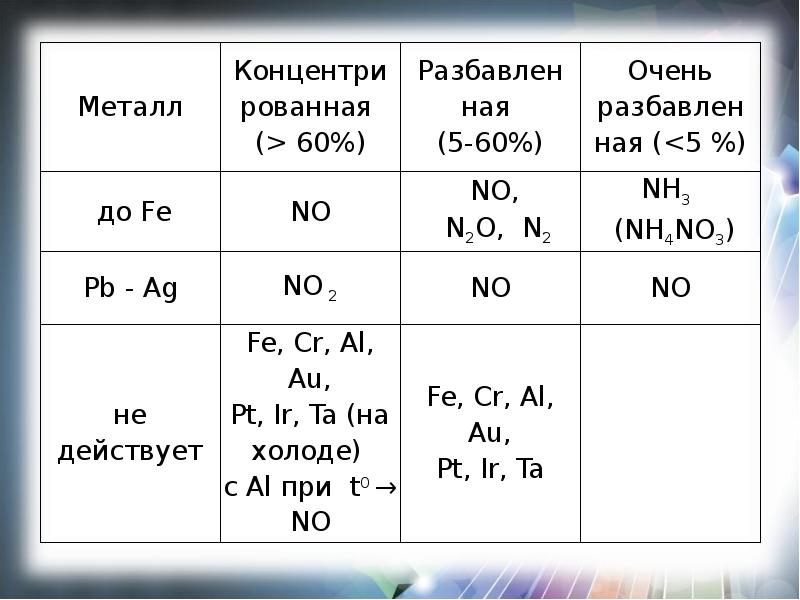
- 14. III. Химические свойства HNO3 2. Окислительные свойства Взаимодействует с металлами:
- 15. III. Химические свойства HNO3 2. Окислительные свойства Взаимодействует с неметаллами:
- 17. IV. Применение азотной кислоты
- 18. Вопросы на закрепление I. Назовите вещества, с которыми может реагировать азотная
- 19. Домашнее задание § 27, упр. 5,6
- 20. Скачать презентацию















Слайды и текст этой презентации
Скачать презентацию на тему Кислородные соединения азота. Азотная кислота можно ниже:
Похожие презентации





























