Молекулярная физика презентация
Содержание
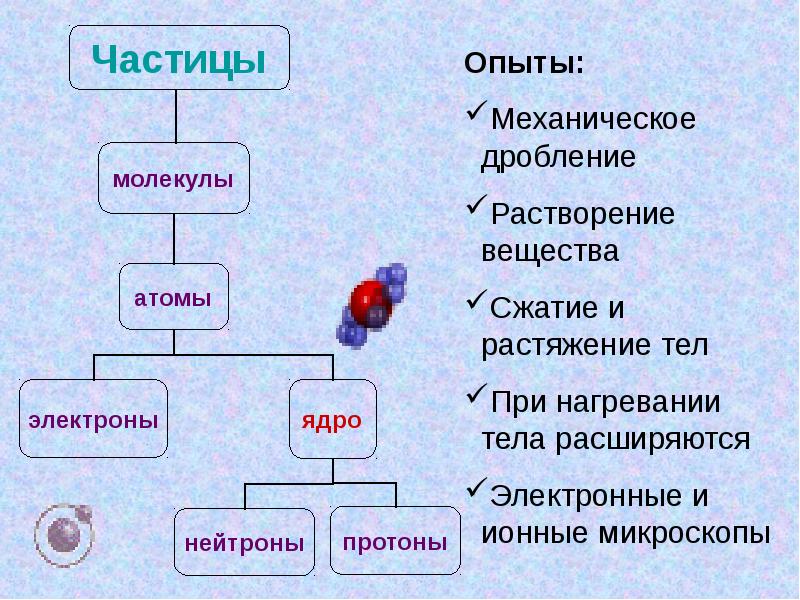
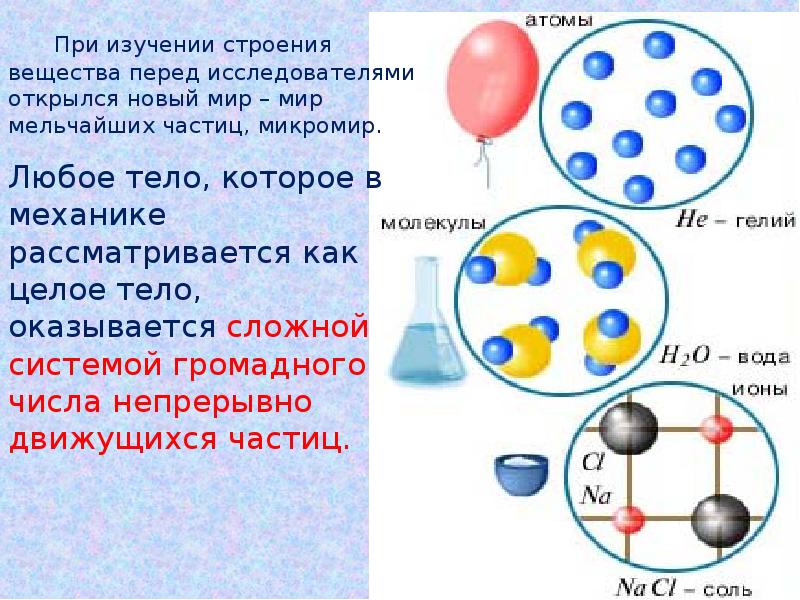
- 2. 1. Молекулярная физика Молекулярная физика рассматривает строение и свойства
- 3. Молекулярно-кинетической теорией ( МКТ) называют учение о строении и свойствах вещества
- 4. В основе молекулярно-кинетической теории лежат три основных положения: Все вещества
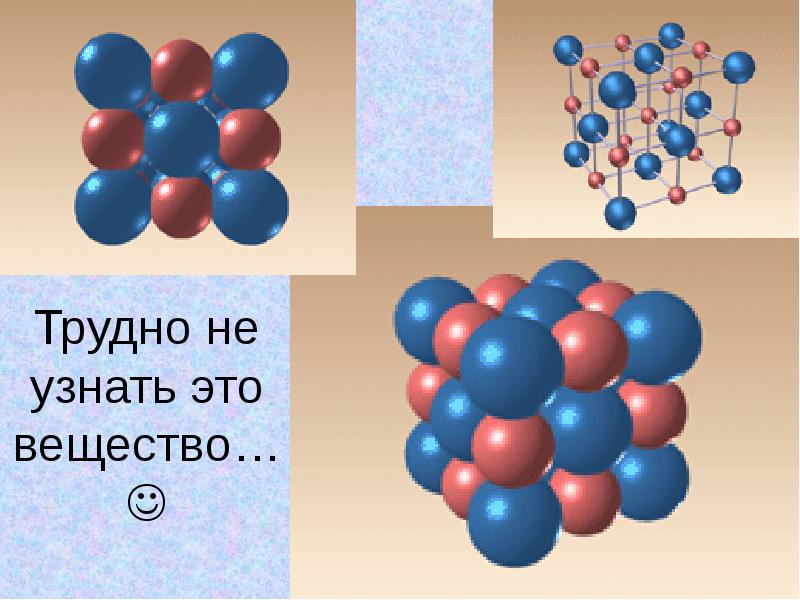
- 6. Трудно не узнать это вещество…
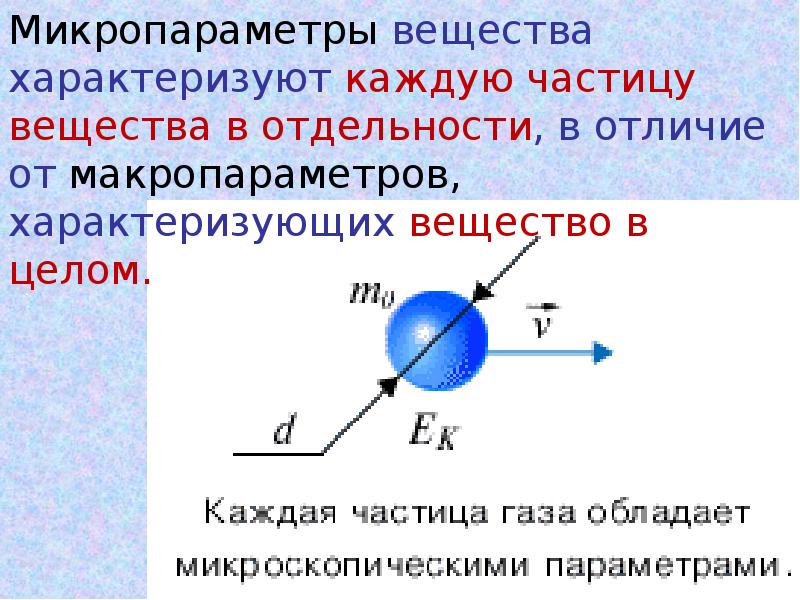
- 7. 2. Атомы и молекулы находятся в непрерывном хаотическом движении. Скорость молекул
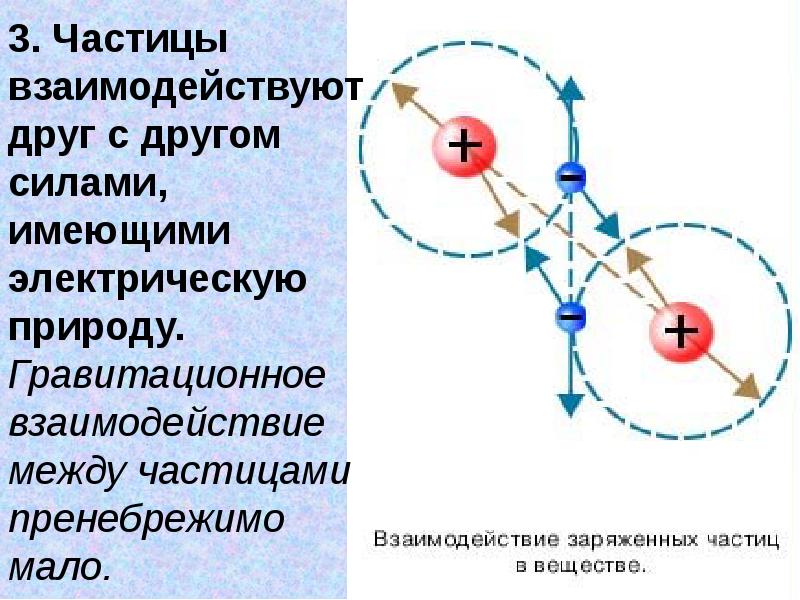
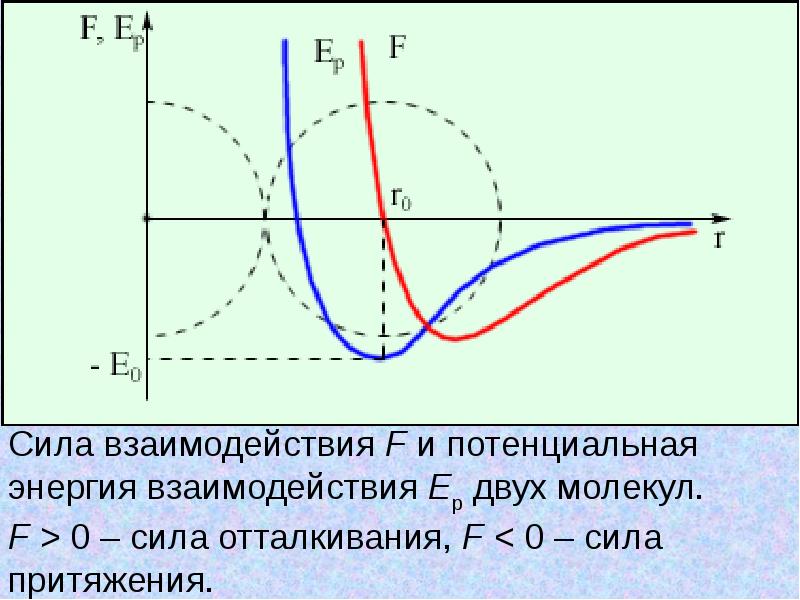
- 9. 3. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное
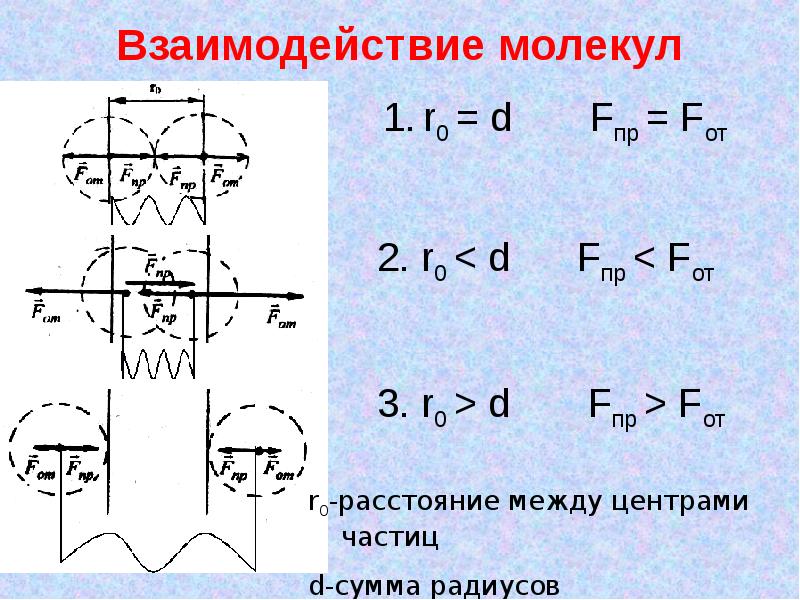
- 10. Взаимодействие молекул
- 12. Явления, подтверждающие идеи МКТ: Высокая сжимаемость газов свидетельствует о наличии больших
- 13. Явления, подтверждающие идеи МКТ: Давление газа на стенки сосуда (или на
- 31. Опыт показывает, что в равных объемах газа при одинаковых давлениях и
- 42. Скачать презентацию

































Слайды и текст этой презентации
Похожие презентации





























