Молекулярно-кинетические представления о строении тел (лекция № 10) презентация
Содержание
- 2. Литература: Глаголев К.В., Морозов А.Н. Физическая термодинамика: Учеб. пособие. – М.:
- 3. Лекция № 10 МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О СТРОЕНИИ ТЕЛ
- 4. Статистический и термодинамический методы описания макроскопических тел
- 5. Методы описания макросистем основаны на применении законов классической механики (затруднительно из-за
- 6. Статистический метод описания основывается на применении законов теории вероятностей, а в
- 7. Использует статистический метод, интересуясь движением не отдельных молекул, а лишь такими
- 8. Термодинамический метод – наиболее общий метод описания макросистем, независимо от конкретной
- 9. Термодинамика – постулативная наука. Ее не интересуют конкретные представления о строении
- 10. Термодинамика – раздел физики, исследующий превращение некоторых видов энергии. Термодинамика
- 11. Изолированная система – нет перетекания энергии (вещества) через стенки системы.
- 12. Состояние макросистемы характеризуют термодинамическими параметрами (наиболее распространенные термодинамические параметры – давление
- 13. Равновесное или состояние термодинамического равновесия термодинамической системы – если при сохранении
- 14. НУЛЕВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Нулевое начало термодинамики. Классическая термодинамика утверждает, что
- 15. Свойства систем, находящихся в состоянии термодинамического равновесия: Свойства систем,
- 16. Заключение. Заключение.
- 17. Термодинамические процессы При изменении параметров состояния макросистемы в ней происходит
- 19. Обратимый процесс – процесс, который может происходить через те же состояния
- 20. Квазистатические (квазиравновесные) процессы представляют собой непрерывную последовательность равновесных состояний системы.
- 21. Внутренняя энергия и температура термодинамической системы Система в данном состоянии
- 22. Температура – величина, характеризующая состояние термодинамического равновесия макросистемы. Температура –
- 23. Свойства температуры термодинамических систем, находящихся в состоянии равновесия: Свойства температуры термодинамических
- 24. Любой метод измерения температуры требует установление температурной шкалы. Для этого используют
- 25. При таком значении Tтр интервал между точками плавления льда и кипения
- 26. В дальнейшем мы выясним физический смысл температуры T. В дальнейшем
- 27. Теплота и работа Передача энергии от одного тела к другому
- 28. Передача энергии от одного тела к другому посредством теплового обмена между
- 29. Идеальный газ Простейшей моделью макросистемы, рассматриваемой статистической физикой, является идеальный
- 30. Т.е. если в единице объема имеется n молекул, то в каждом
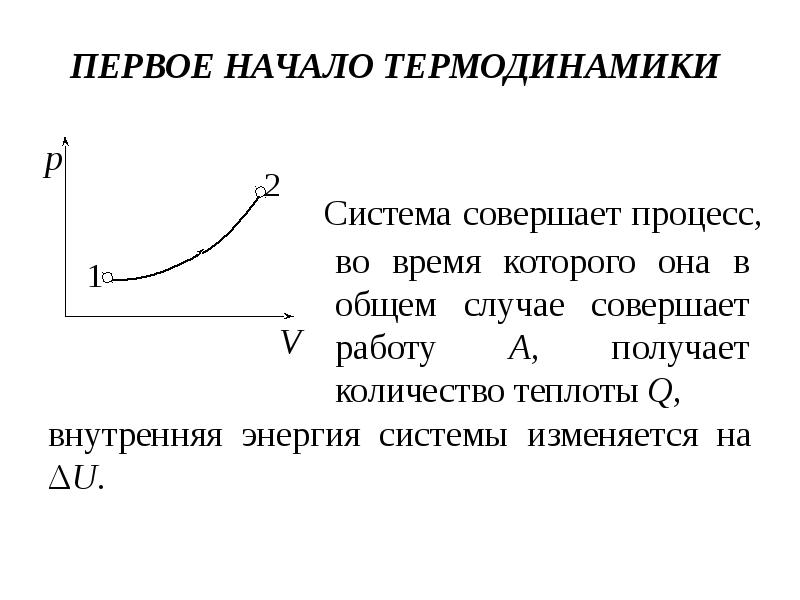
- 31. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Система совершает процесс,
- 32. Первое начало термодинамики: количество теплоты Q, сообщенное макросистеме, идет на приращение
- 33. Если Q < 0, то тепло отводится от системы; A <
- 34. Первое начало термодинамики для элементарного процесса (в дифференциальной форме): Первое
- 35. Скачать презентацию
































Слайды и текст этой презентации
Скачать презентацию на тему Молекулярно-кинетические представления о строении тел (лекция № 10) можно ниже:
Похожие презентации





























