Окислительно - восстановительные реакции презентация
Содержание










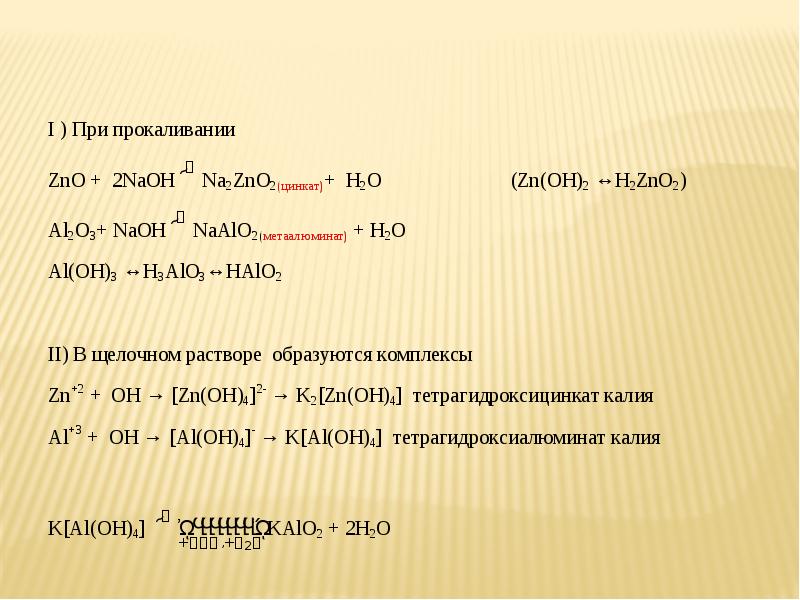


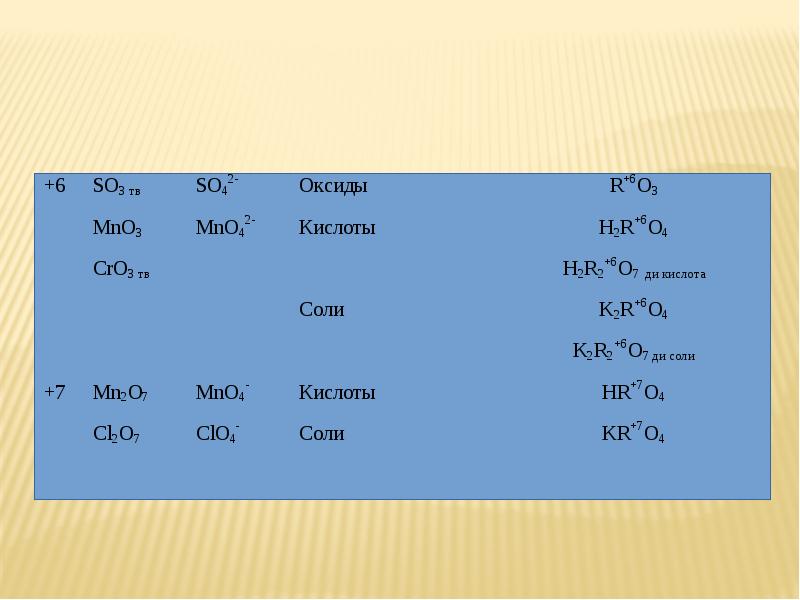
Слайды и текст этой презентации
Скачать презентацию на тему Окислительно - восстановительные реакции можно ниже:
Похожие презентации





























