Основы общей химии презентация
Содержание
- 2. Если на систему, находящуюся в состоянии истинного равновесия, оказывается внешнее воздействие,
- 3. Л.5 Кинетика химических реакций Законы химической термодинамики позволяют определить направление и
- 4. СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ Скорость химической реакции есть число элементарных
- 5. Наиболее часто в химии рассматривается зависимость концентрации реагентов от времени.
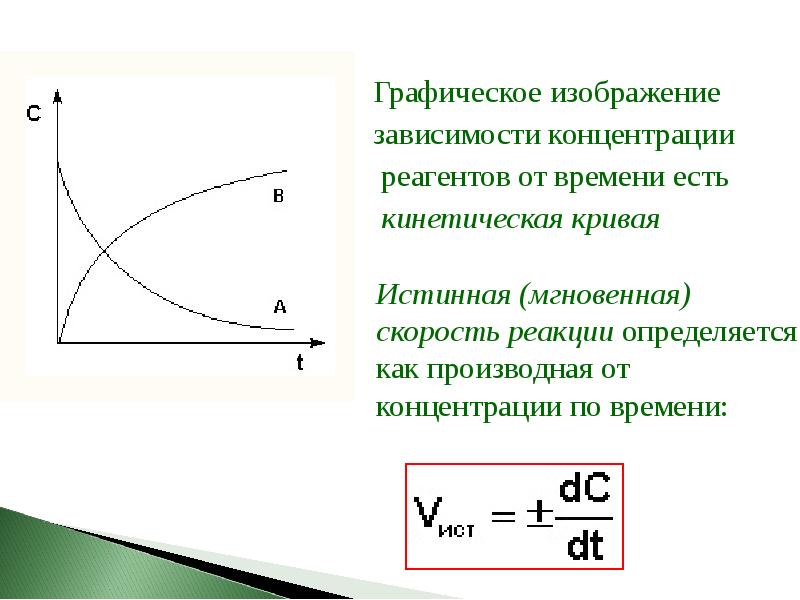
- 6. Графическое изображение
- 7. Истинную скорость реакции можно определить графически, проведя касательную к кинетической кривой.
- 8. Если стехиометрические коэффициенты в уравнении химической реакции неодинаковы, величина скорости реакции
- 9. Скорость химической реакции зависит от множества факторов: Скорость химической реакции
- 10. Кинетическое уравнение химической реакции. Порядок реакции. Одной из задач, стоящих перед
- 11. Для реакции Для реакции аА + bВ + dD + ...
- 12. Зависимость скорости реакции от концентраций реагирующих веществ определяется экспериментально и называется
- 13. Сумма показателей степени в кинетическом уравнении химической реакции (x + y
- 14. В химической кинетике принято классифицировать реакции по величине общего порядка реакции.
- 15. Реакции нулевого порядка Для реакций нулевого порядка кинетическое уравнение имеет следующий
- 16. Реакции первого порядка Рассмотрим зависимость от времени концентрации исходного вещества А
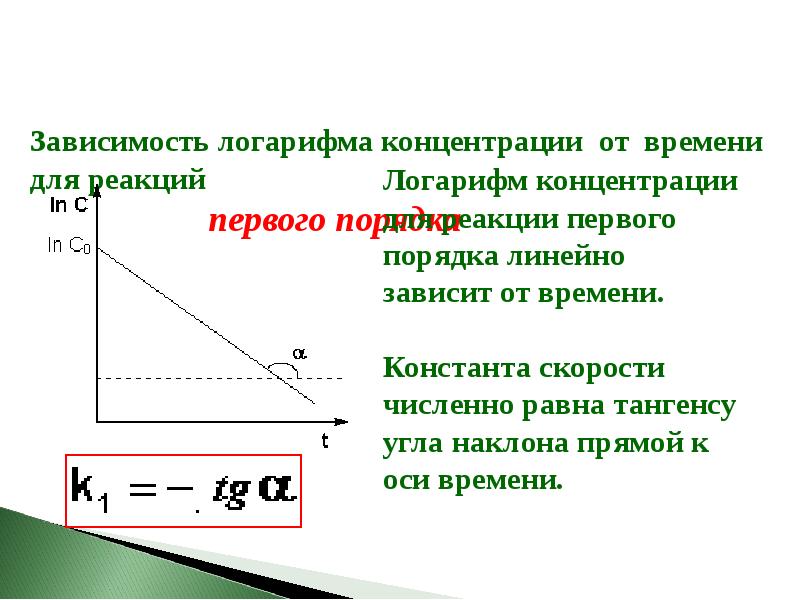
- 17. Зависимость логарифма концентрации от времени для реакций
- 18. Из уравнения Из уравнения легко получить выражение для
- 19. Реакции второго порядка Для реакций второго порядка кинетическое уравнение имеет
- 20. После разделения переменных и интегрирования получаем: После разделения переменных и интегрирования
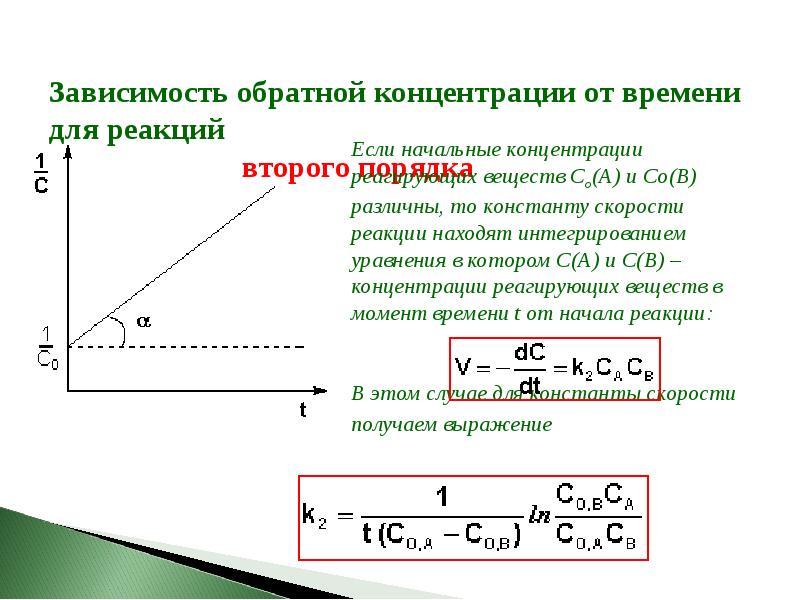
- 21. Зависимость обратной концентрации от времени для реакций второго порядка
- 22. Порядок химической реакции есть формально-кинетическое понятие, физический смысл которого для элементарных
- 23. Л.6 Рассмотрим пример: Рассмотрим в качестве примера элементарную реакцию гидролиза этилового
- 24. При проведении этой же реакции в условиях большого избытка одного из
- 25. Методы определения порядка реакции Проведение реакции в условиях, когда концентрация
- 26. Графический метод заключается в построении графика зависимости концентрации реагента от
- 27. Если построить графики этих зависимостей на основании опытных данных, то лишь
- 28. Метод подбора кинетического уравнения заключается в подстановке экспериментальных данных изучения
- 30. Метод определения времени полупревращения заключается в определении t1/2 для нескольких
- 32. Молекулярность элементарных реакций Элементарными (простыми) называют реакции, идущие в одну
- 33. Мономолекулярные – реакции, Мономолекулярные – реакции, в которых происходит
- 34. Бимолекулярные – реакции, Бимолекулярные – реакции, элементарный акт которых
- 35. Тримолекулярные – реакции, элементарный акт которых осуществляется при столкновении трех частиц:
- 36. Для элементарных реакций, проводимых при близких концентрациях исходных веществ, величины молекулярности
- 37. Сложные реакции Сложными называют химические реакции, протекающие более чем в одну
- 38. Сделать вывод о том, является реакция элементарной или сложной, можно на
- 39. Классификация сложных реакций Последовательные реакции. Последовательными называются сложные реакции, протекающие таким
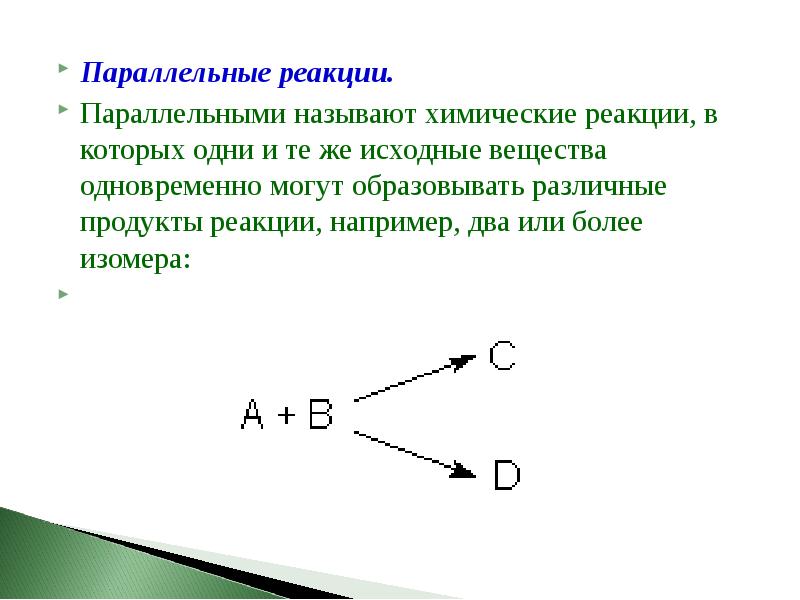
- 40. Параллельные реакции. Параллельные реакции. Параллельными называют химические реакции, в которых одни
- 41. Сопряжённые реакции. Сопряжённые реакции. Сопряжёнными принято называть сложные реакции, протекающие следующим
- 42. Например, бензол в водном растворе не окисляется пероксидом водорода, но при
- 43. Цепные реакции. Цепными называют реакции, состоящие из ряда взаимосвязанных стадий, когда
- 44. Обрыв цепи возможен также при взаимодействии активных частиц с материалом стенки
- 45. Разветвленными называют цепные реакции, в которых на каждую прореагировавшую активную частицу
- 46. Влияние температуры на константу скорости реакции Константа скорости реакции есть функция
- 47. Величина, показывающая, во сколько раз увеличивается константа скорости при повышении температуры
- 48. Уравнение Аррениуса Взаимодействие частиц осуществляется при их столкновениях; однако число
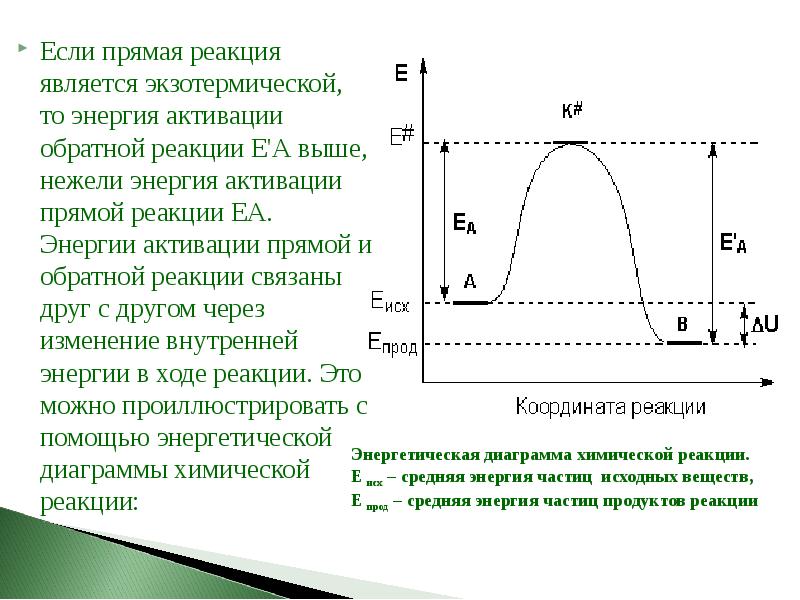
- 49. Рассмотрим путь некоторой элементарной реакции Рассмотрим путь некоторой элементарной реакции
- 50. Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано,
- 51. Если прямая реакция является экзотермической, то энергия активации обратной реакции Е'А
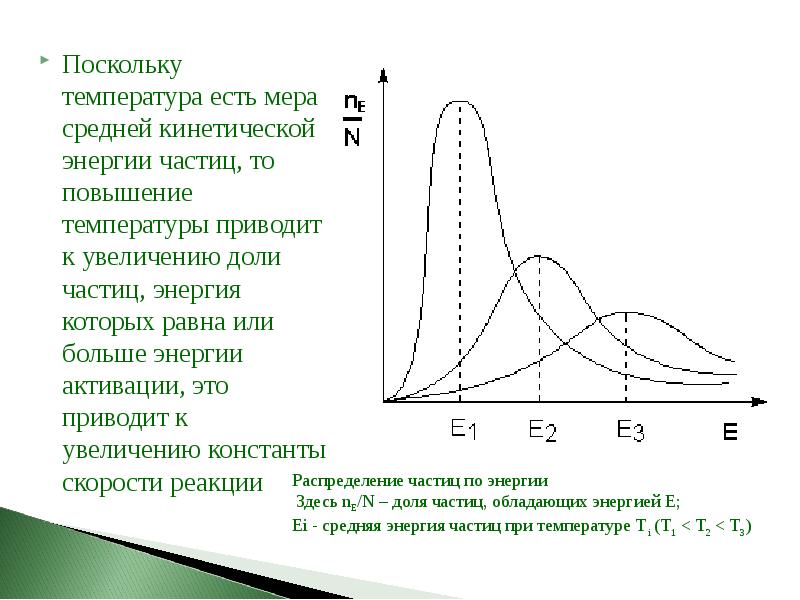
- 52. Поскольку температура есть мера средней кинетической энергии частиц, то повышение температуры
- 53. Термодинамический вывод выражения, описывающего зависимость константы скорости реакции от температуры и
- 54. Здесь С – некоторая константа. Постулировав, что С = 0, получаем
- 55. Зависимость логарифма константы скорости химической реакции от обратной температуры Зависимость
- 56. Зная энергию активации реакции и константу скорости при какой-либо температуре T1,
- 57. Кинетика двусторонних (обратимых) реакций Химические реакции часто являются двусторонними (обратимыми), т.е.
- 58. Общая скорость двусторонней реакции в любой момент времени равна разности скоростей
- 59. Кинетика гетерогенных химических реакций Когда реакция совершается между веществами, находящимися в
- 60. Стадии 1 и 5 называются диффузионными, Стадии 1 и 5
- 61. ФОТОХИМИЧЕСКИЕ РЕАКЦИИ Передача энергии для активации вступающих во взаимодействие молекул может
- 62. Излучение, отражённое веществом, а также прошедшее сквозь него, не вызывают никаких
- 63. Взаимодействие света с веществом может идти по трём возможным направлениям: Взаимодействие
- 64. Между количеством лучистой энергии, поглощенной молекулами вещества, и количеством фотохимически прореагировавших
- 65. Поскольку фотохимическая реакция, как правило, включает в себя и т.н. вторичные
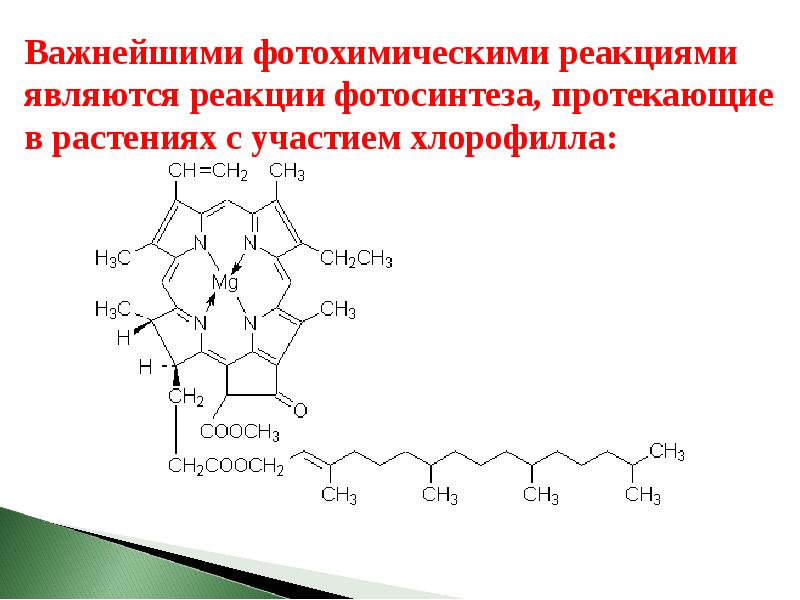
- 66. Важнейшими фотохимическими реакциями являются реакции фотосинтеза, протекающие в растениях с участием
- 67. Процесс фотосинтеза составляют две стадии: световая, связанная с поглощением фотонов, и
- 68. Протекание данного окислительно-восстановительного процесса (связанного с переносом электронов) возможно благодаря наличию
- 69. КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Скорость химической реакции при данной температуре определяется скоростью
- 70. Различают положительный и отрицательный катализ (соответственно увеличение и уменьшение скорости реакции),
- 71. Специфичность катализатора заключается в его способности ускорять только одну реакцию или
- 72. Селективность катализатора – способность ускорять одну из возможных при данных условиях
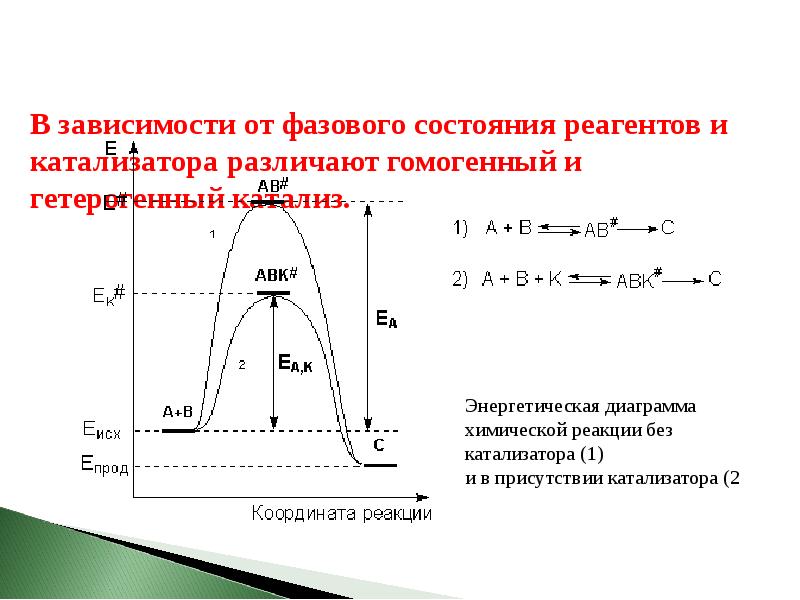
- 73. Причиной увеличения скорости реакции при положительном катализе является уменьшение энергии активации
- 74. Действительно, если предположить, что предэкспоненциальные множители в уравнении Аррениуса для каталитической
- 75. Наличие катализатора не влияет на величину изменения термодинамического потенциала в результате
- 76. В зависимости от фазового состояния реагентов и катализатора различают гомогенный и
- 77. Гомогенный катализ. Гомогенный катализ – каталитические реакции, в которых реагенты и
- 78. Примером такого процесса может служить реакция разложения ацетальдегида, энергия активации которой
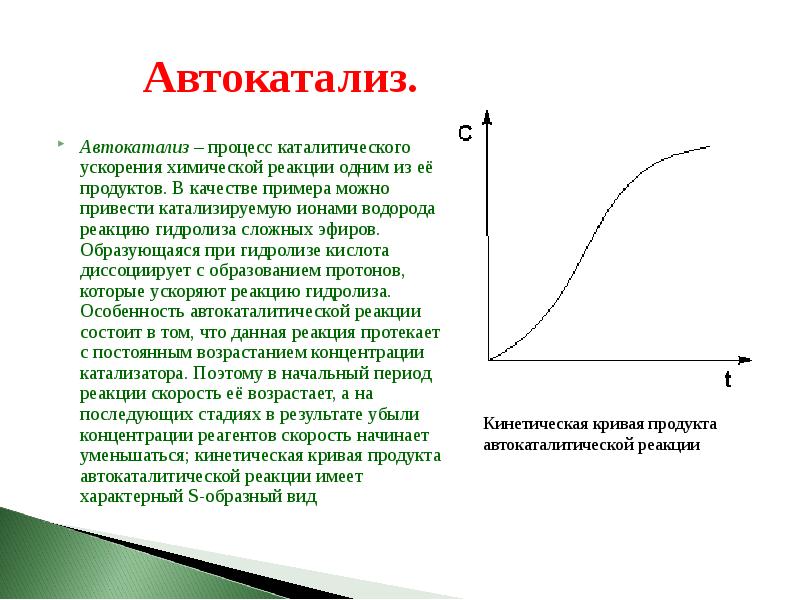
- 79. Автокатализ. Автокатализ – процесс каталитического ускорения химической реакции одним
- 80. Гетерогенный катализ. Гетерогенный катализ – каталитические реакции, идущие на поверхности раздела
- 81. Специфической особенностью гетерокаталитических процессов является способность катализатора к промотированию и отравлению.
- 82. Для объяснения этих особенностей гетерогенно-каталитических процессов Г. Тэйлором было высказано следующее предположение:
- 83. 1. Активный центр катализатора представляет собой совокупность определенного числа адсорбционных центров,
- 84. Ферментативный катализ. Ферментативный катализ – каталитические реакции, протекающие с участием ферментов
- 85. Скачать презентацию











































































Слайды и текст этой презентации
Похожие презентации





























