Поверхностные явления. Уравнение Гиббса презентация
Содержание
- 2. План лекции Общие понятия Поверхностное натяжение Процессы, происходящие на подвижных поверхностях
- 3. Поверхностный слой вещества Промежуточная фаза, содержащая один или несколько молекулярных слоев
- 4. Поверхностные явления незначительны, если соотношения между массой тела и поверхностью в
- 5. Поверхностная энергия Гиббса GS GS = S –
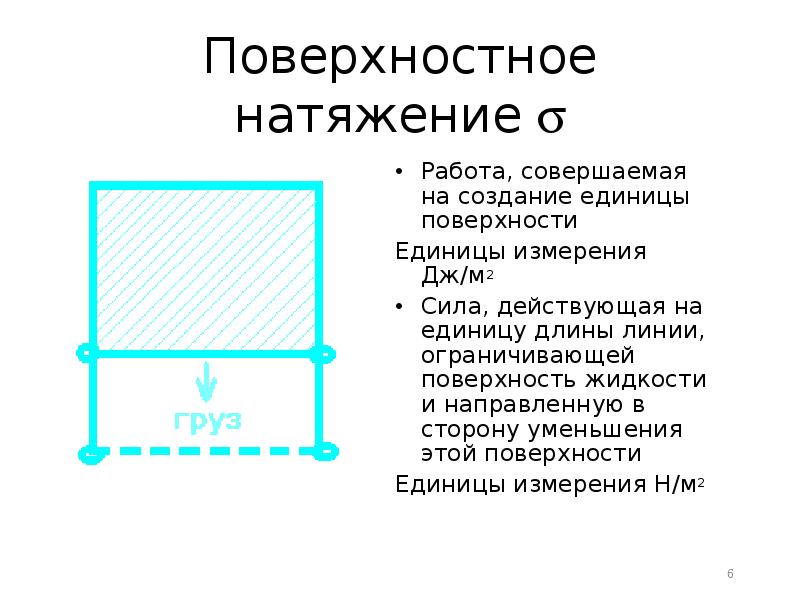
- 6. Поверхностное натяжение Работа, совершаемая на создание единицы поверхности Единицы измерения
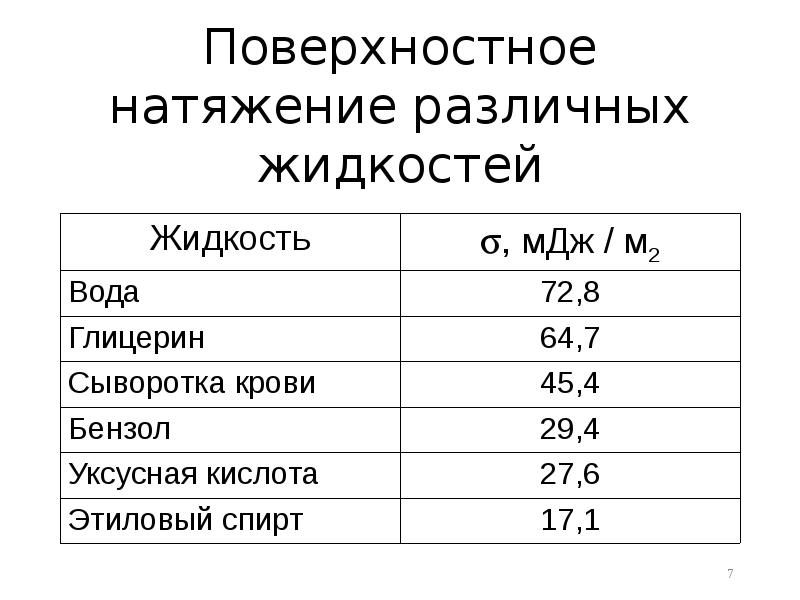
- 7. Поверхностное натяжение различных жидкостей
- 8. Процессы на подвижных поверхностях Сорбция – поглощение каким-либо веществом других веществ
- 9. Величина адсорбции Г Выражается количеством молей вещества (сорбтива), приходящегося на единицу
- 10. Поверхностные явления Происходят в следующих системах: Газ / твердое тело Газ
- 11. Поверхностные явления в растворах Накопление растворенного вещества в поверхностном слое Процесс
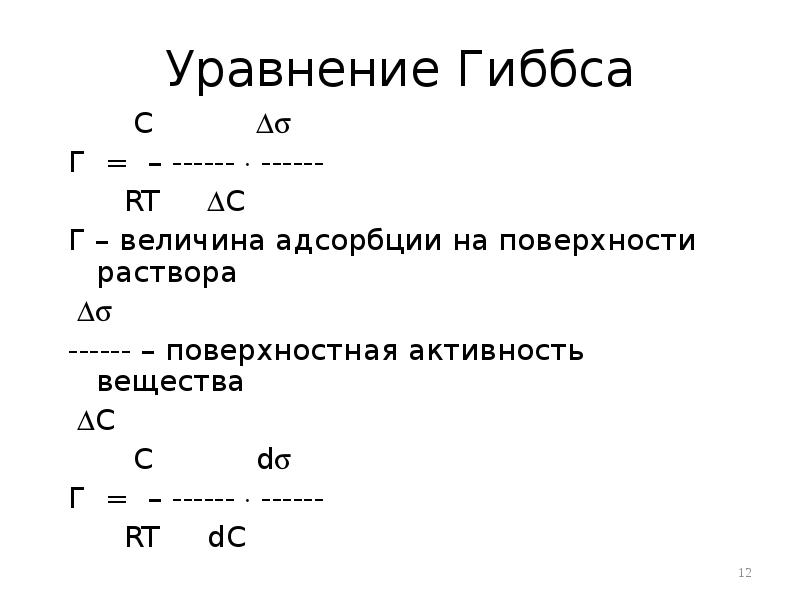
- 12. Уравнение Гиббса С Г = – ------
- 13. Анализ уравнение Гиббса ------ = 0; Г = 0
- 14. Свойства ПАВ Ограниченно растворимы Обладают меньшим поверхностным натяжением, чем жидкости Резко
- 15. Классификация ПАВ Молекулярные или неионогенные – спирты, желчь, белковые вещества Ионогенные
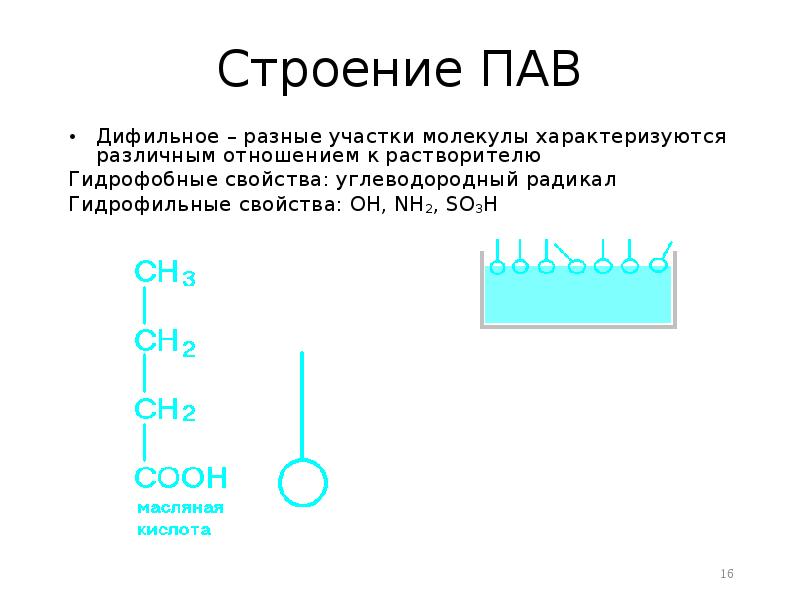
- 16. Строение ПАВ Дифильное – разные участки молекулы характеризуются различным отношением к
- 17. Правило Траубе-Дюкло Удлинение цепи на радикал – CH2 – увеличивает способность
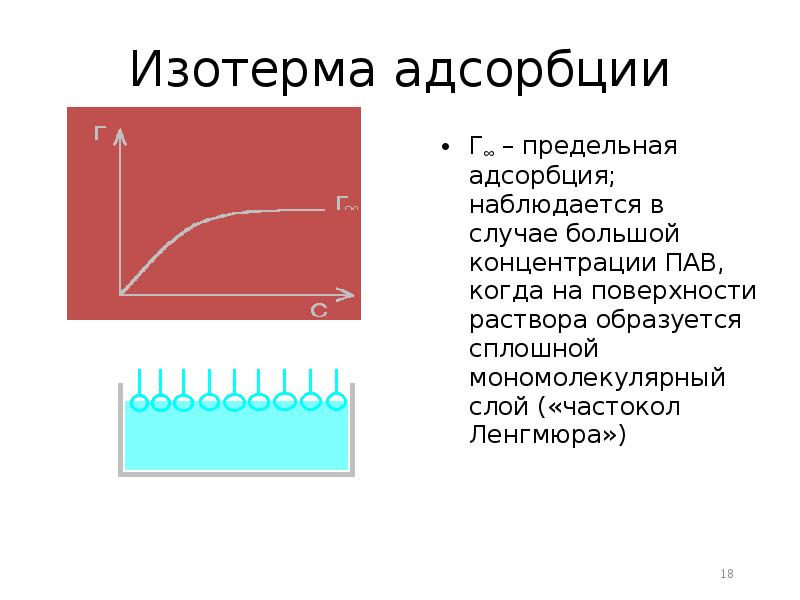
- 18. Изотерма адсорбции Г – предельная адсорбция; наблюдается в случае большой концентрации
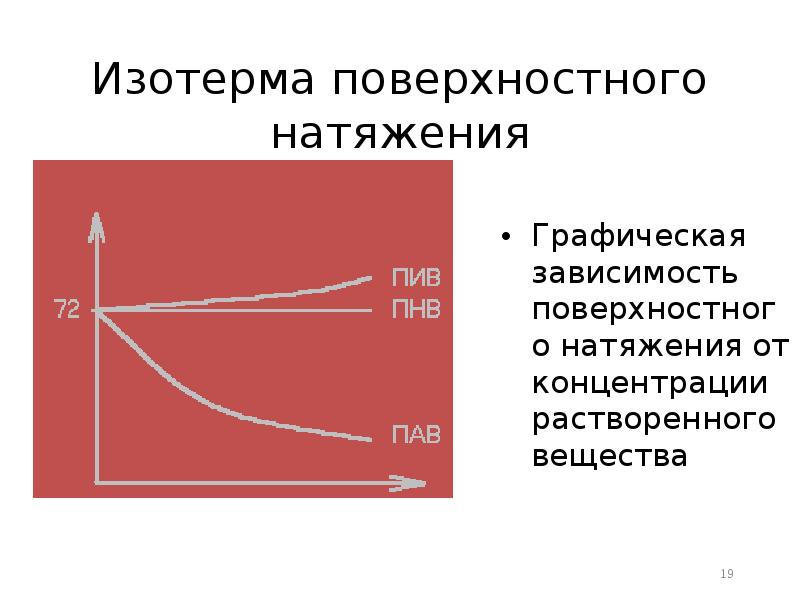
- 19. Изотерма поверхностного натяжения Графическая зависимость поверхностного натяжения от концентрации растворенного вещества
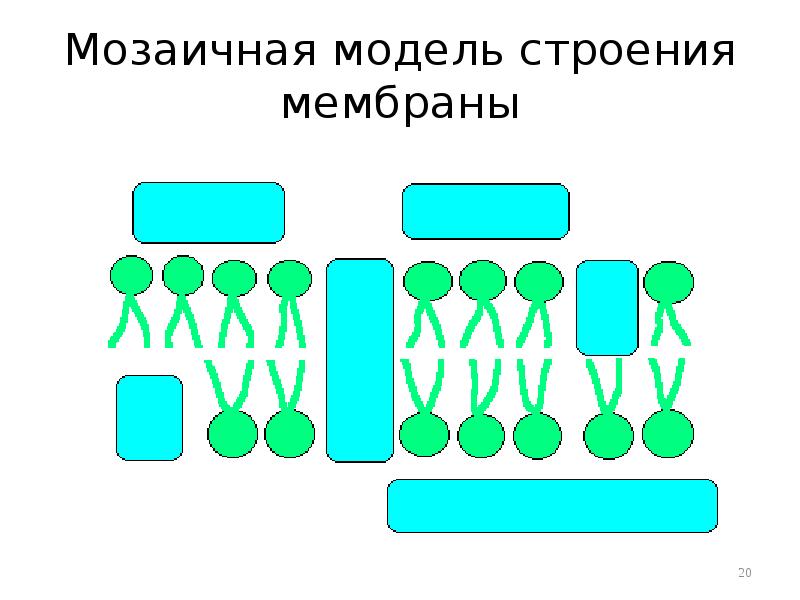
- 20. Мозаичная модель строения мембраны
- 21. Значение поверхностных явлений Всасывание питательных веществ Обмен веществ через стенку кровеносных
- 22. Применение ПАВ Получение растворимых форм лекарственных веществ (твины и спаны) В
- 23. Межфазное поверхностное натяжение на границе жидкость/жидкость Поверхностное натяжение значительно меньше, чем
- 24. Способы измерения поверхностного натяжения жидкости Метод отрыва кольца от поверхности жидкости
- 25. Скачать презентацию
















Слайды и текст этой презентации
Скачать презентацию на тему Поверхностные явления. Уравнение Гиббса можно ниже:
Похожие презентации





























