Процессы и аппараты нефтегазопереработки и нефтехимии презентация
Содержание
- 2. Содержание Лекция 1. Введение Лекция 2. Массообменные процессы. Лекция 3.
- 3. Основной учебник А.И. Скобло, Ю.К. Молоканов, А.И. Владимиров, В.А. Щелкунов ПРОЦЕССЫ
- 4. Дополнительная литература Касаткин А.Г. Основные процессы и аппараты химической технологии. –
- 5. Введение в курс «Процессы и аппараты» Лекция 1.
- 6. Основные понятия и определения Цель курса: Изучение физико-химических основ процессов нефтегазопереработки
- 7. Основные понятия и определения Процесс - всякое естественное или искусственное изменение
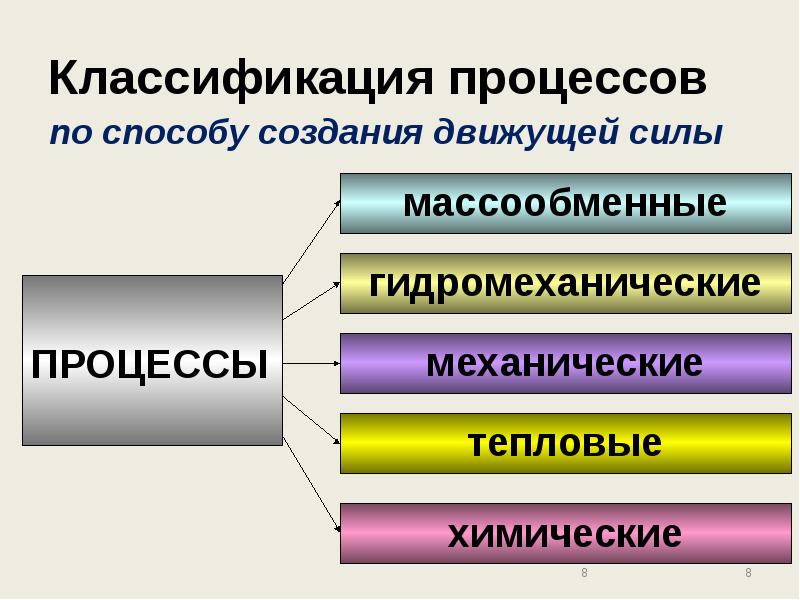
- 8. Классификация процессов по способу создания движущей силы
- 9. Массообменные процессы переход вещества из одной фазы в другую за счет
- 10. Массообменные процессы тв→ж растворение твердых веществ; ж →тв кристаллизация; ж →ж
- 11. Гидромеханические процессы связаны с переработкой суспензий Суспензия – неоднородная система, состоящая
- 12. Гидромеханические процессы 1) перемещение жидкости или газа; 2) перемешивание в жидкой
- 13. Механические процессы - связаны с обработкой твердых тел и их перемещением
- 14. Механические процессы 1) измельчение; 2) рассев; 3) транспортирование; 4) дозирование; 5)
- 15. Тепловые процессы - связаны с теплообменом Движущая сила: разность температур
- 16. Тепловые процессы нагревание; охлаждение; испарение; конденсация;
- 17. Химические процессы - связаны с химическими превращениями участвующих в процессе веществ
- 18. Химические процессы 1) каталитический крекинг; 2) гидроочистка;
- 19. Классификация аппаратов В основу классификации положен основной процесс, определяющий назначение аппарата
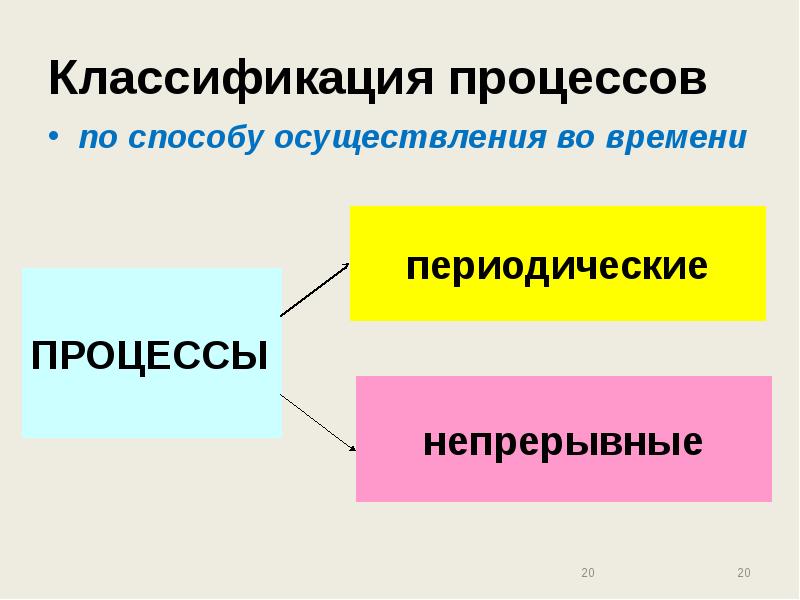
- 20. Классификация процессов по способу осуществления во времени
- 21. Периодические процессы Характеризуются единством места проведения и неустановившимся состоянием во времени
- 22. Непрерывные процессы Характеризуются единством времени проведения всех стадий процесса и установившимся
- 23. Расчет процессов и аппаратов Цель расчета: определение расходов, выбор
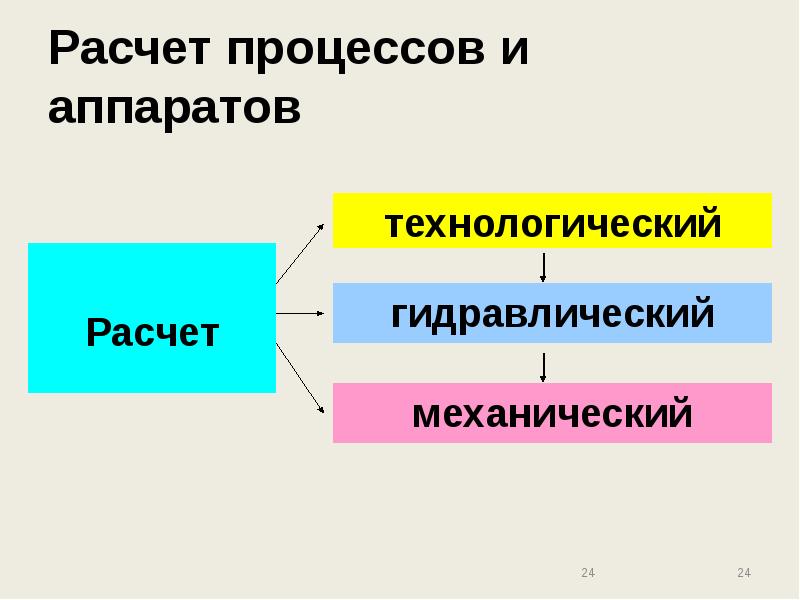
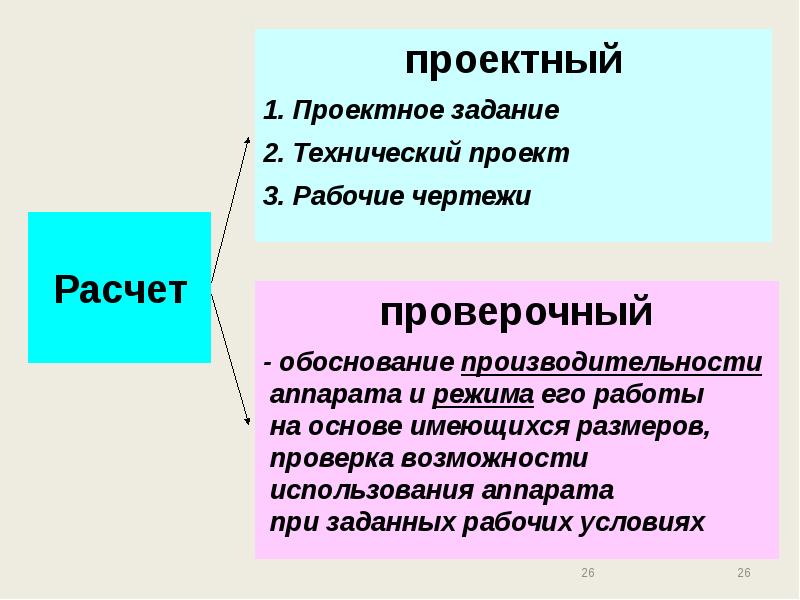
- 24. Расчет процессов и аппаратов
- 25. ТЕХНОЛОГИЧЕСКИЙ РАСЧЕТ ТЕХНОЛОГИЧЕСКИЙ РАСЧЕТ обоснование рабочих параметров процесса (температура, давление), определение
- 27. Теоретические основы курса – основные физические законы: 2-й закон термодинамики, законы,
- 28. Материальный баланс По закону сохранения массы: количество веществ, поступающих на переработку,
- 29. Энергетический баланс По закону сохранения энергии: количество энергии, введенной в процесс,
- 30. Материальные и тепловые балансы Внешние: для завода для установки для аппарата
- 31. Условия равновесия характеризуют статику процесса и показывают пределы, до которых может
- 32. Понятие о концентрации Концентрация – относительное содержание отдельного компонента в смеси
- 33. Способы выражения состава фаз в массовых концентрациях:
- 34. Способы выражения состава фаз в мольных концентрациях:
- 35. Способы выражения состава фаз в объёмных концентрациях;
- 36. Взаимный пересчет массовых и мольных концентраций
- 37. Взаимный пересчет массовых и мольных концентраций
- 38. Средняя мольная масса смеси
- 39. Массообменные процессы Лекция 2.
- 40. Основные признаки массообменных процессов 1) применяют для разделения смесей, 2) участвуют
- 41. Основные признаки массообменных процессов 5) перенос вещества происходит через границу раздела
- 42. Основное уравнение массопередачи Скорость любого процесса определяется количеством вещества М (кг),
- 43. Основное уравнение массопередачи Скорость массопередачи по газовой фазе:
- 44. Основное уравнение массопередачи Разность концентраций изменяется во времени, поэтому используем среднюю
- 45. Основное уравнение массопередачи Размерность коэффициента массопередачи: Размерность движущей силы для газовой
- 46. Основное уравнение массопередачи по жидкой фазе:
- 47. Материальный баланс массообменного процесса Переход вещества из газовой фазы в жидкую
- 48. Материальный баланс массообменного процесса Количество переданной массы по всему аппарату:
- 49. Материальный баланс массообменного процесса Материальный баланс нижней части аппарата до сечения
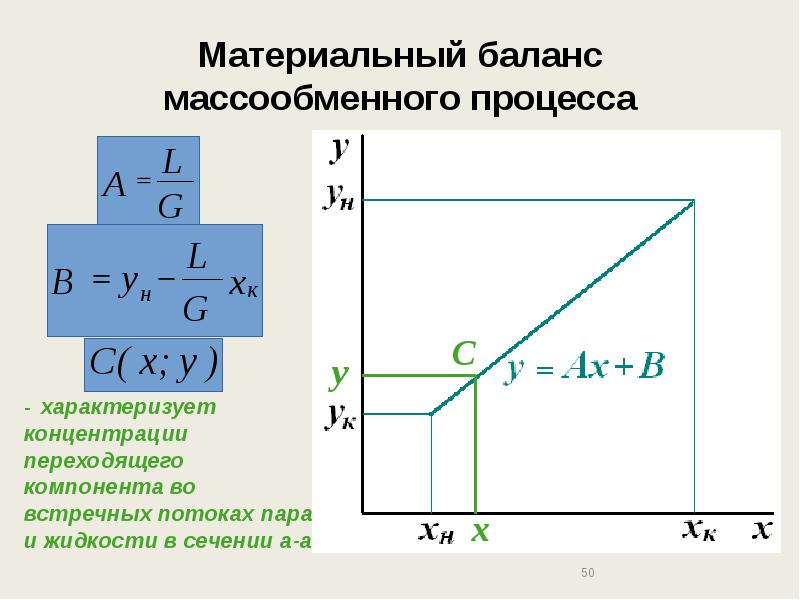
- 50. Материальный баланс массообменного процесса
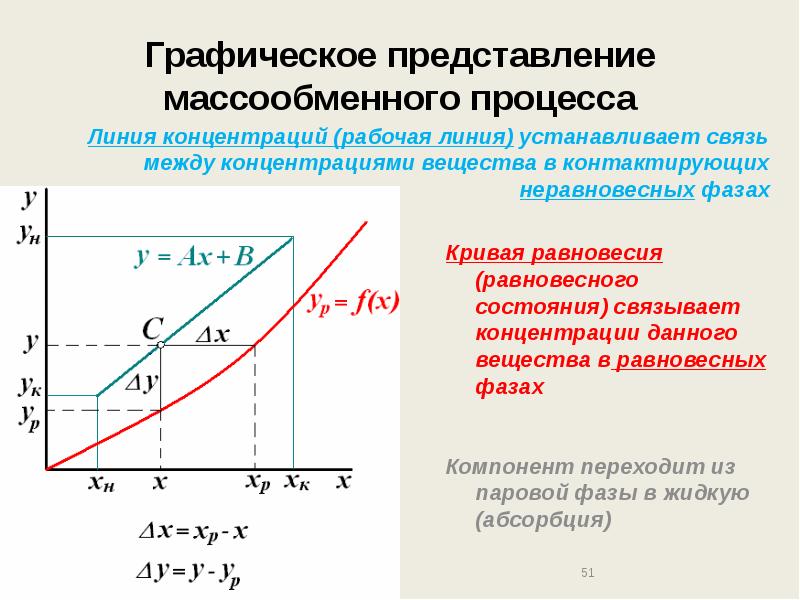
- 51. Графическое представление массообменного процесса Линия концентраций (рабочая линия) устанавливает связь между
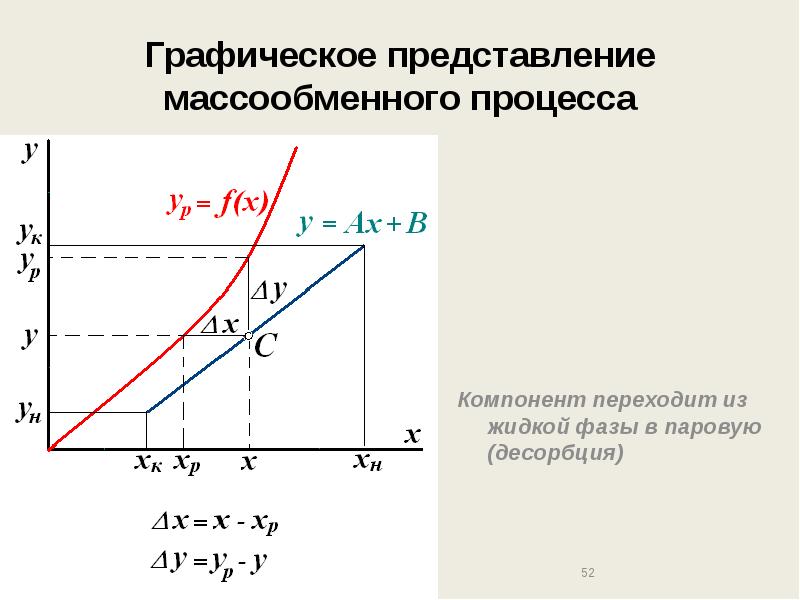
- 52. Графическое представление массообменного процесса Компонент переходит из жидкой
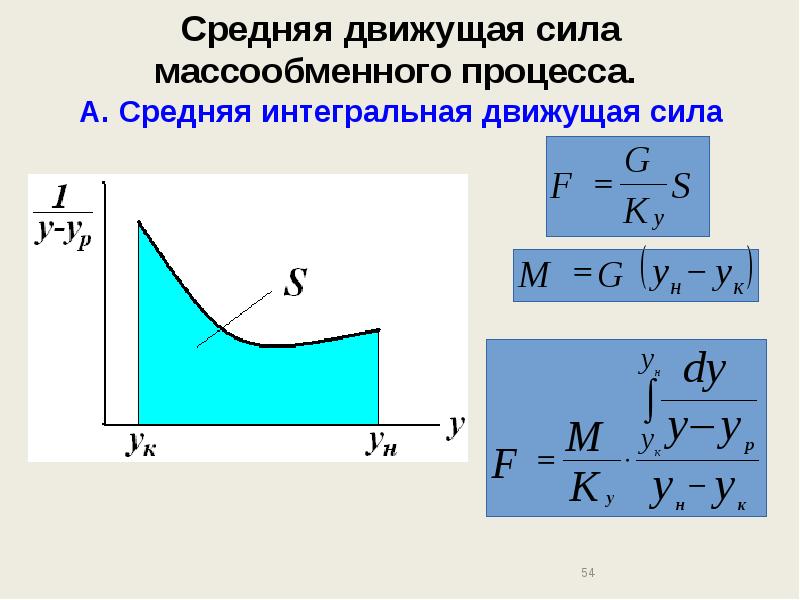
- 53. Средняя движущая сила массообменного процесса. А. Средняя интегральная движущая сила Дифференциальное
- 54. Средняя движущая сила массообменного процесса. А. Средняя интегральная движущая сила
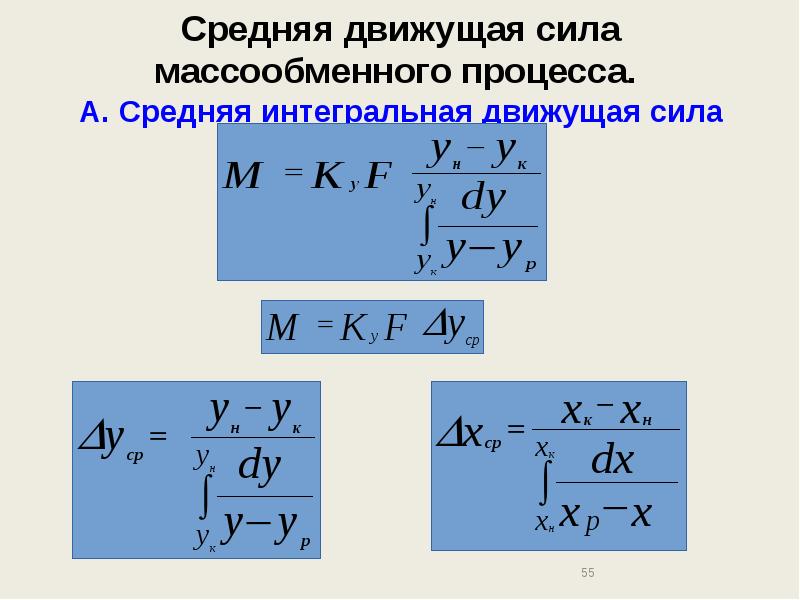
- 55. Средняя движущая сила массообменного процесса. А. Средняя интегральная движущая сила
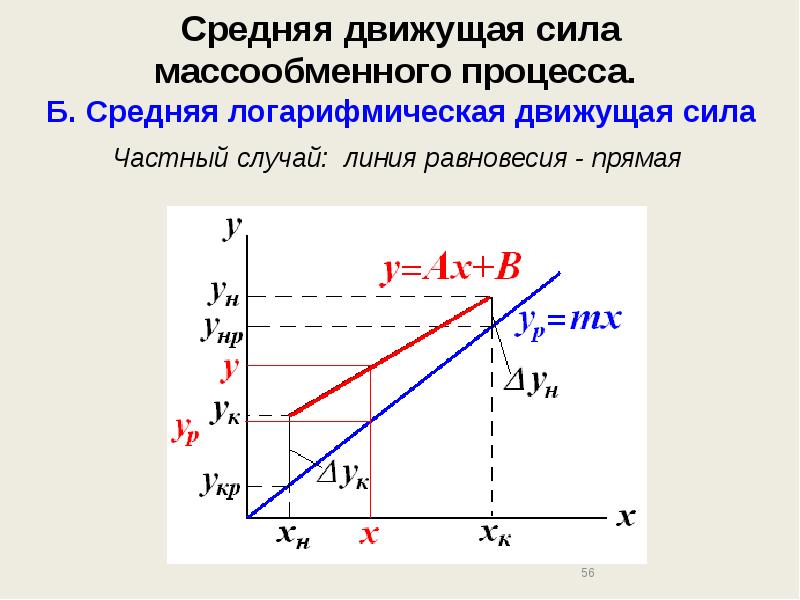
- 56. Средняя движущая сила массообменного процесса. Б. Средняя логарифмическая движущая сила
- 57. Средняя движущая сила массообменного процесса. Б. Средняя логарифмическая движущая сила
- 58. Средняя движущая сила массообменного процесса. Б. Средняя логарифмическая движущая сила
- 59. Средняя движущая сила массообменного процесса. Б. Средняя логарифмическая движущая сила
- 60. Средняя движущая сила массообменного процесса. Б. Средняя логарифмическая движущая сила
- 61. Средняя движущая сила массообменного процесса. Б. Средняя логарифмическая движущая сила
- 62. Лекция 3
- 63. Число единиц переноса. Число теоретических тарелок .
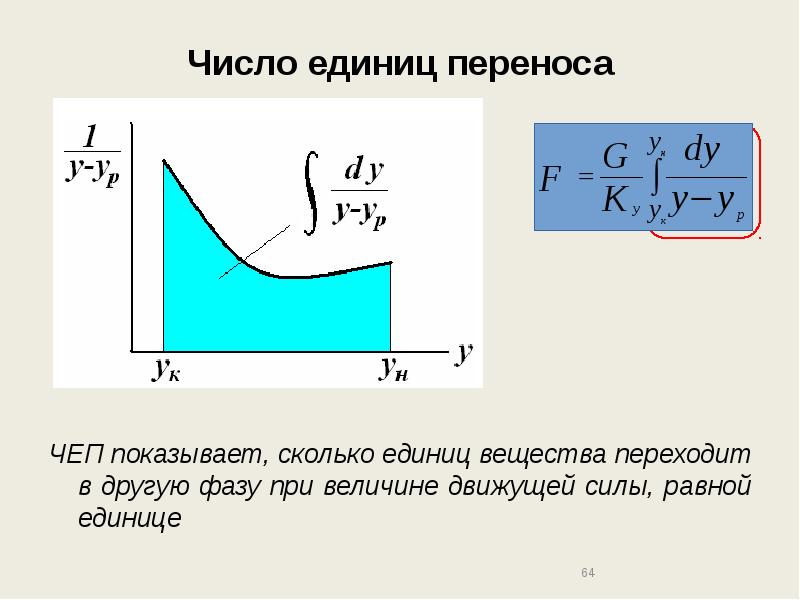
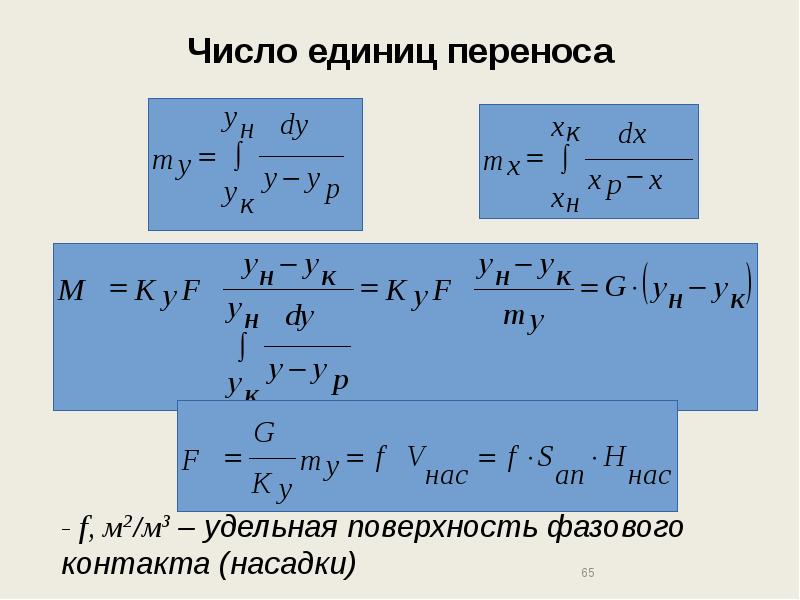
- 64. Число единиц переноса ЧЕП показывает, сколько единиц вещества переходит в другую
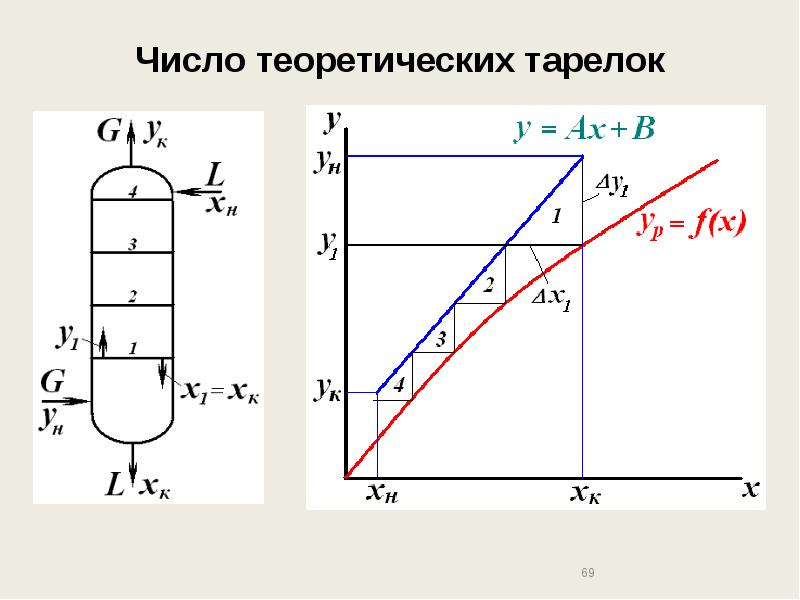
- 68. Число теоретических тарелок Теоретическая тарелка – контактное устройство, которое обеспечивает получение
- 69. Число теоретических тарелок
- 70. Коэффициент полезного действия локальный или точечный к.п.д. к.п.д. тарелки к.п.д. колонны
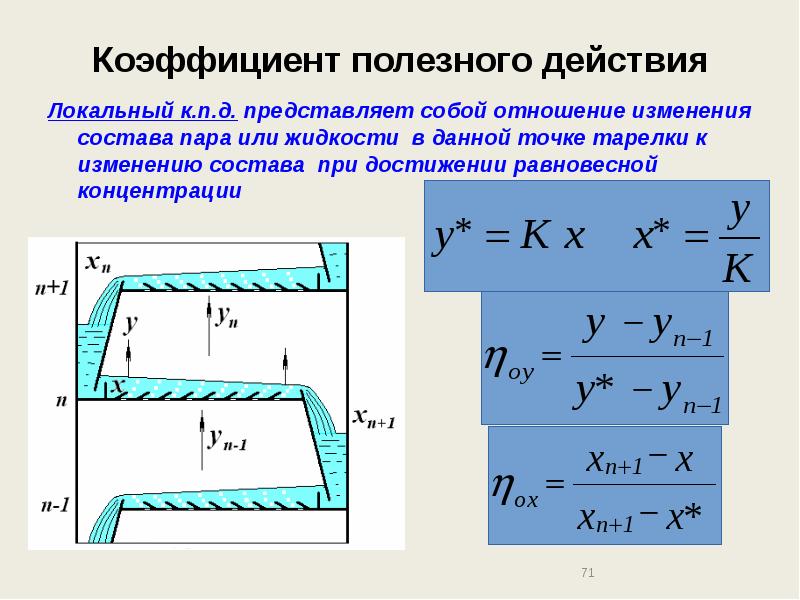
- 71. Коэффициент полезного действия Локальный к.п.д. представляет собой отношение изменения состава пара
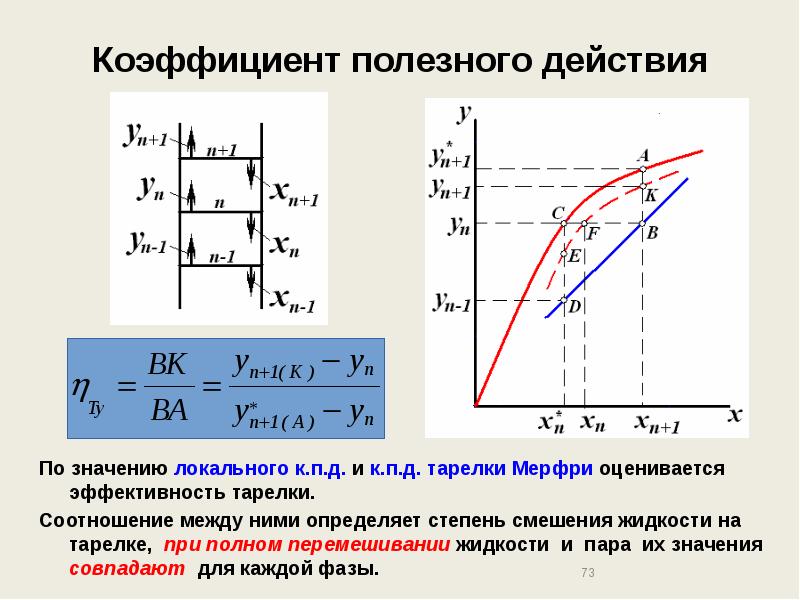
- 72. Коэффициент полезного действия К.п.д. тарелки или к.п.д. Мерфри, представляет собой отношение
- 73. Коэффициент полезного действия По значению локального к.п.д. и к.п.д. тарелки Мерфри
- 74. Коэффициент полезного действия К.п.д. колонны представляет собой отношение числа теоретических тарелок
- 75. Коэффициент полезного действия Для насадочных колонн отношение полной высоты слоя насадки
- 76. Способы расчета числа единиц переноса Лекция 4.
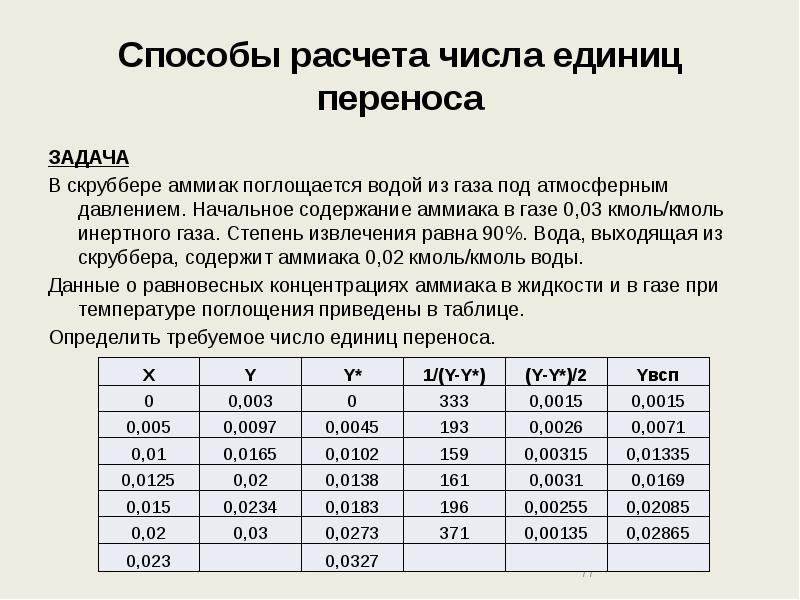
- 77. Способы расчета числа единиц переноса ЗАДАЧА В скруббере аммиак поглощается водой
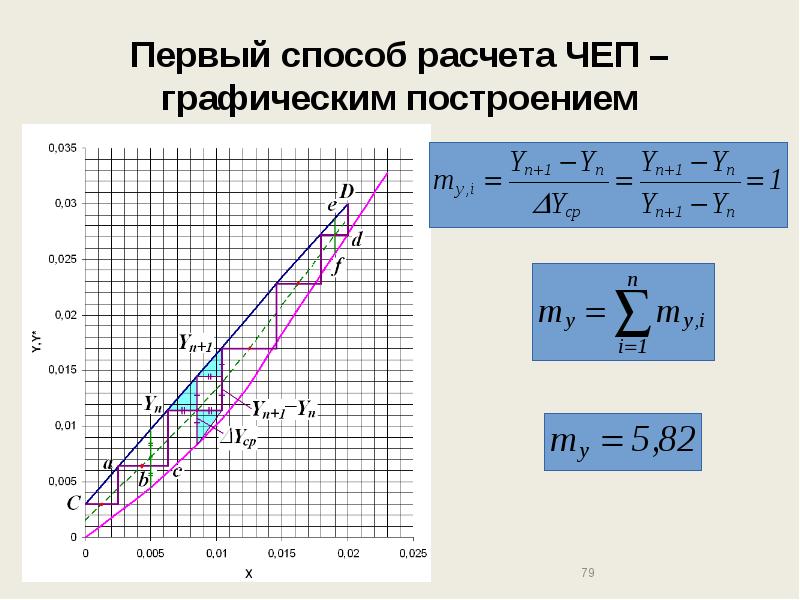
- 78. Первый способ расчета ЧЕП – графическим построением По данным таблицы строим
- 79. Первый способ расчета ЧЕП – графическим построением
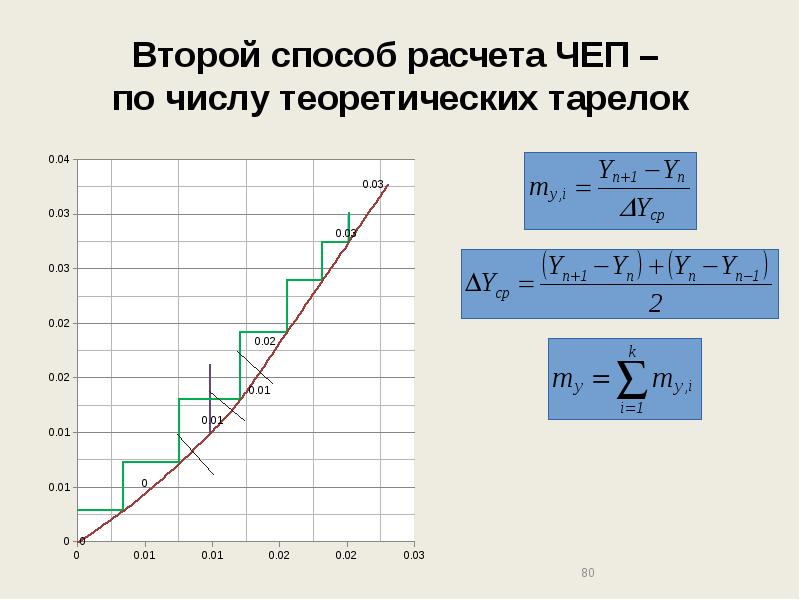
- 80. Второй способ расчета ЧЕП – по числу теоретических тарелок
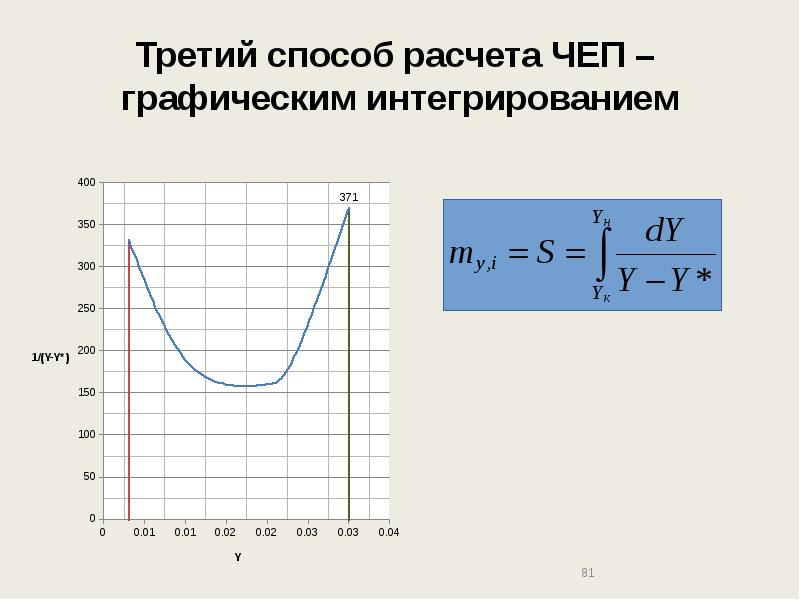
- 81. Третий способ расчета ЧЕП – графическим интегрированием
- 82. РАВНОВЕСНЫЕ СИСТЕМЫ. РАВНОВЕСИЕ ИДЕАЛЬНЫХ РАСТВОРОВ Лекция 5.
- 83. Равновесные системы
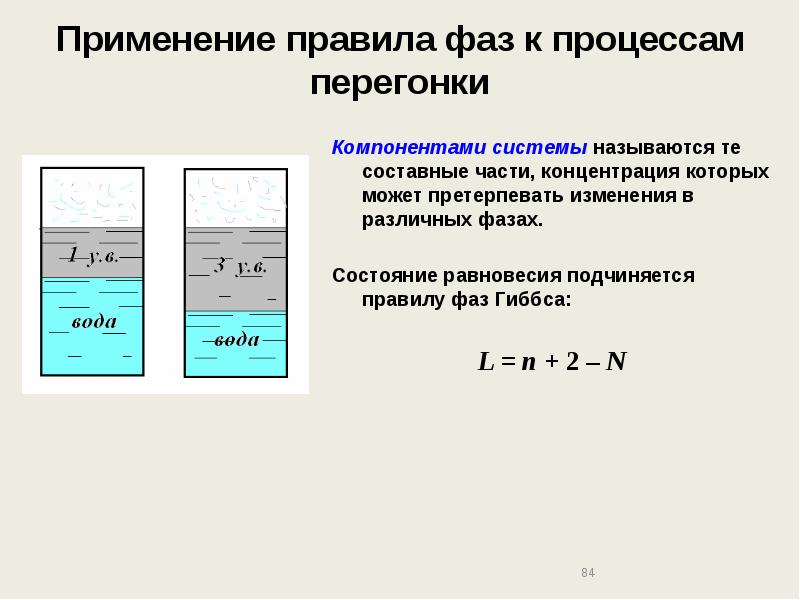
- 84. Применение правила фаз к процессам перегонки Компонентами системы называются те составные
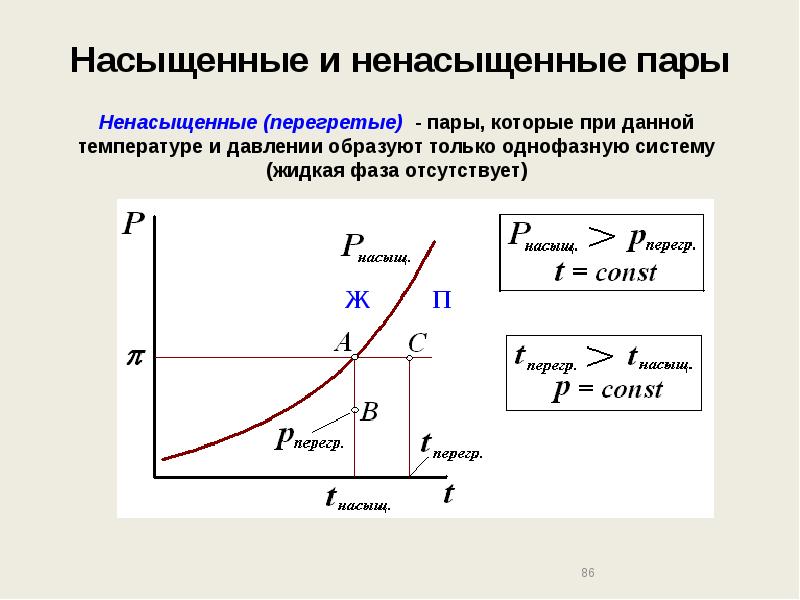
- 85. Насыщенные и ненасыщенные пары Насыщенный – пар, находящийся в равновесии (сосуществующий)
- 86. Насыщенные и ненасыщенные пары
- 87. Насыщенные и ненасыщенные пары
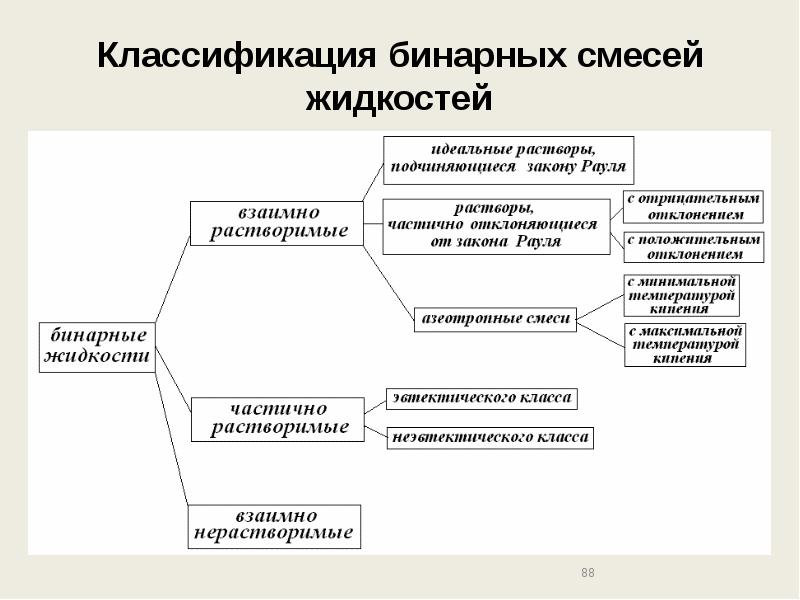
- 88. Классификация бинарных смесей жидкостей
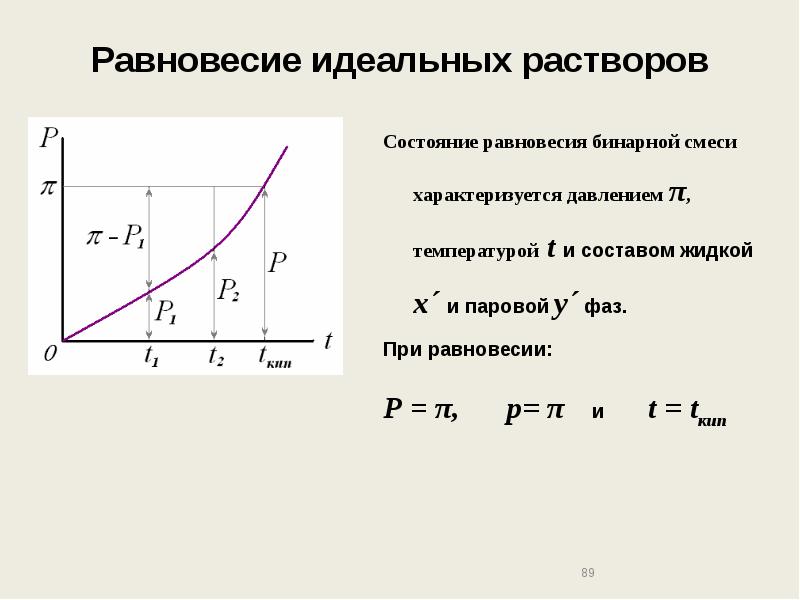
- 89. Равновесие идеальных растворов Состояние равновесия бинарной смеси характеризуется давлением π, температурой
- 90. Равновесие идеальных растворов Закон Дальтона Давление смеси газов равно сумме парциальных
- 91. Равновесие идеальных растворов Закон Рауля Парциальное давление одного из компонентов, входящих
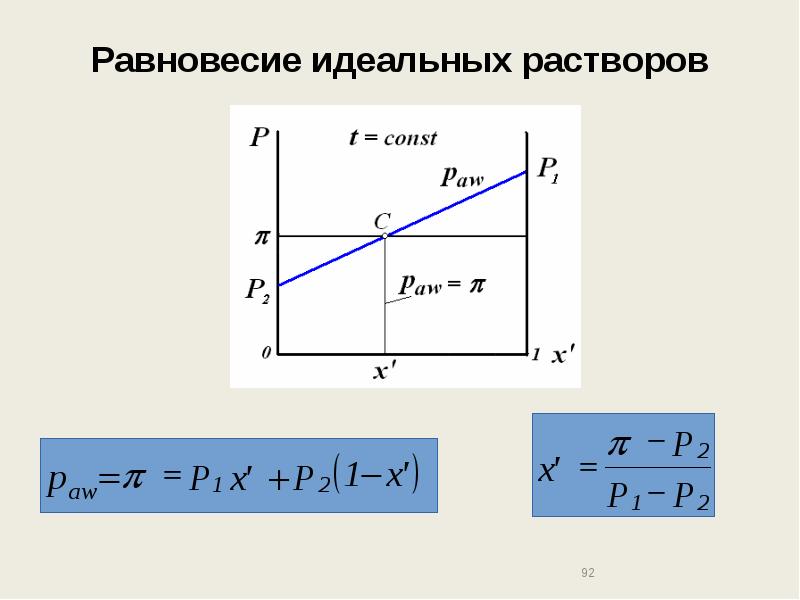
- 92. Равновесие идеальных растворов
- 93. Равновесие идеальных растворов
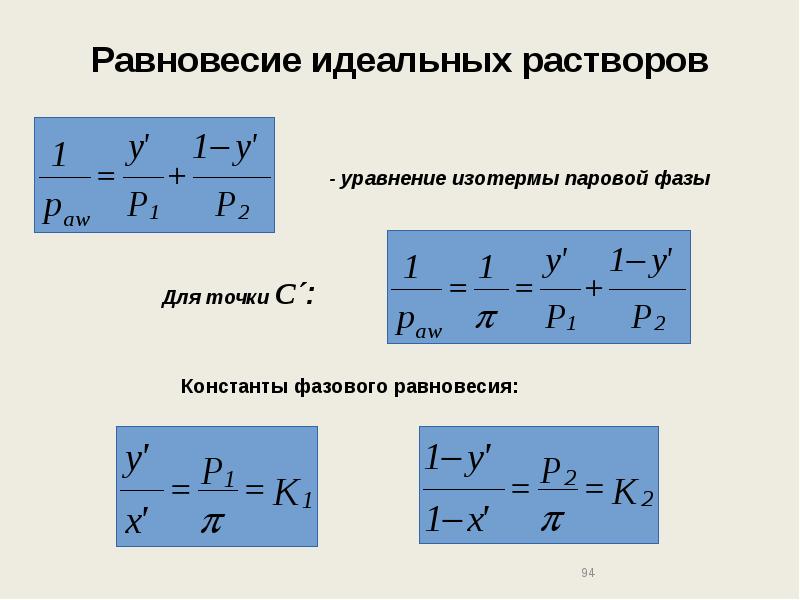
- 94. Равновесие идеальных растворов
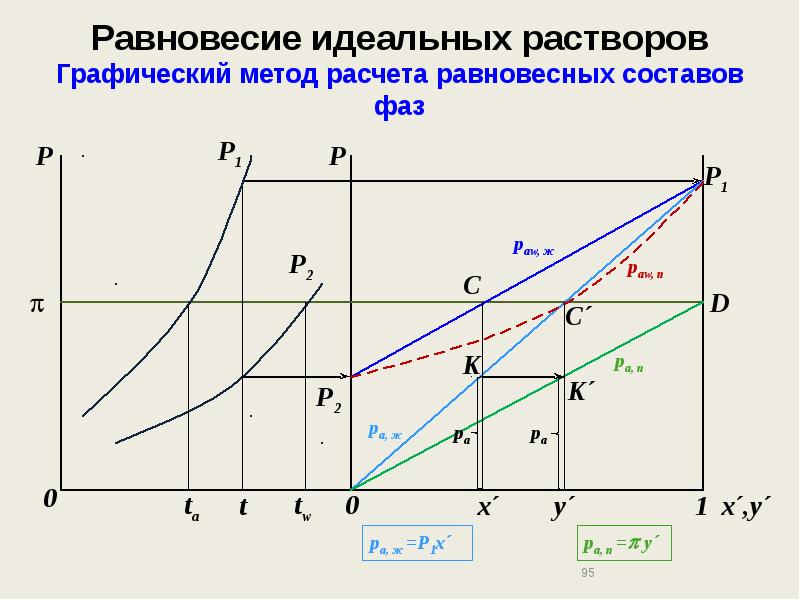
- 95. Равновесие идеальных растворов Графический метод расчета равновесных составов фаз
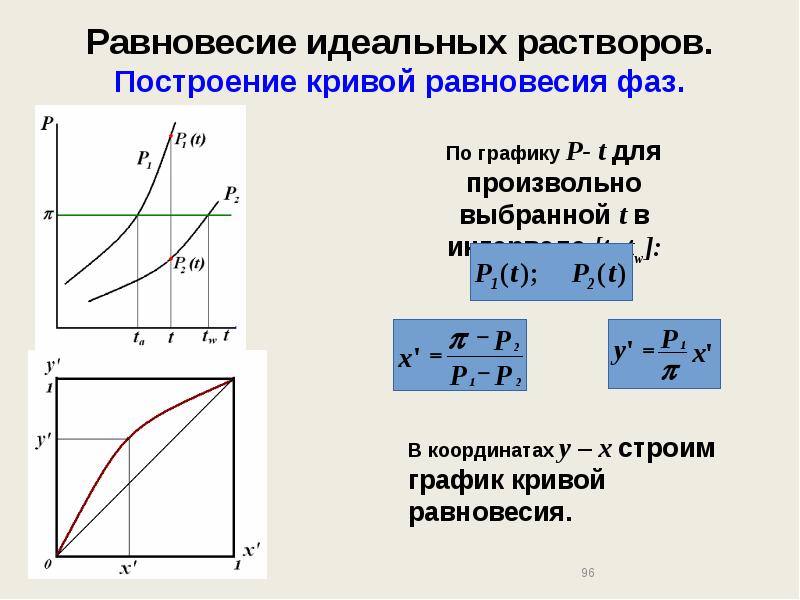
- 96. Равновесие идеальных растворов. Построение кривой равновесия фаз.
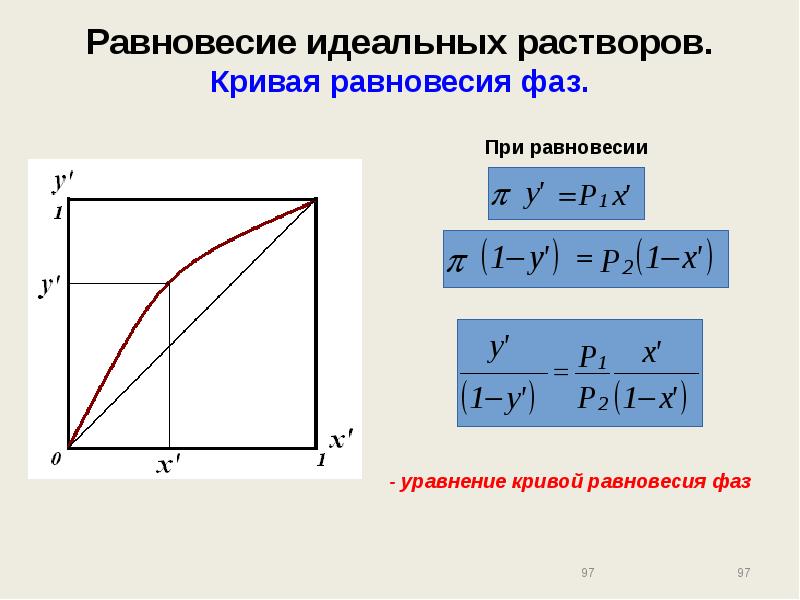
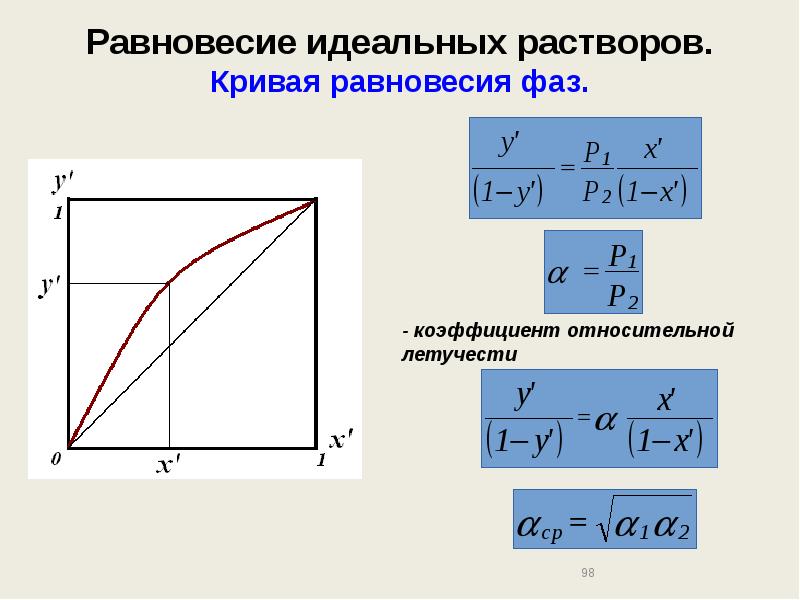
- 97. Равновесие идеальных растворов. Кривая равновесия фаз.
- 98. Равновесие идеальных растворов. Кривая равновесия фаз.
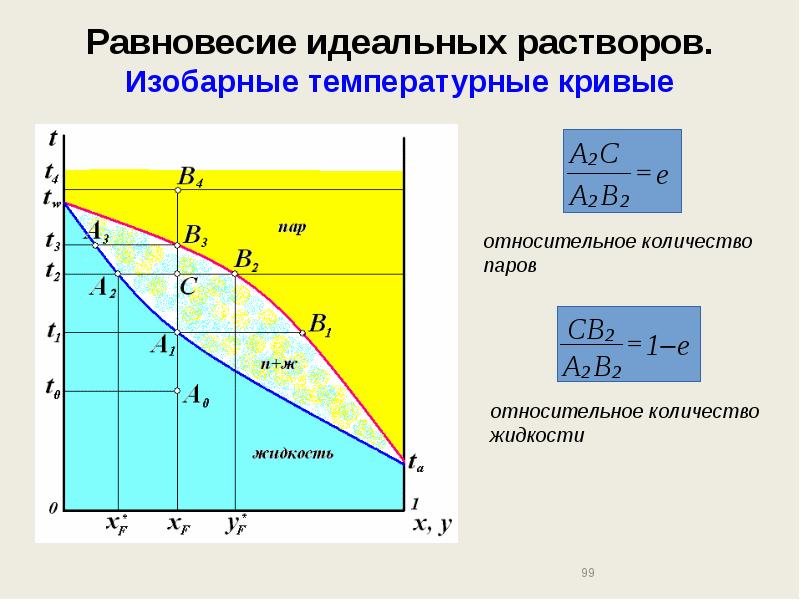
- 99. Равновесие идеальных растворов. Изобарные температурные кривые
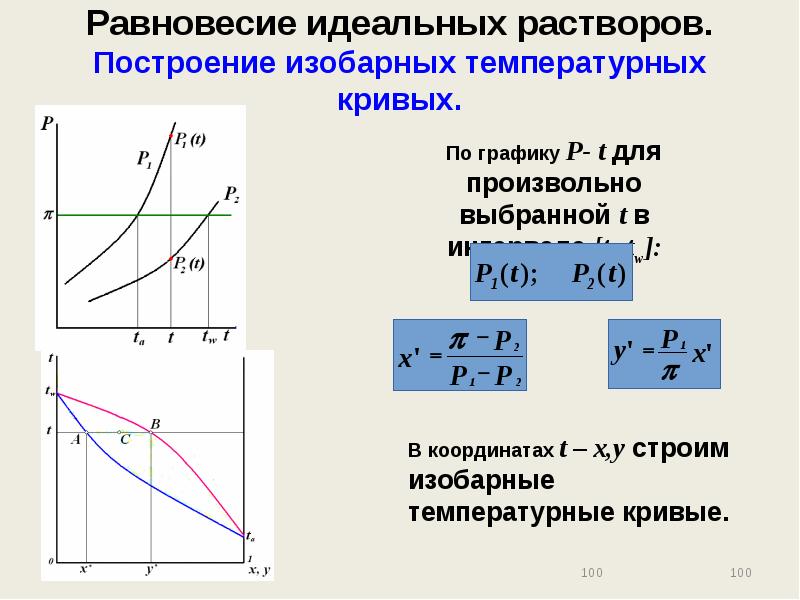
- 100. Равновесие идеальных растворов. Построение изобарных температурных кривых.
- 101. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ (продолжение) Лекция 6.
- 102. Равновесие идеальных растворов. Энтальпийная (тепловая) диаграмма
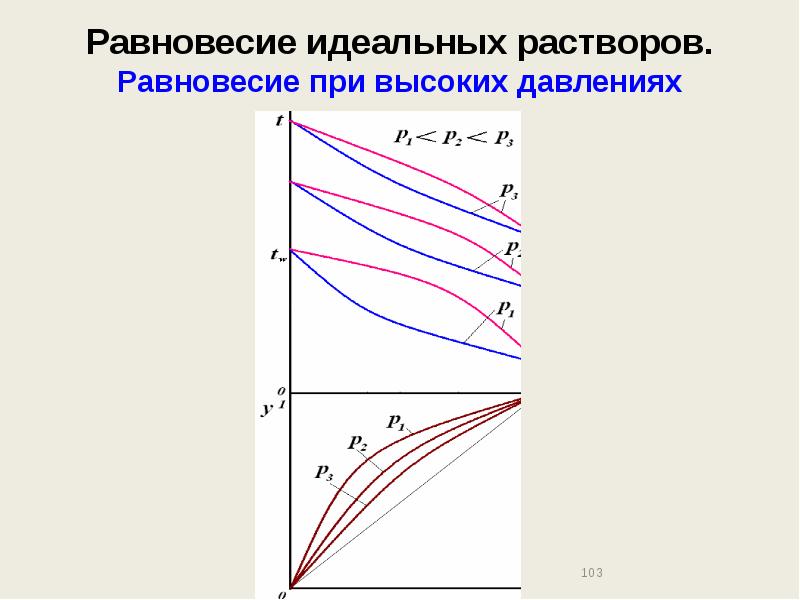
- 103. Равновесие идеальных растворов. Равновесие при высоких давлениях
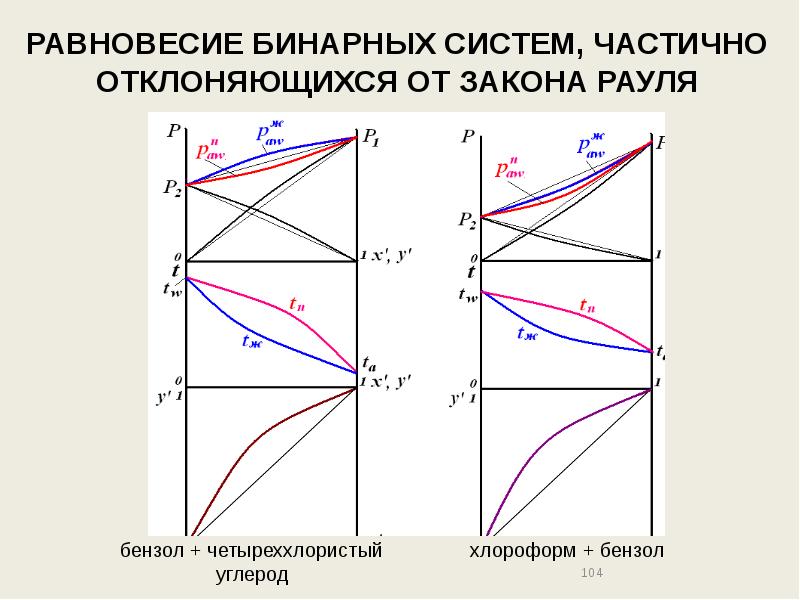
- 104. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ, ЧАСТИЧНО ОТКЛОНЯЮЩИХСЯ ОТ ЗАКОНА РАУЛЯ
- 105. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ, ЧАСТИЧНО ОТКЛОНЯЮЩИХСЯ ОТ ЗАКОНА РАУЛЯ
- 106. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ, ЧАСТИЧНО ОТКЛОНЯЮЩИХСЯ ОТ ЗАКОНА РАУЛЯ
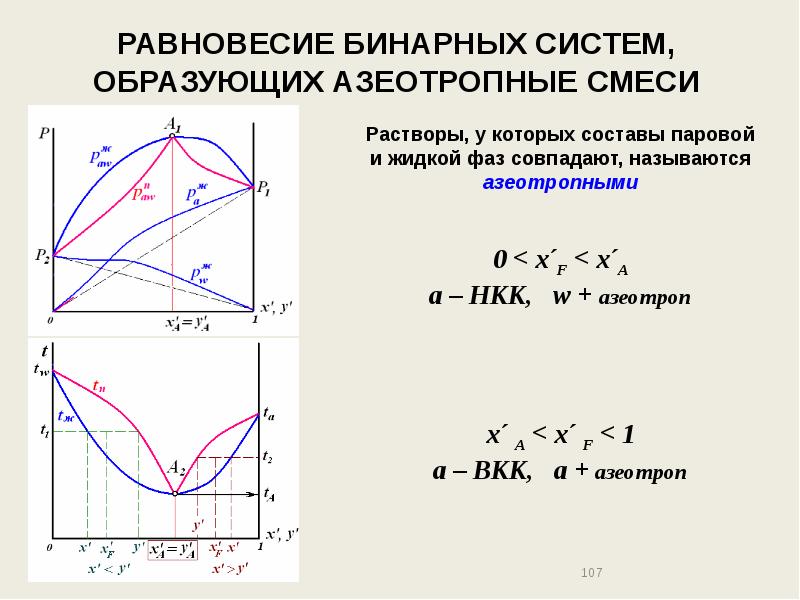
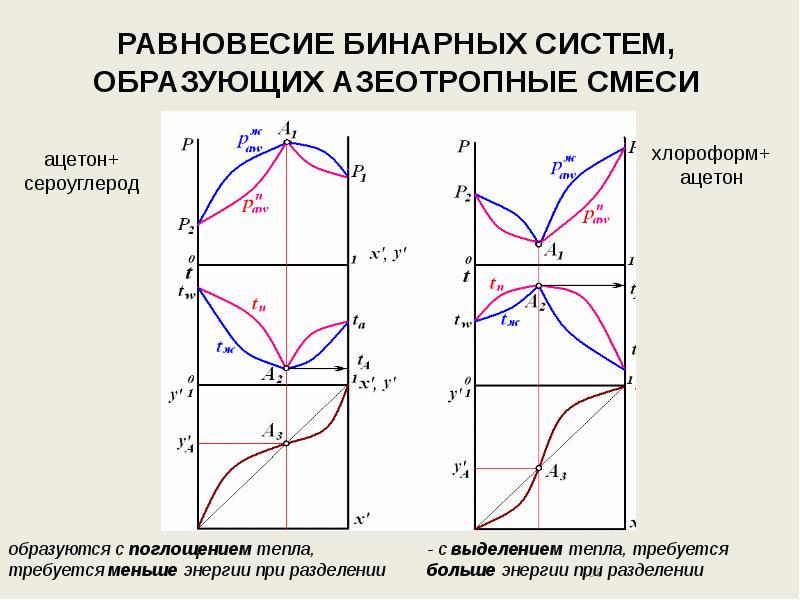
- 107. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ, ОБРАЗУЮЩИХ АЗЕОТРОПНЫЕ СМЕСИ
- 108. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ, ОБРАЗУЮЩИХ АЗЕОТРОПНЫЕ СМЕСИ
- 109. РАВНОВЕСИЕ БИНАРНЫХ СИСТЕМ, ОБРАЗУЮЩИХ АЗЕОТРОПНЫЕ СМЕСИ Особенности гомогенных в жидкой фазе
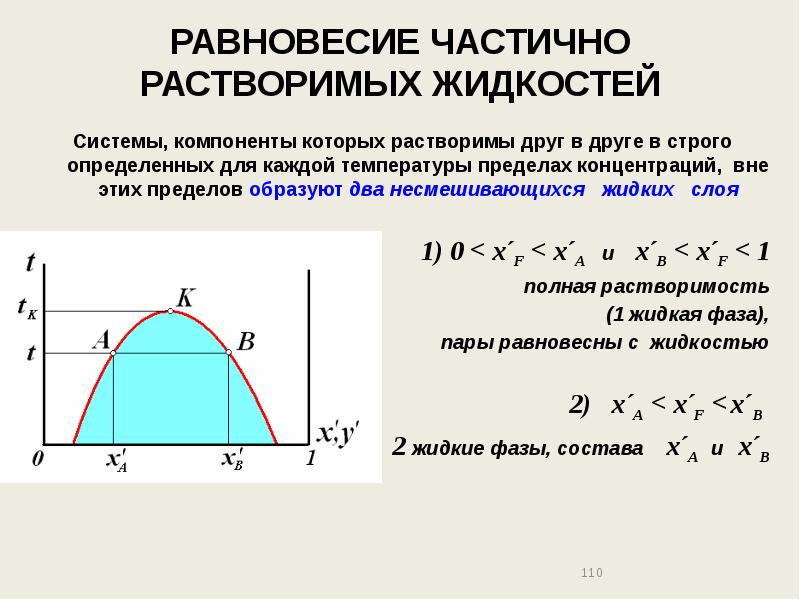
- 110. РАВНОВЕСИЕ ЧАСТИЧНО РАСТВОРИМЫХ ЖИДКОСТЕЙ Системы, компоненты которых растворимы друг в друге
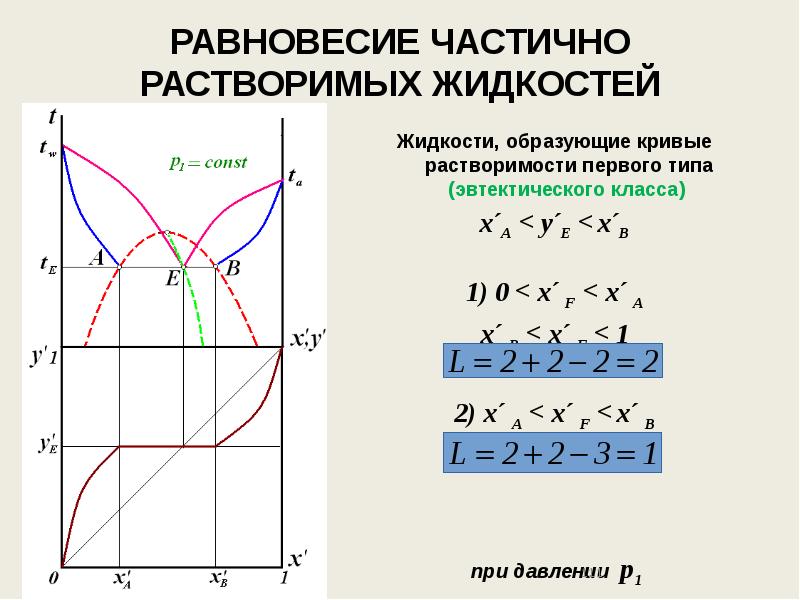
- 111. РАВНОВЕСИЕ ЧАСТИЧНО РАСТВОРИМЫХ ЖИДКОСТЕЙ Жидкости, образующие кривые растворимости первого типа (эвтектического
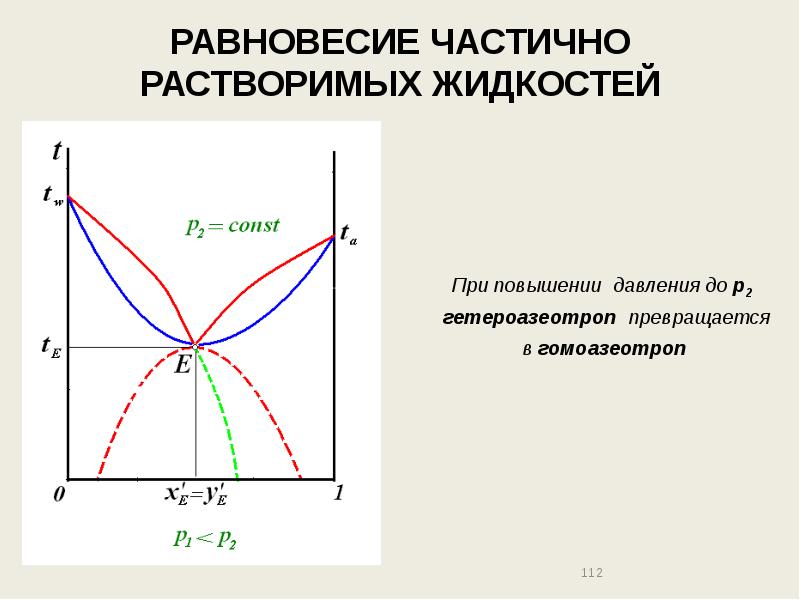
- 112. РАВНОВЕСИЕ ЧАСТИЧНО РАСТВОРИМЫХ ЖИДКОСТЕЙ При повышении давления до р2 гетероазеотроп
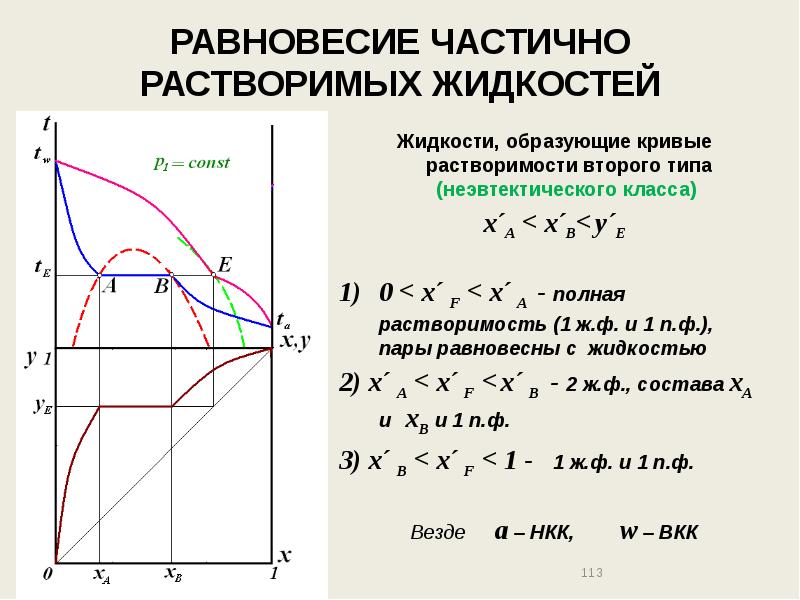
- 113. РАВНОВЕСИЕ ЧАСТИЧНО РАСТВОРИМЫХ ЖИДКОСТЕЙ Жидкости, образующие кривые растворимости второго типа (неэвтектического
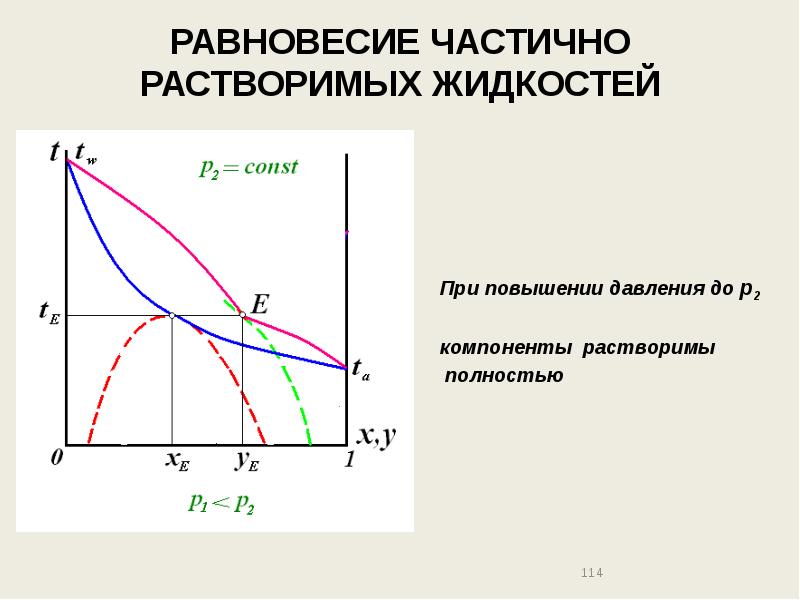
- 114. РАВНОВЕСИЕ ЧАСТИЧНО РАСТВОРИМЫХ ЖИДКОСТЕЙ При повышении давления до р2
- 115. РАВНОВЕСИЕ ВЗАИМНО НЕРАСТВОРИМЫХ ЖИДКОСТЕЙ Лекция 7.
- 116. РАВНОВЕСИЕ ВЗАИМНО НЕРАСТВОРИМЫХ ЖИДКОСТЕЙ 2 ж.ф. + 1 п.ф.
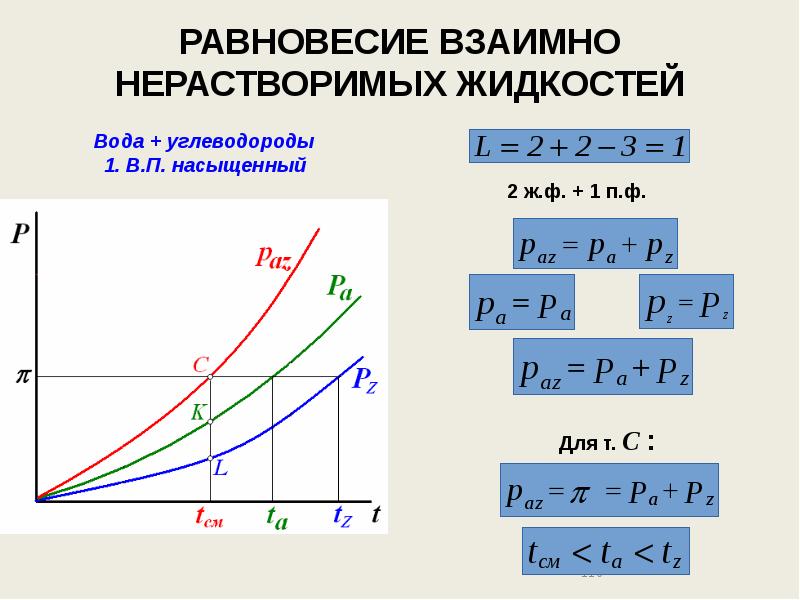
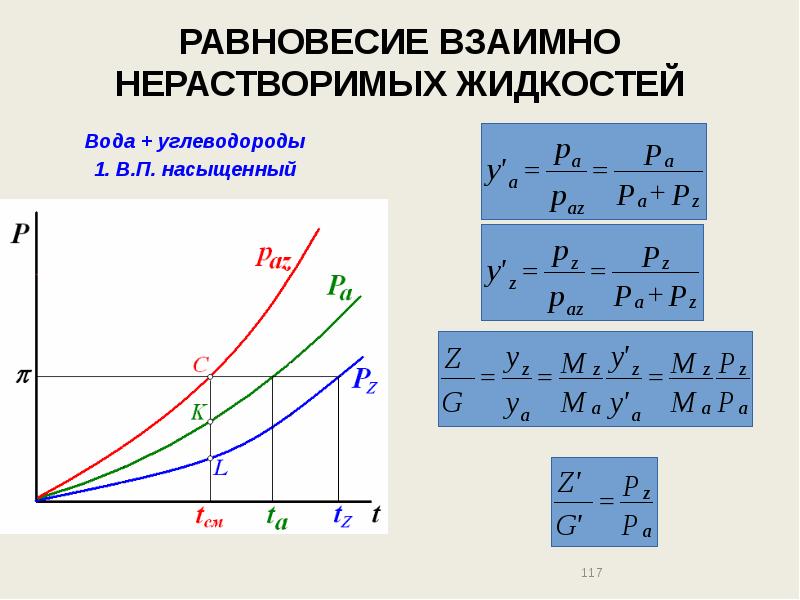
- 117. РАВНОВЕСИЕ ВЗАИМНО НЕРАСТВОРИМЫХ ЖИДКОСТЕЙ Вода + углеводороды 1. В.П. насыщенный
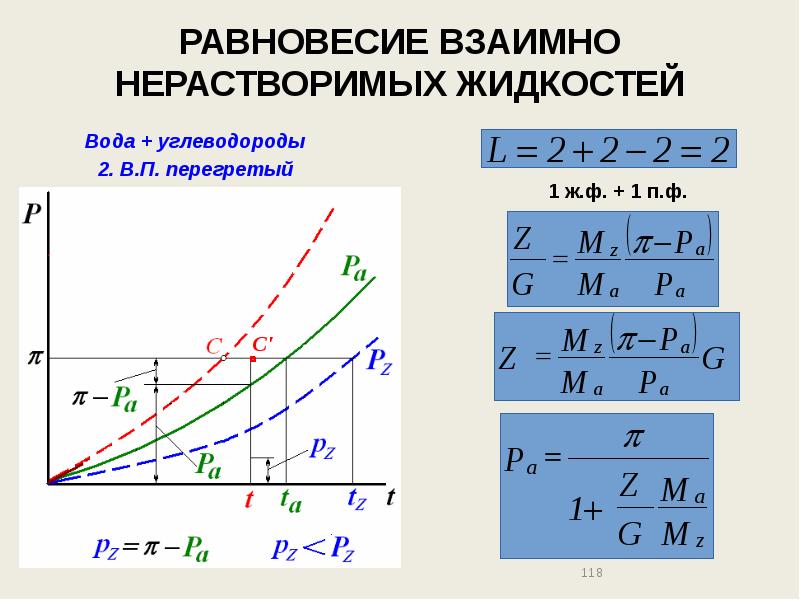
- 118. РАВНОВЕСИЕ ВЗАИМНО НЕРАСТВОРИМЫХ ЖИДКОСТЕЙ Вода + углеводороды 2. В.П. перегретый
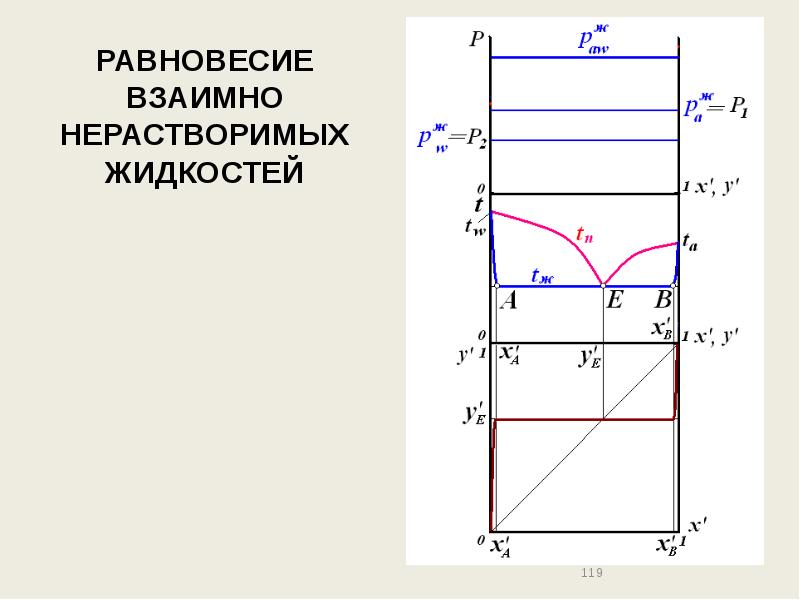
- 119. РАВНОВЕСИЕ ВЗАИМНО НЕРАСТВОРИМЫХ ЖИДКОСТЕЙ
- 120. РАВНОВЕСИЕ БИНАРНОЙ СИСТЕМЫ В ПРИСУТСТВИИ ВОДЯНОГО ПАРА В.П. + 2 углеводорода
- 121. РАВНОВЕСИЕ БИНАРНОЙ СИСТЕМЫ В ПРИСУТСТВИИ ВОДЯНОГО ПАРА В.П. + 2 углеводорода
- 122. РАВНОВЕСИЕ БИНАРНОЙ СИСТЕМЫ В ПРИСУТСТВИИ ВОДЯНОГО ПАРА В.П. + 2 углеводорода
- 123. Основы перегонки
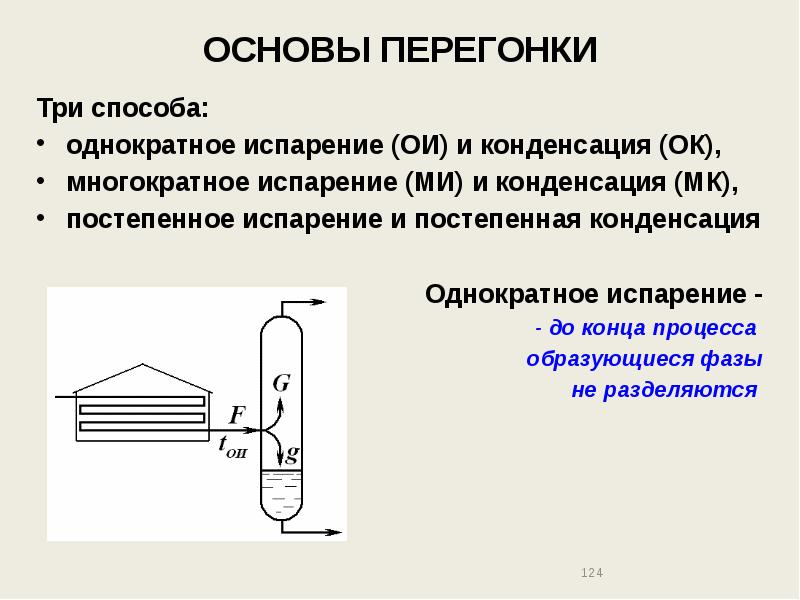
- 124. ОСНОВЫ ПЕРЕГОНКИ Три способа: однократное испарение (ОИ) и конденсация (ОК), многократное
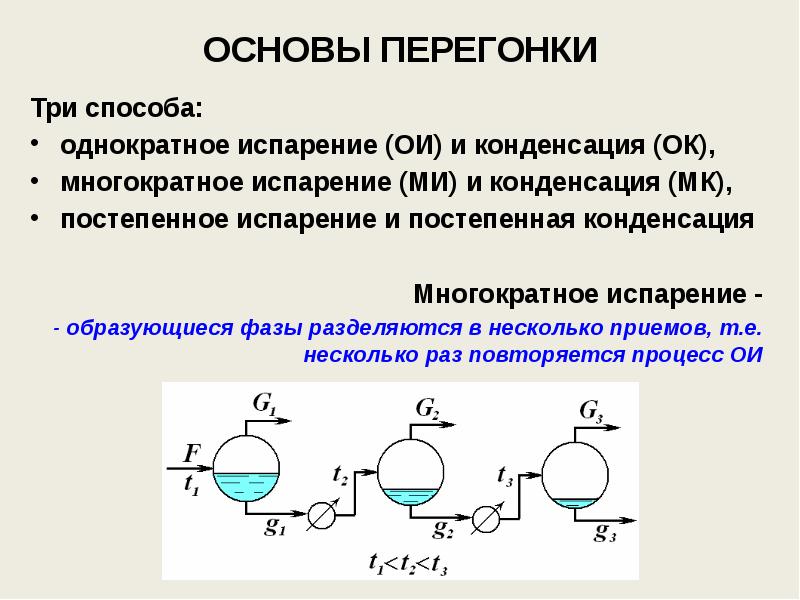
- 125. ОСНОВЫ ПЕРЕГОНКИ Три способа: однократное испарение (ОИ) и конденсация (ОК), многократное
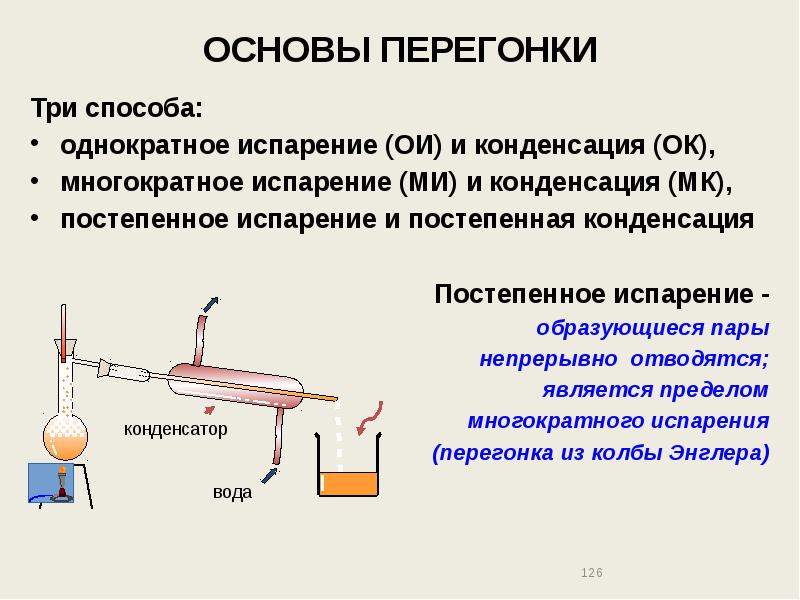
- 126. ОСНОВЫ ПЕРЕГОНКИ Три способа: однократное испарение (ОИ) и конденсация (ОК), многократное
- 127. Основы перегонки Лекция 9
- 128. Обозначения F – расход сырья, поступающего на перегонку G – расход
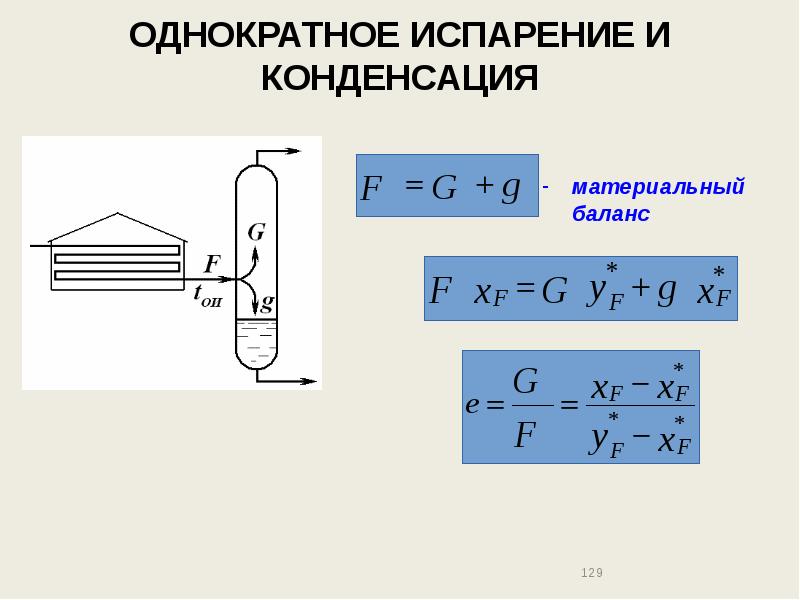
- 129. ОДНОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ материальный баланс
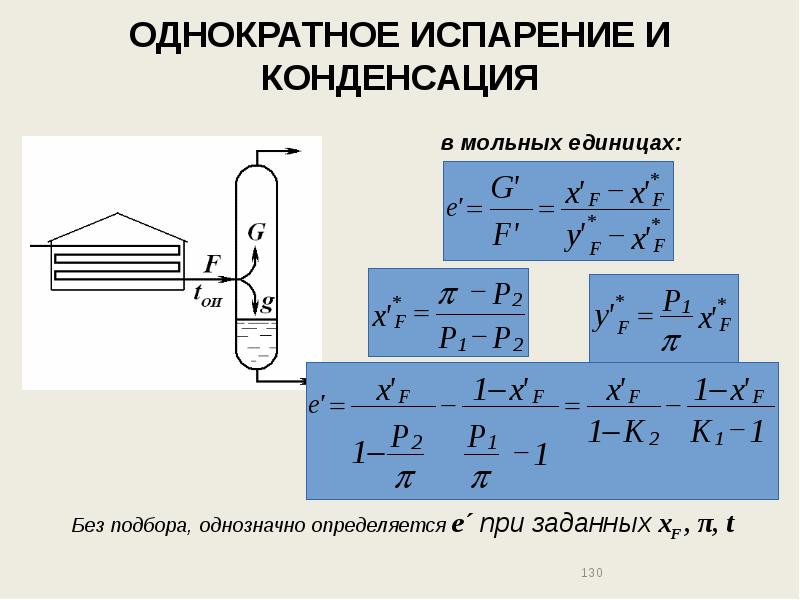
- 130. ОДНОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ в мольных единицах:
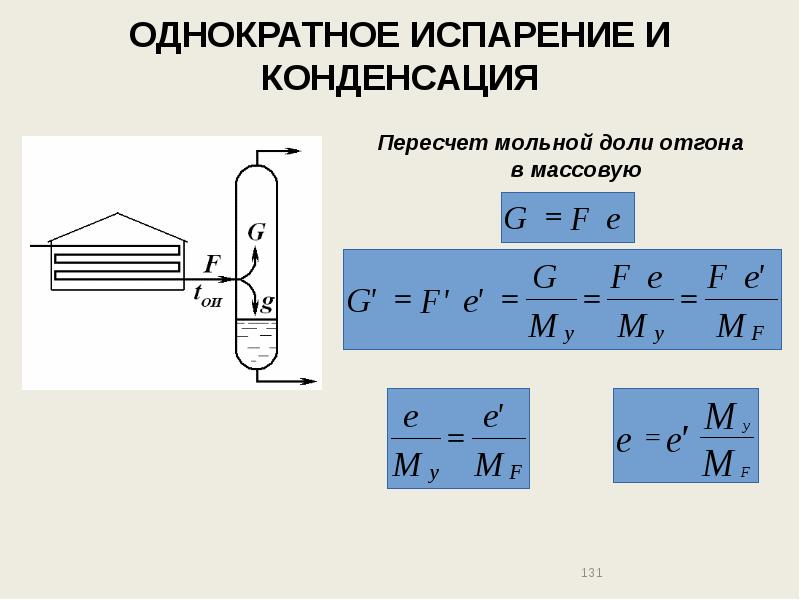
- 131. ОДНОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ Пересчет мольной доли отгона в массовую
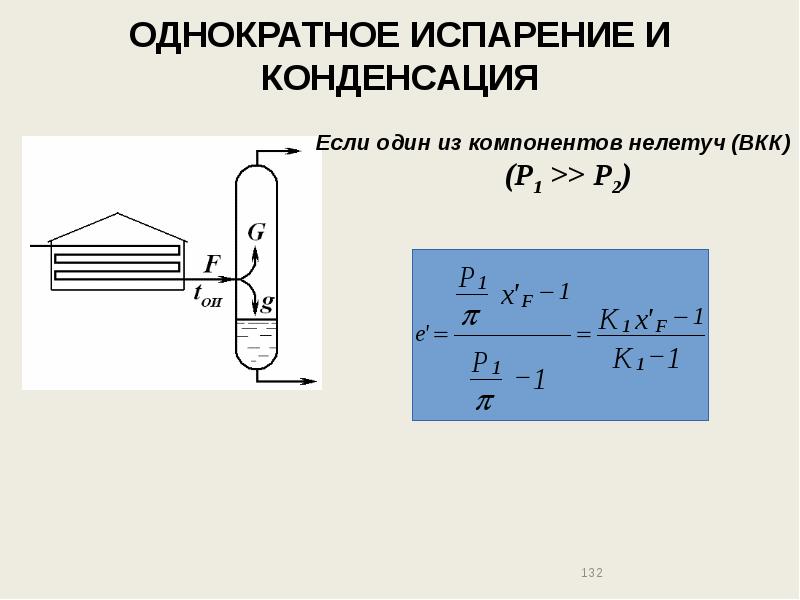
- 132. ОДНОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ Если один из компонентов нелетуч (ВКК) (Р1
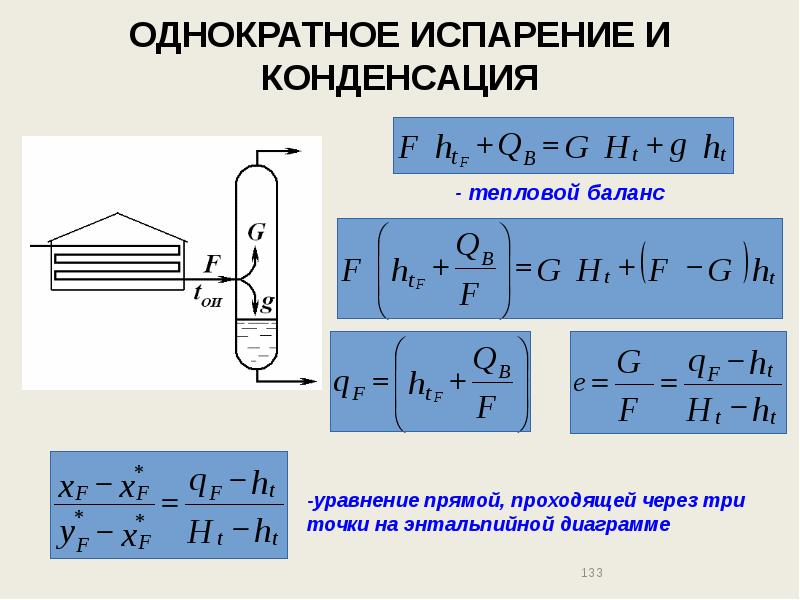
- 133. ОДНОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ - тепловой баланс
- 134. ОДНОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ
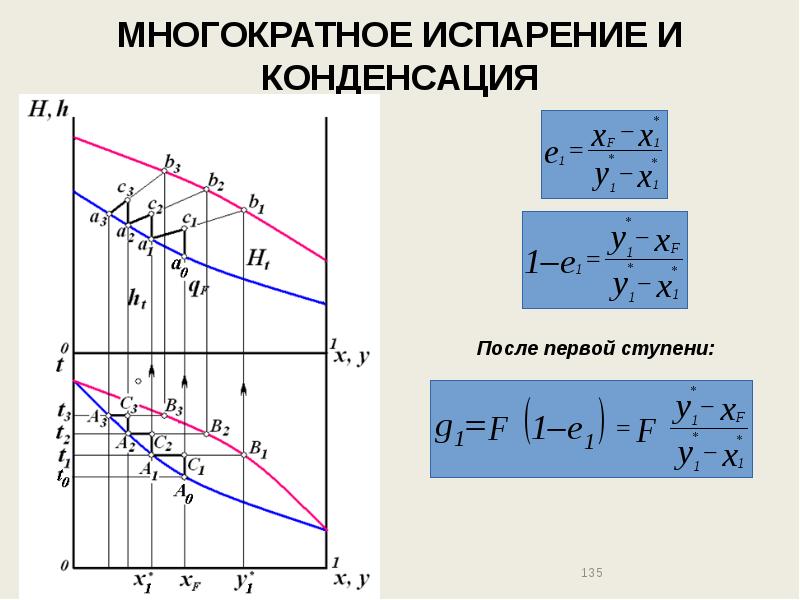
- 135. МНОГОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ
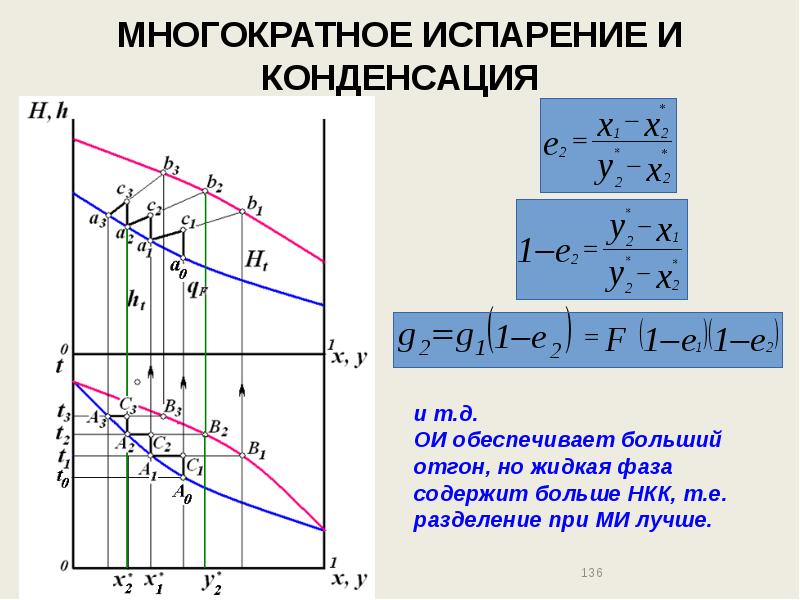
- 136. МНОГОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ
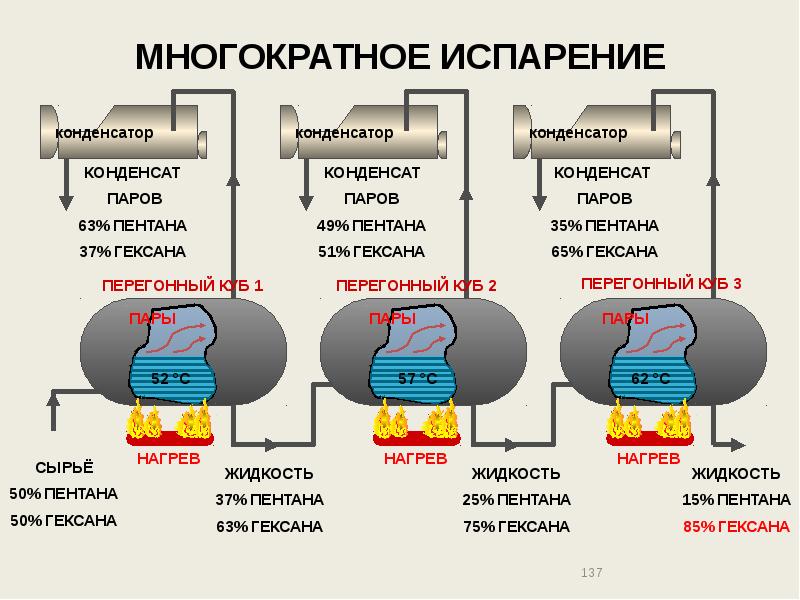
- 137. МНОГОКРАТНОЕ ИСПАРЕНИЕ
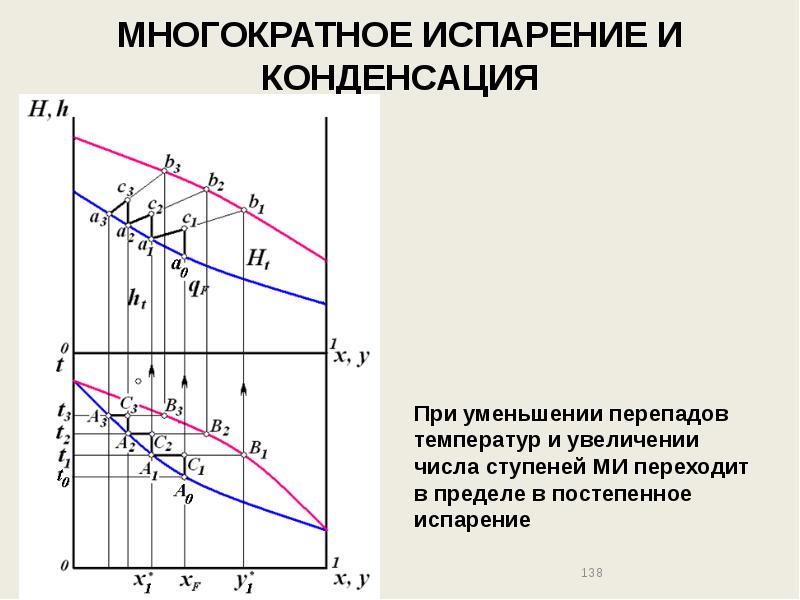
- 138. МНОГОКРАТНОЕ ИСПАРЕНИЕ И КОНДЕНСАЦИЯ
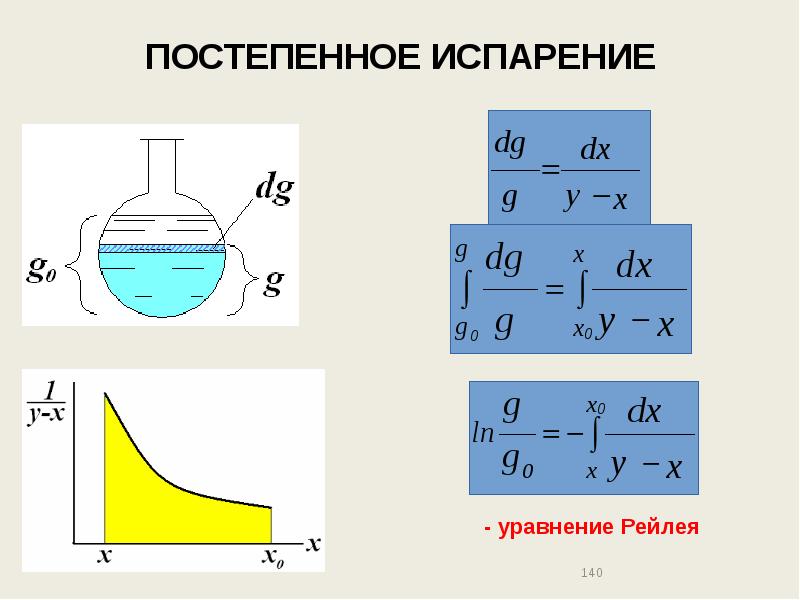
- 139. ПОСТЕПЕННОЕ ИСПАРЕНИЕ Начало перегонки: g0, x0 В рассматриваемый момент: g, x
- 140. ПОСТЕПЕННОЕ ИСПАРЕНИЕ - уравнение Рейлея
- 141. ПОСТЕПЕННАЯ КОНДЕНСАЦИЯ
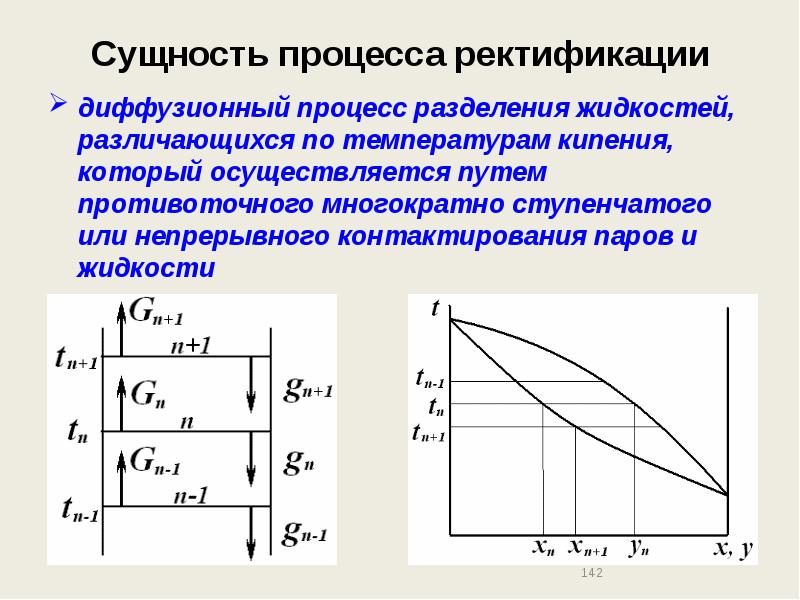
- 142. Сущность процесса ректификации диффузионный процесс разделения жидкостей, различающихся по температурам кипения,
- 143. Ректификация Учебный фильм
- 144. ректификация Лекция 10
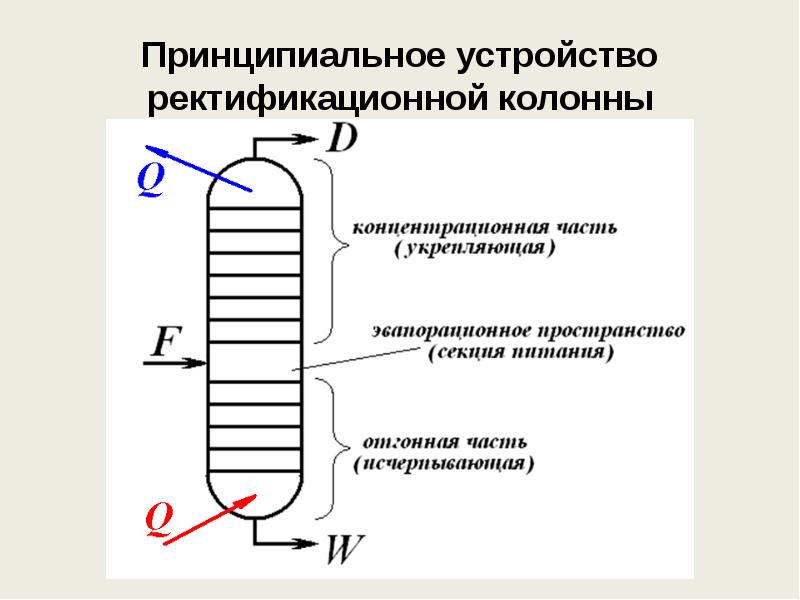
- 145. Принципиальное устройство ректификационной колонны
- 146. Принципиальное устройство ректификационной колонны
- 147. Материальный баланс колонны
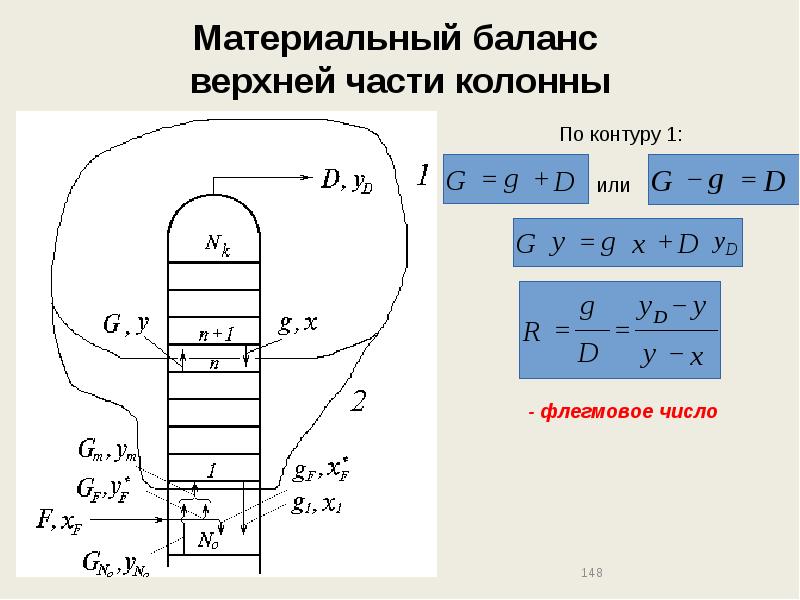
- 148. Материальный баланс верхней части колонны
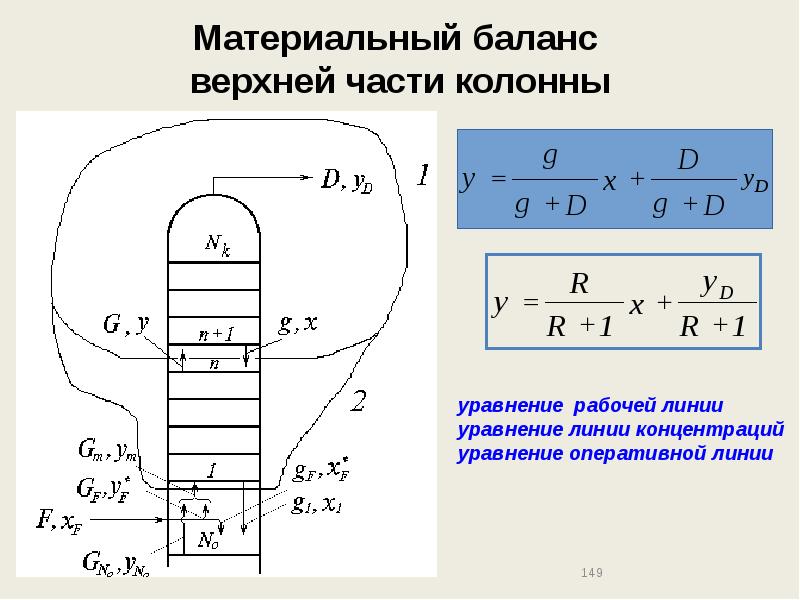
- 149. Материальный баланс верхней части колонны
- 150. Материальный баланс верхней части колонны
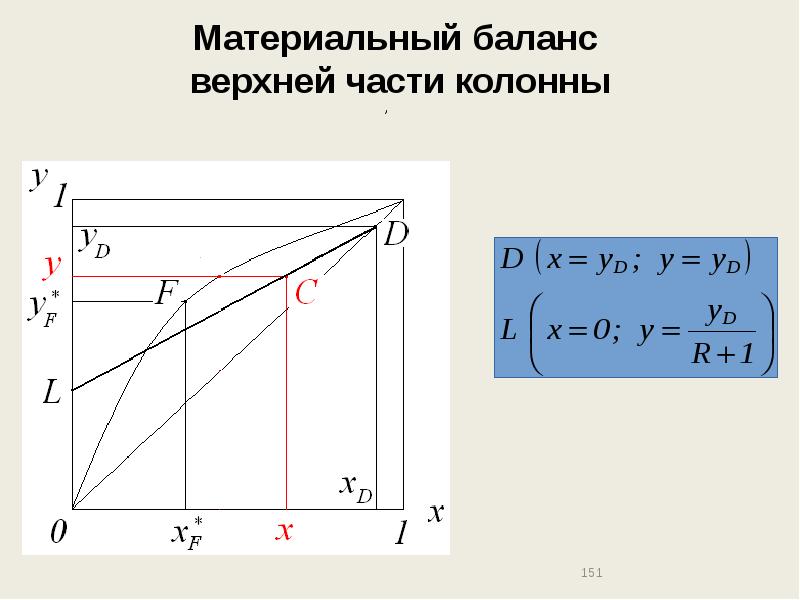
- 151. Материальный баланс верхней части колонны
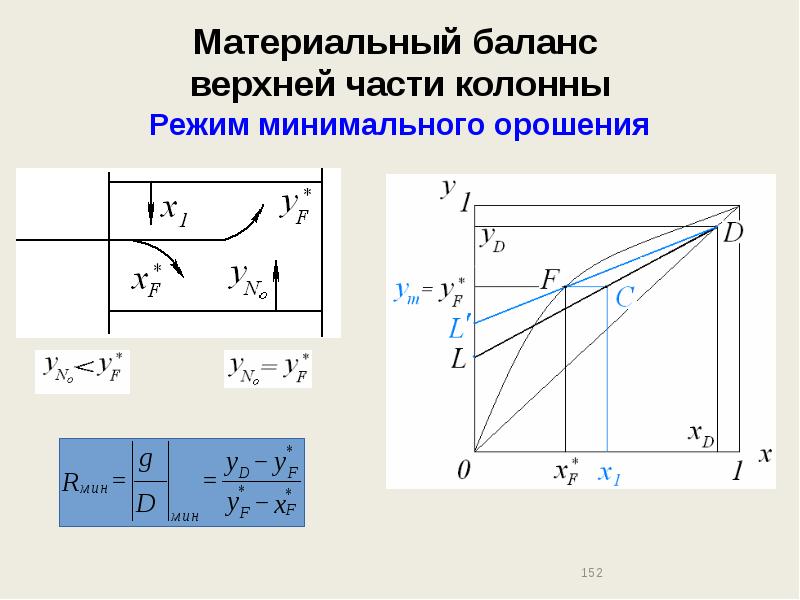
- 152. Материальный баланс верхней части колонны Режим минимального орошения
- 153. Материальный и тепловой баланс колонны Лекция 11.
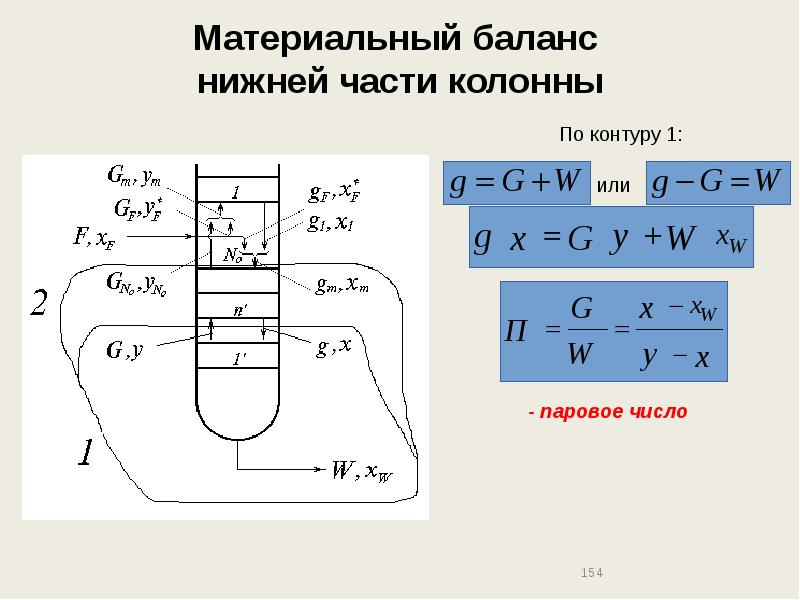
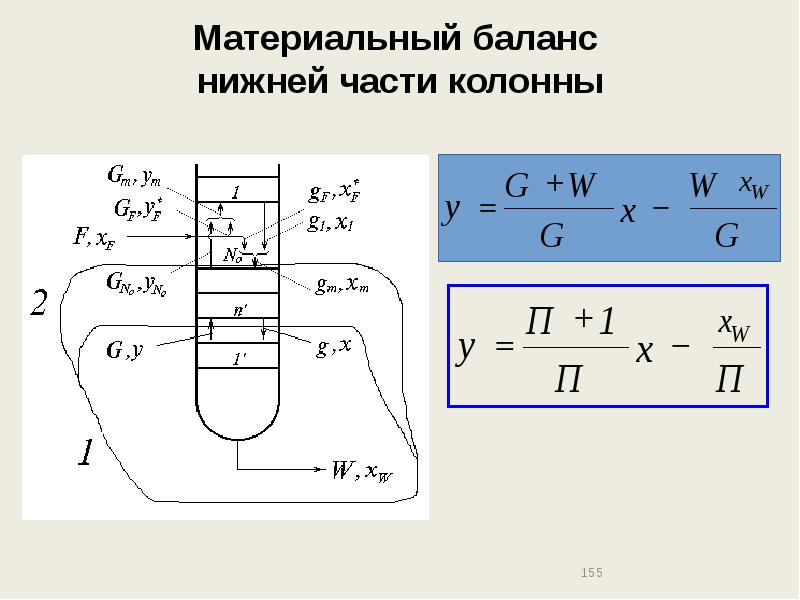
- 154. Материальный баланс нижней части колонны
- 155. Материальный баланс нижней части колонны
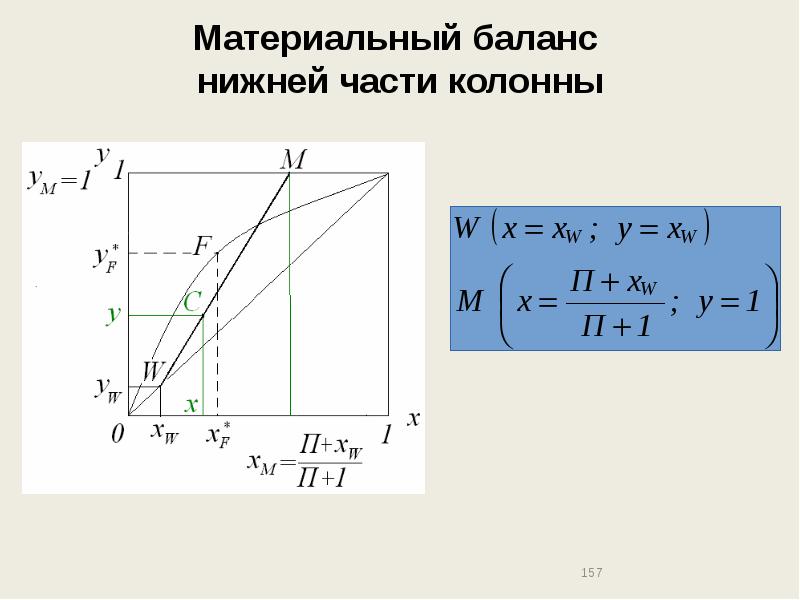
- 156. Материальный баланс нижней части колонны
- 157. Материальный баланс нижней части колонны
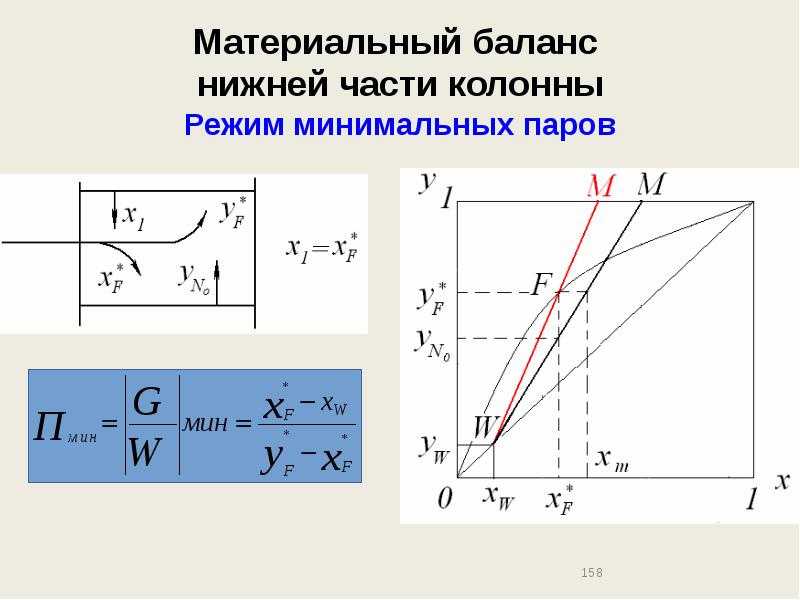
- 158. Материальный баланс нижней части колонны Режим минимальных паров
- 159. Общий вид уравнения рабочей линии для нижней части колонны
- 160. Общий вид уравнения рабочей линии
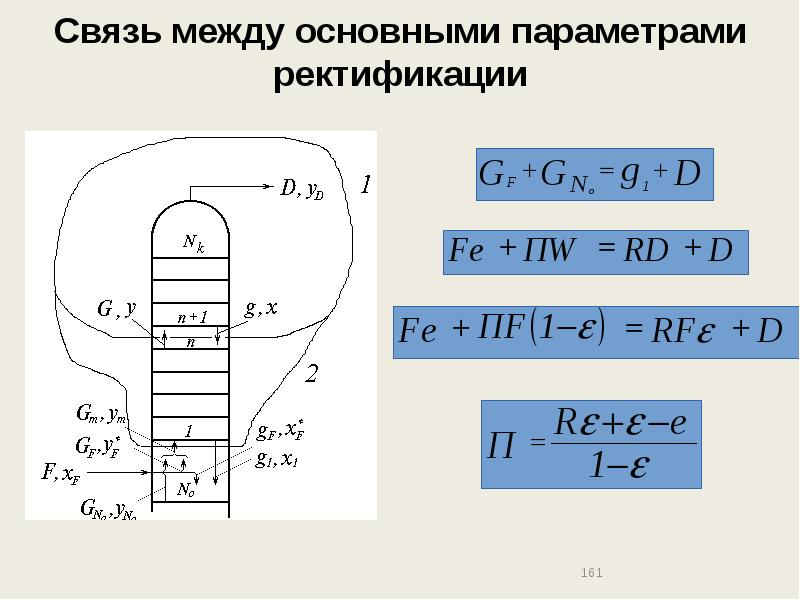
- 161. Связь между основными параметрами ректификации
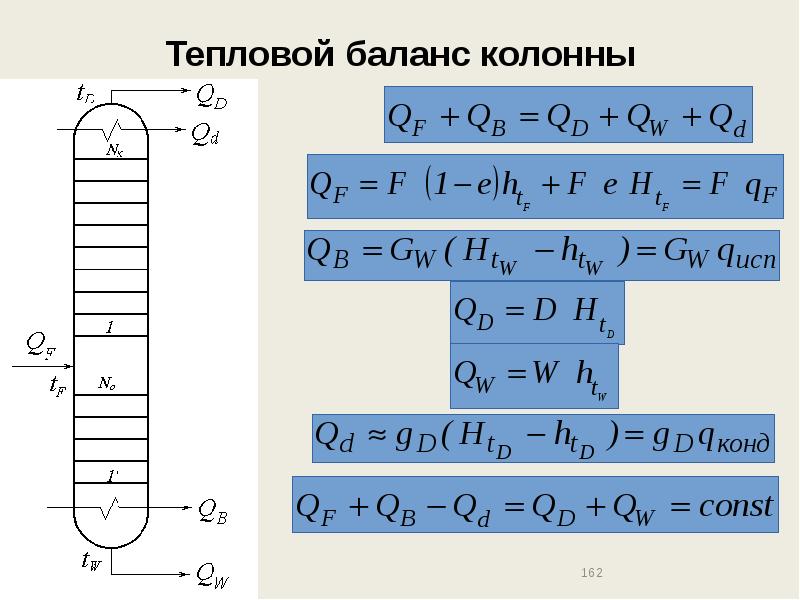
- 162. Тепловой баланс колонны
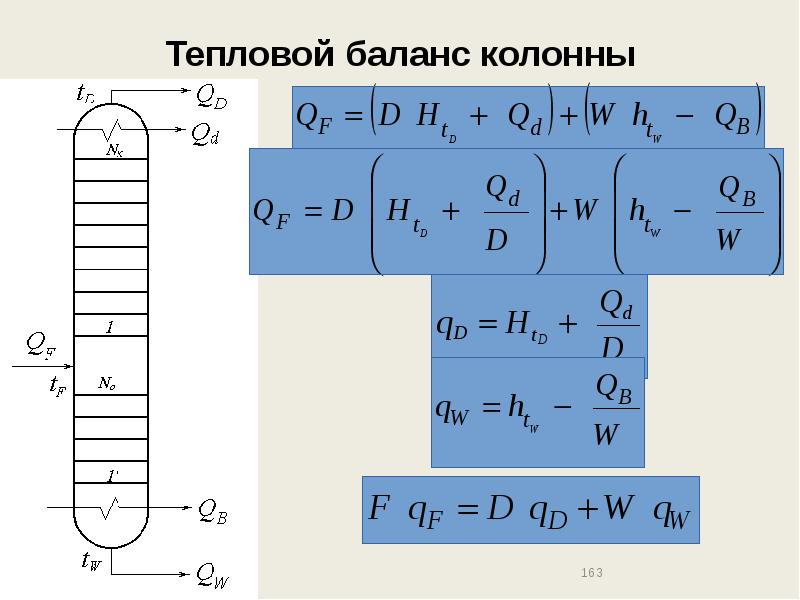
- 163. Тепловой баланс колонны
- 164. Тепловой баланс колонны
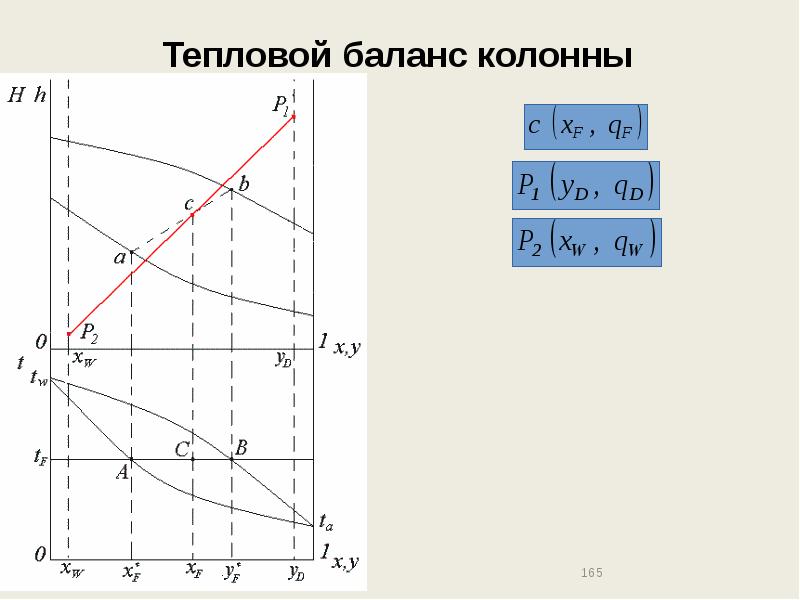
- 165. Тепловой баланс колонны
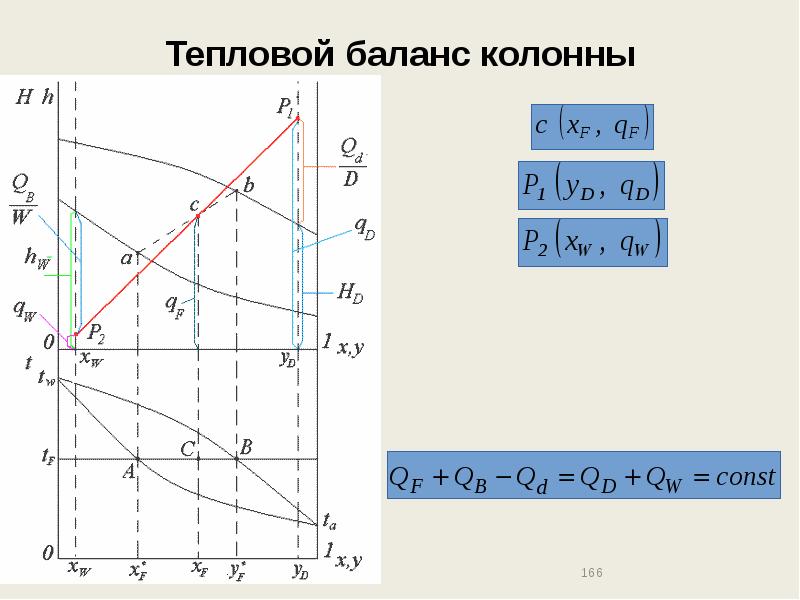
- 166. Тепловой баланс колонны
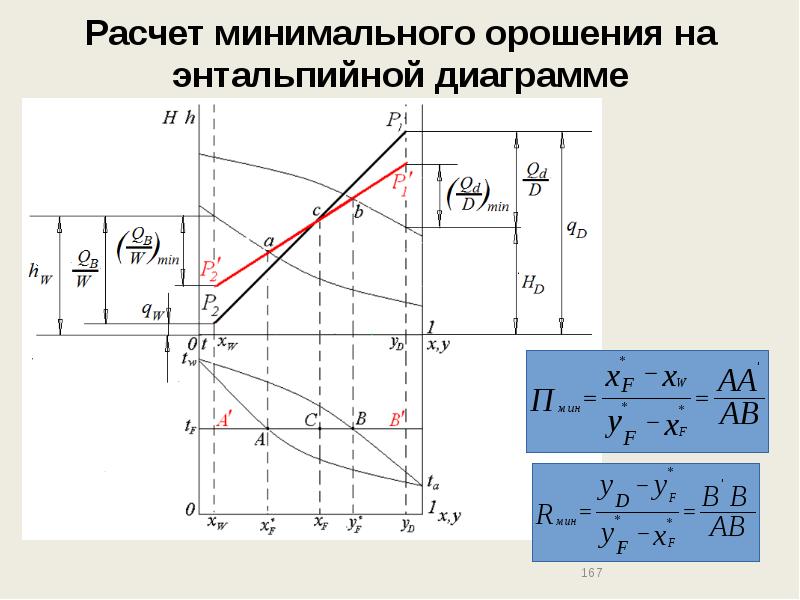
- 167. Расчет минимального орошения на энтальпийной диаграмме
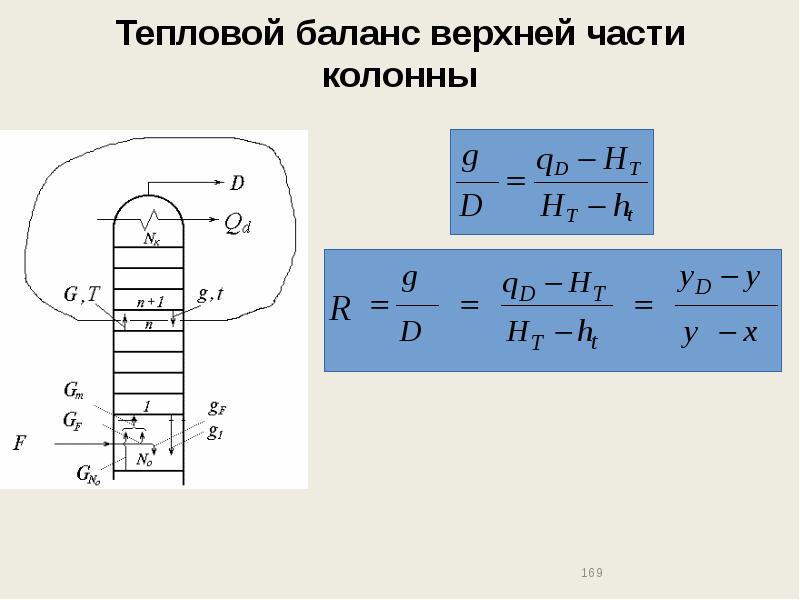
- 168. Тепловой баланс верхней части колонны
- 169. Тепловой баланс верхней части колонны
- 170. Тепловой баланс колонны (продолжение) Лекция 11.
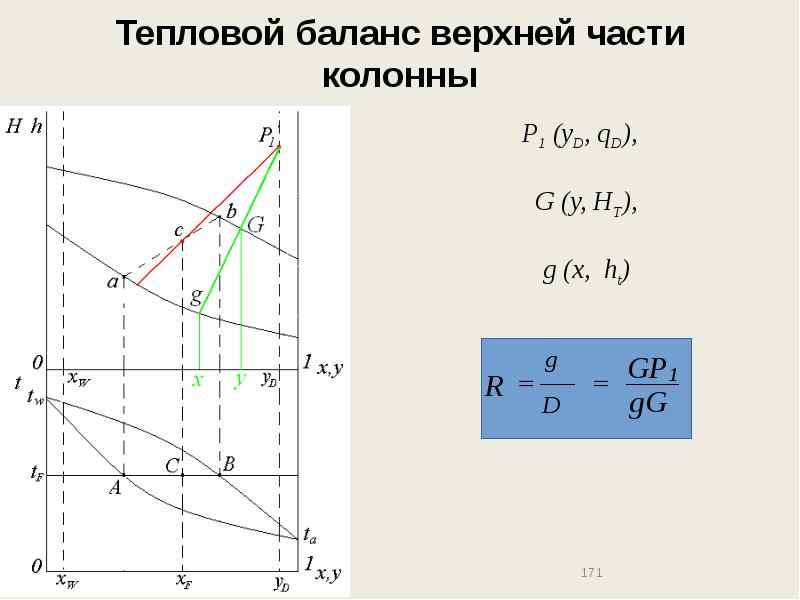
- 171. Тепловой баланс верхней части колонны
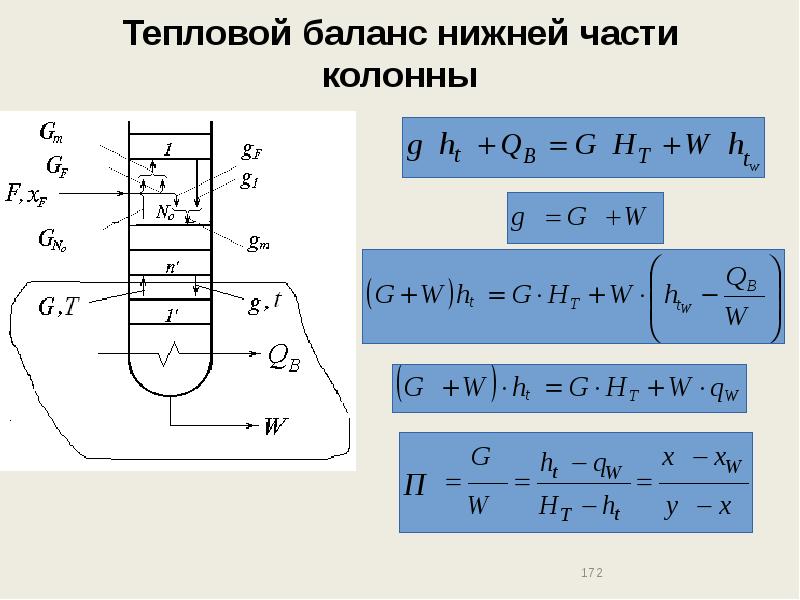
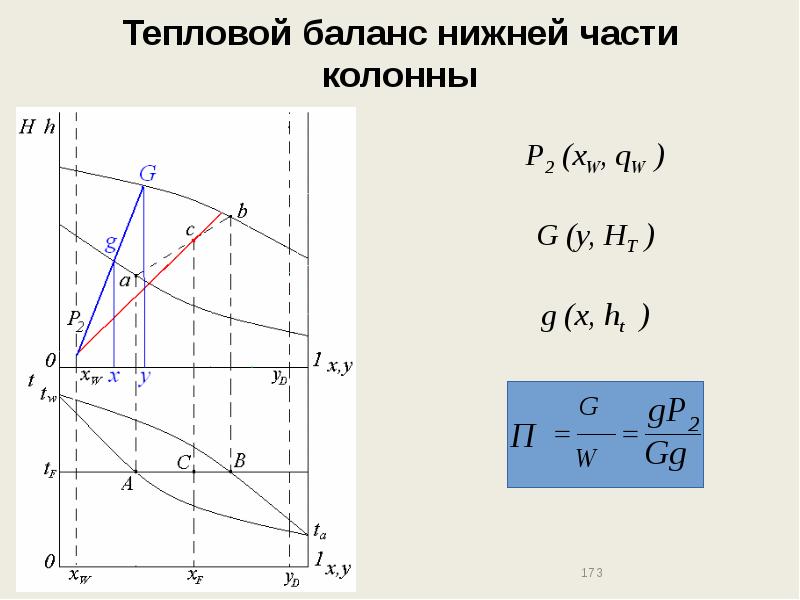
- 172. Тепловой баланс нижней части колонны
- 173. Тепловой баланс нижней части колонны
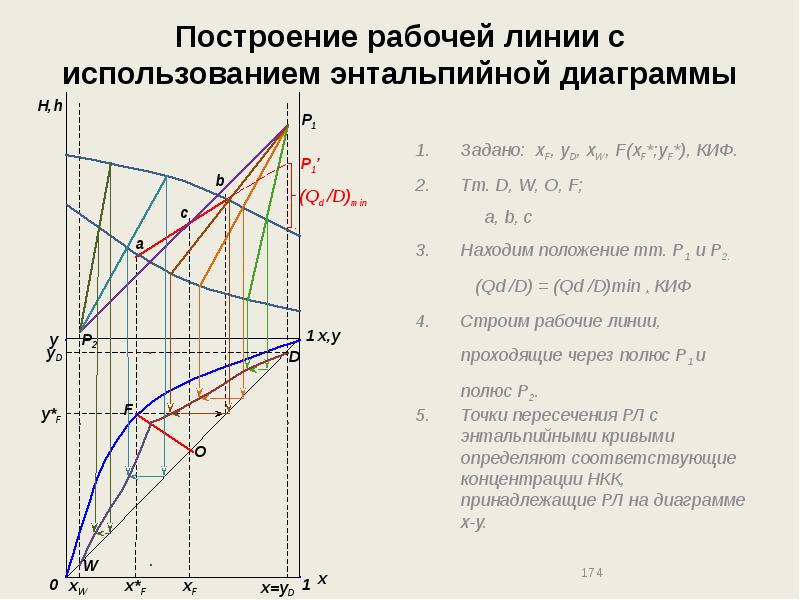
- 174. Построение рабочей линии с использованием энтальпийной диаграммы Задано: xF, yD, xW,
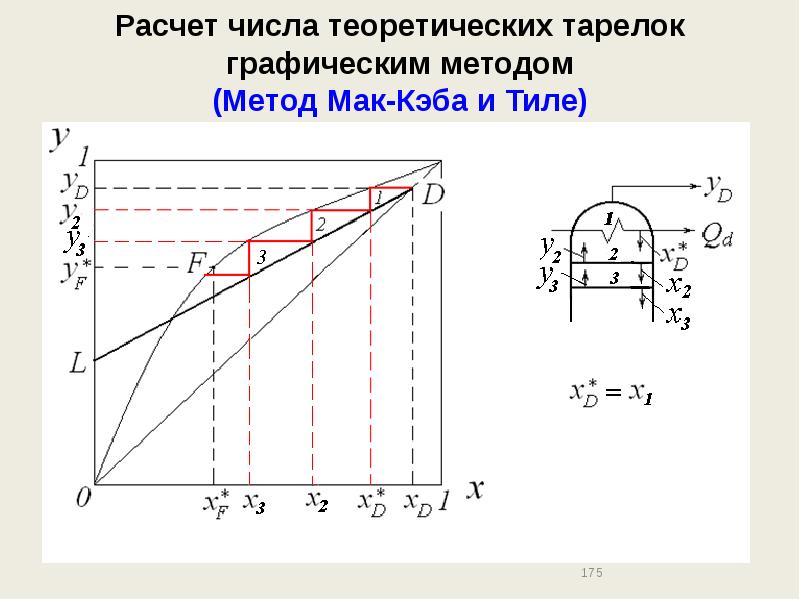
- 175. Расчет числа теоретических тарелок графическим методом (Метод Мак-Кэба и Тиле)
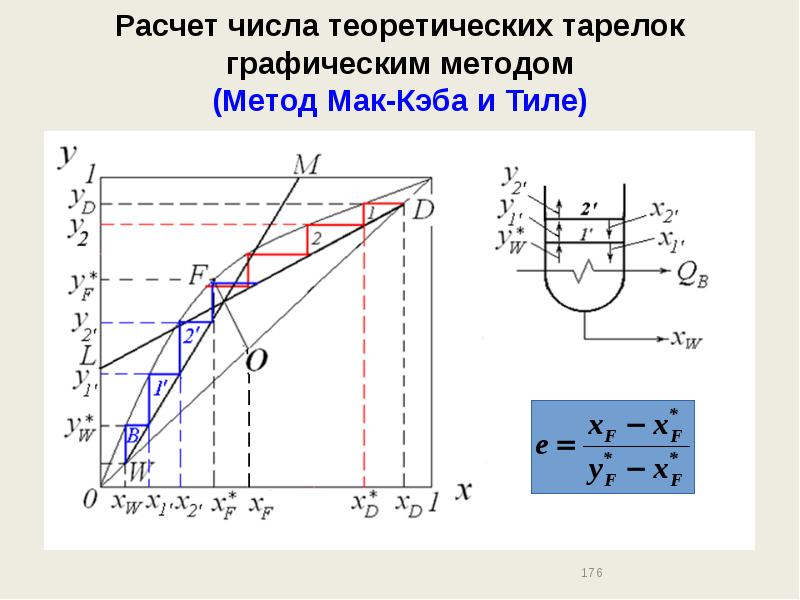
- 176. Расчет числа теоретических тарелок графическим методом (Метод Мак-Кэба и Тиле)
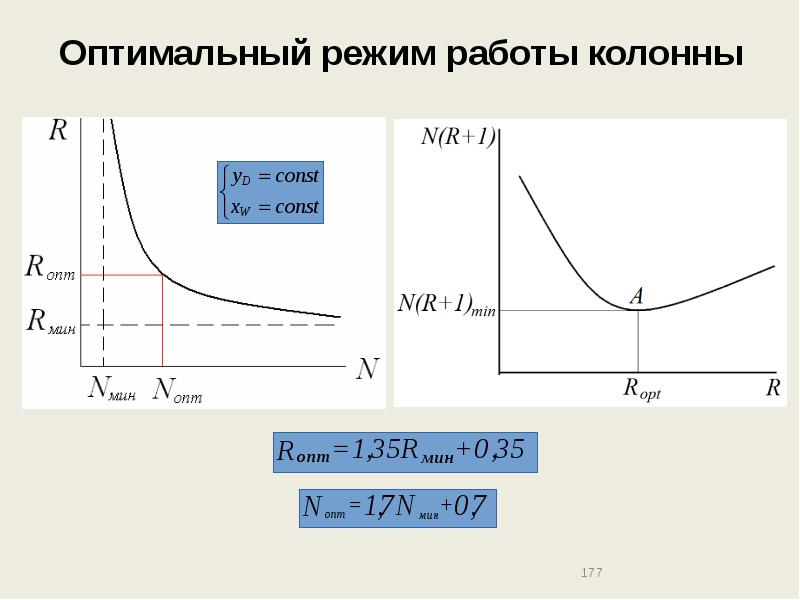
- 177. Оптимальный режим работы колонны
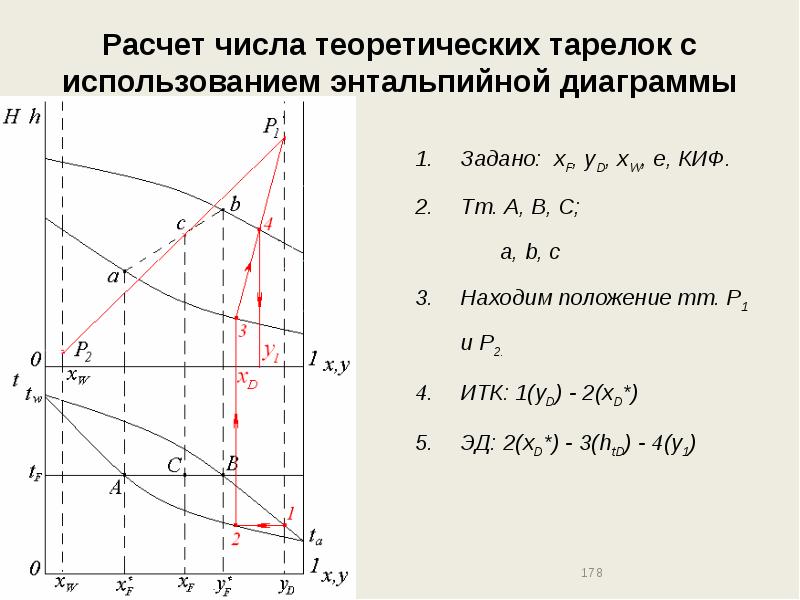
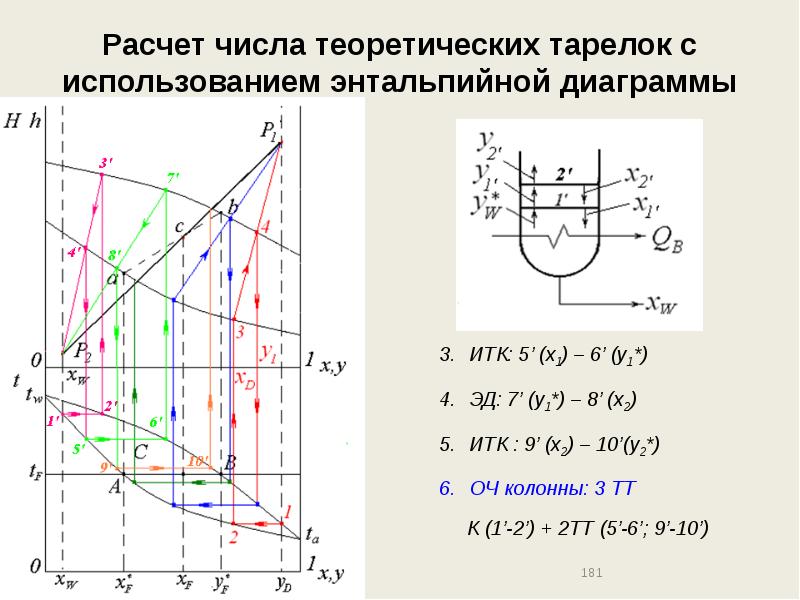
- 178. Расчет числа теоретических тарелок с использованием энтальпийной диаграммы
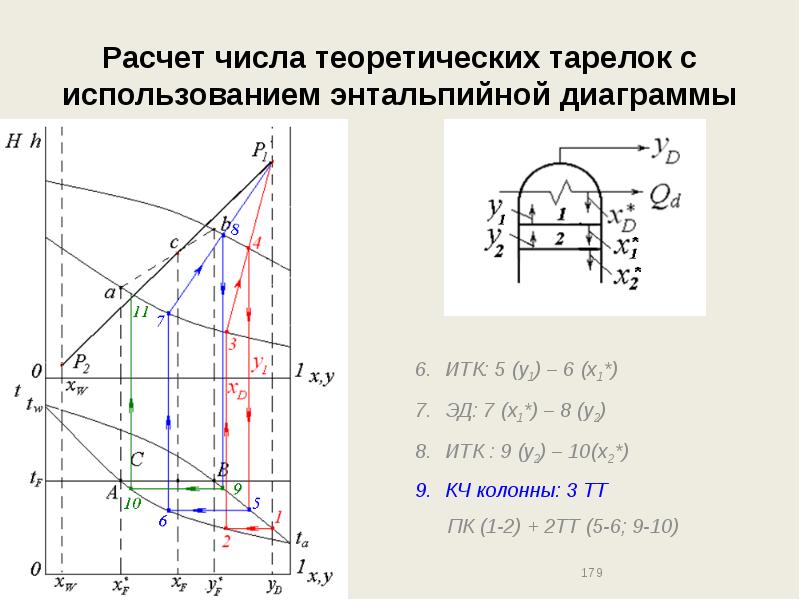
- 179. Расчет числа теоретических тарелок с использованием энтальпийной диаграммы ИТК: 5 (y1)
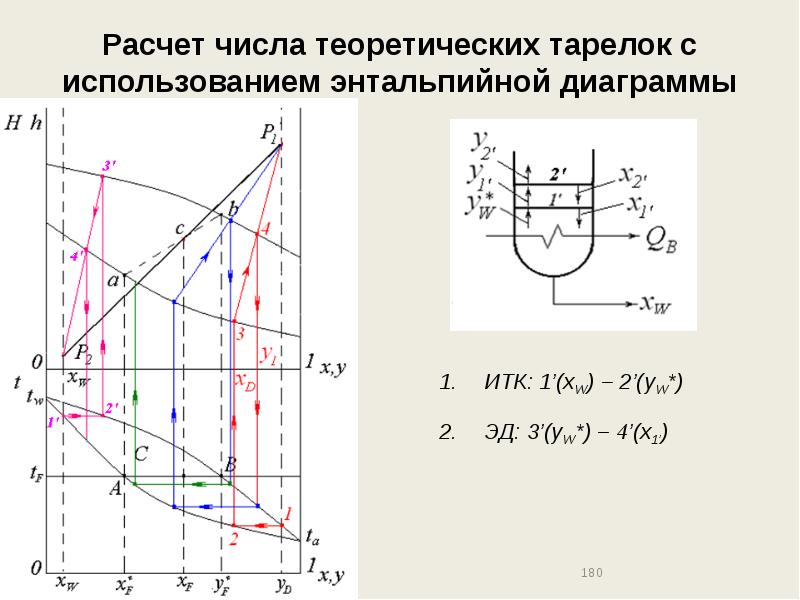
- 180. Расчет числа теоретических тарелок с использованием энтальпийной диаграммы
- 181. Расчет числа теоретических тарелок с использованием энтальпийной диаграммы
- 182. Способы отвода и подвода тепла Лекция 12.
- 183. Расчет температур верха и низа колонны Температура верха
- 184. Расчет температуры ввода сырья в колонну При е 1
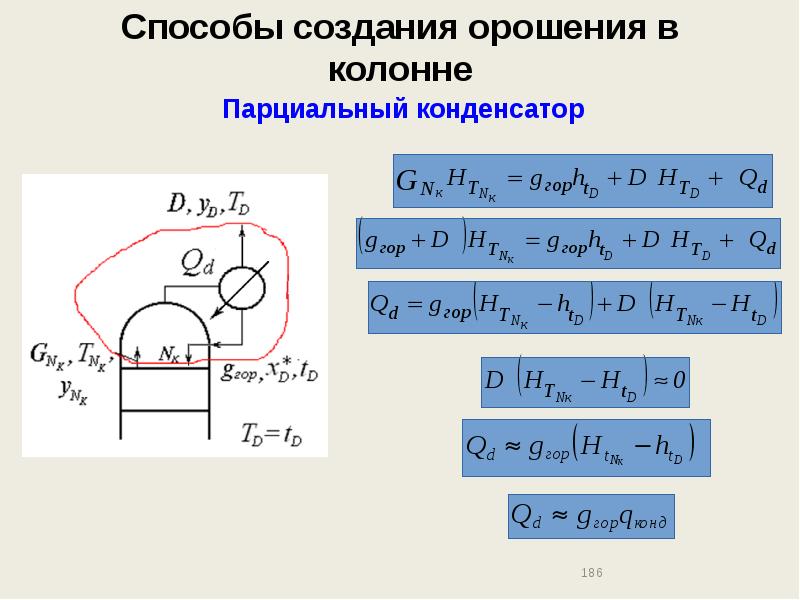
- 185. Способы создания орошения в колонне Парциальный конденсатор Холодное испаряющееся орошение Циркуляционное
- 186. Способы создания орошения в колонне
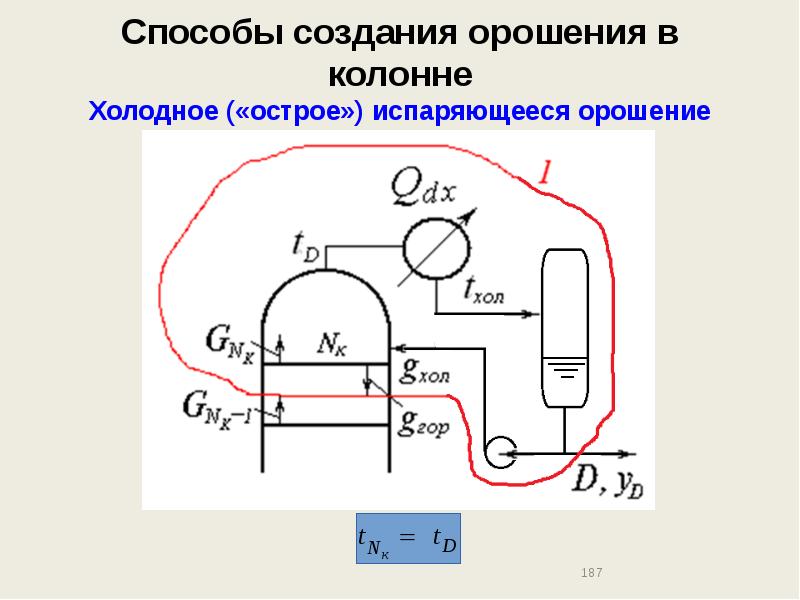
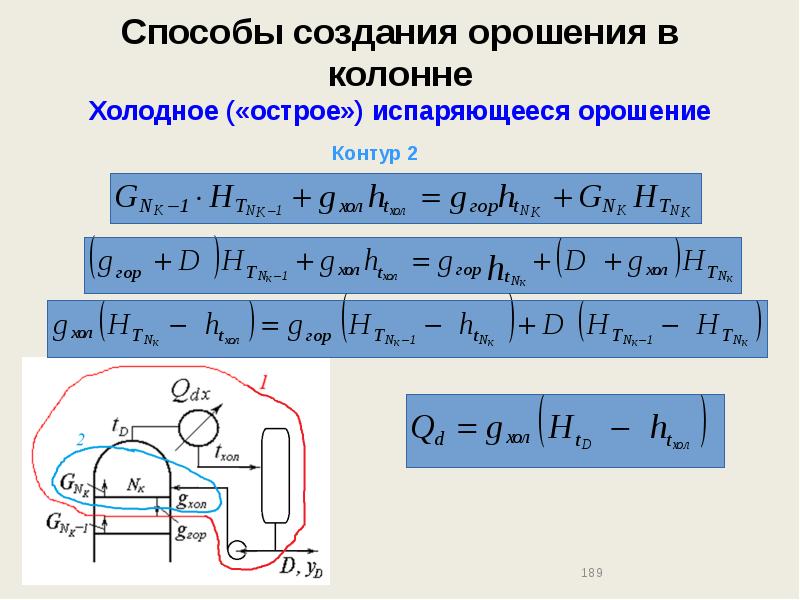
- 187. Способы создания орошения в колонне Холодное («острое») испаряющееся орошение
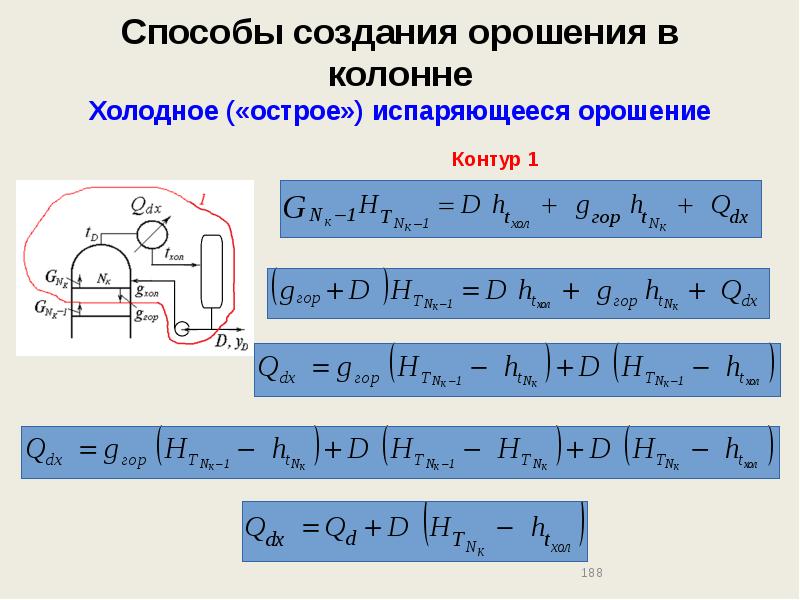
- 188. Способы создания орошения в колонне Холодное («острое») испаряющееся орошение
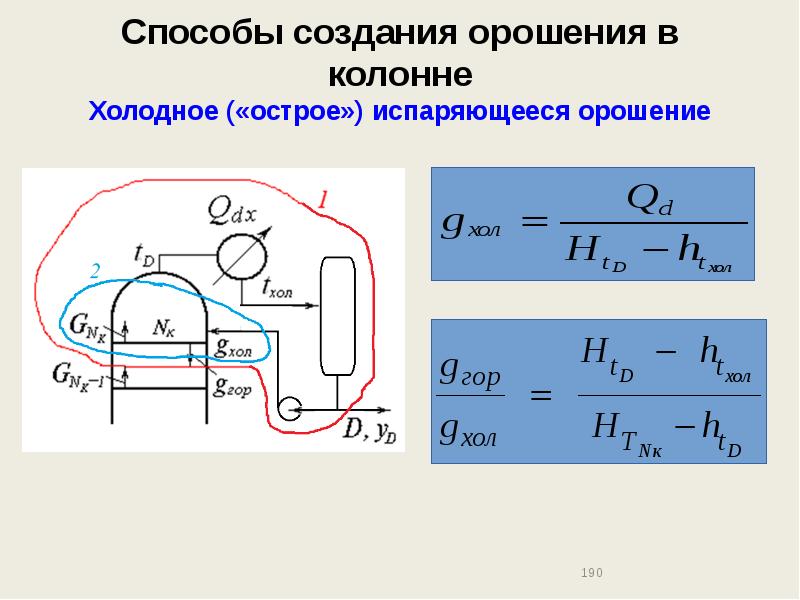
- 189. Способы создания орошения в колонне Холодное («острое») испаряющееся орошение
- 190. Способы создания орошения в колонне Холодное («острое») испаряющееся орошение
- 191. Способы создания орошения в колонне Верхнее циркуляционное неиспаряющееся орошение
- 192. Способы создания орошения в колонне Верхнее циркуляционное неиспаряющееся орошение
- 193. Способы подвода тепла в низ колонны 1. Змеевики или пучки труб,
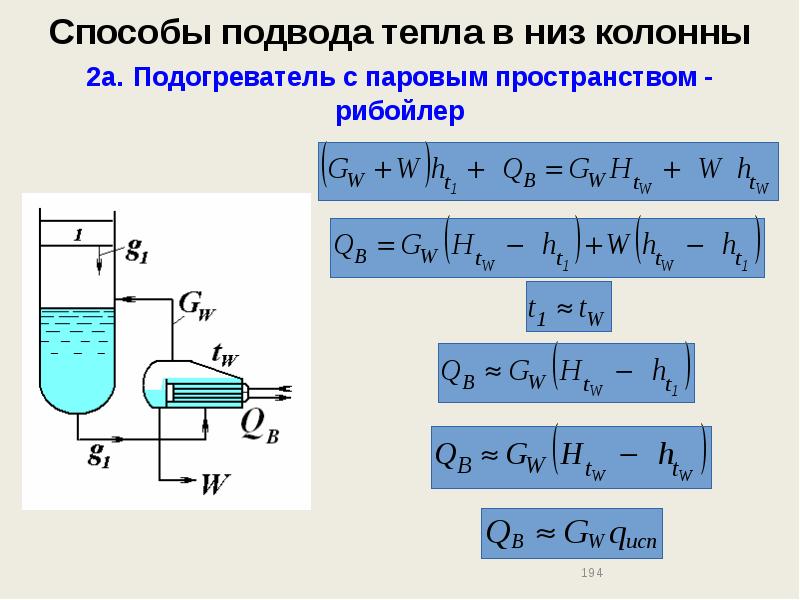
- 194. Способы подвода тепла в низ колонны 2а. Подогреватель с паровым пространством
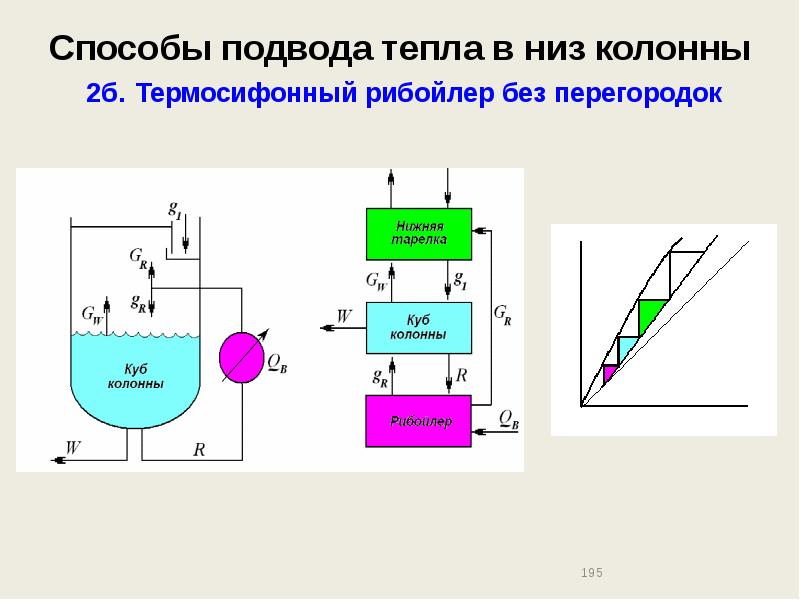
- 195. Способы подвода тепла в низ колонны 2б. Термосифонный рибойлер без перегородок
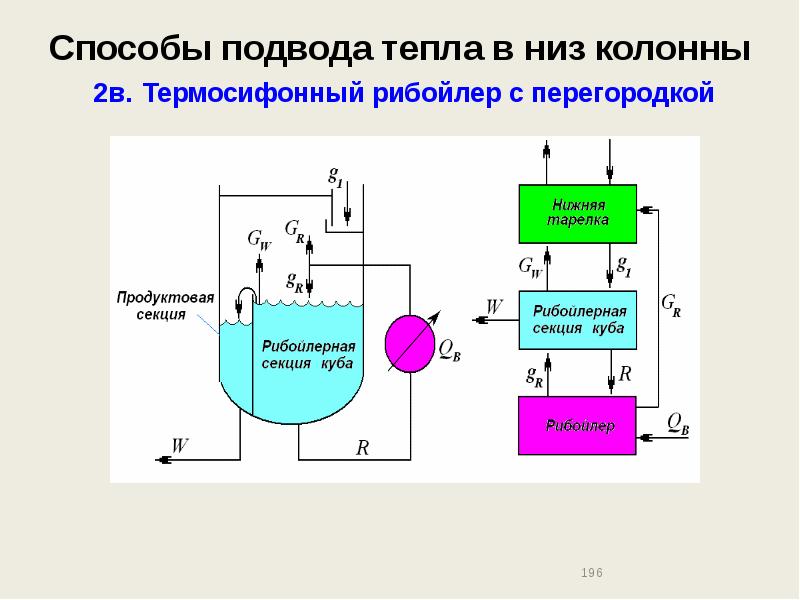
- 196. Способы подвода тепла в низ колонны 2в. Термосифонный рибойлер с перегородкой
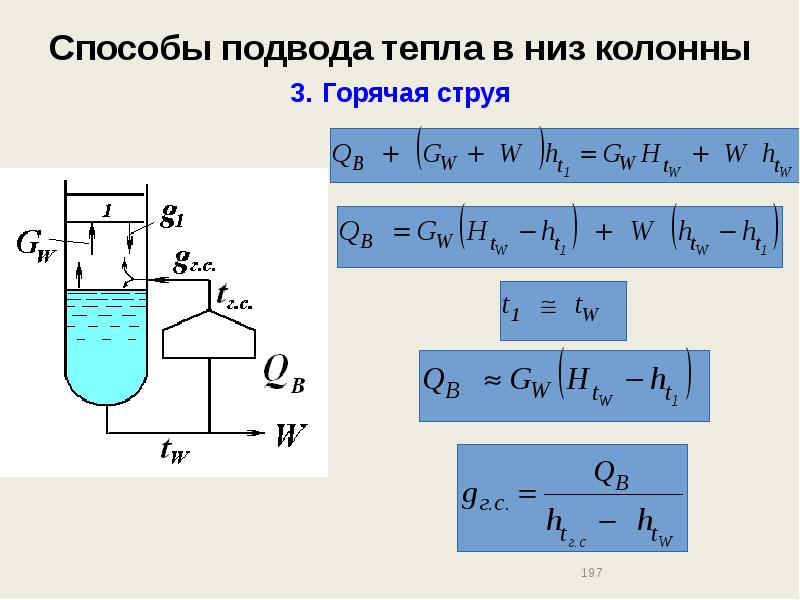
- 197. Способы подвода тепла в низ колонны 3. Горячая струя
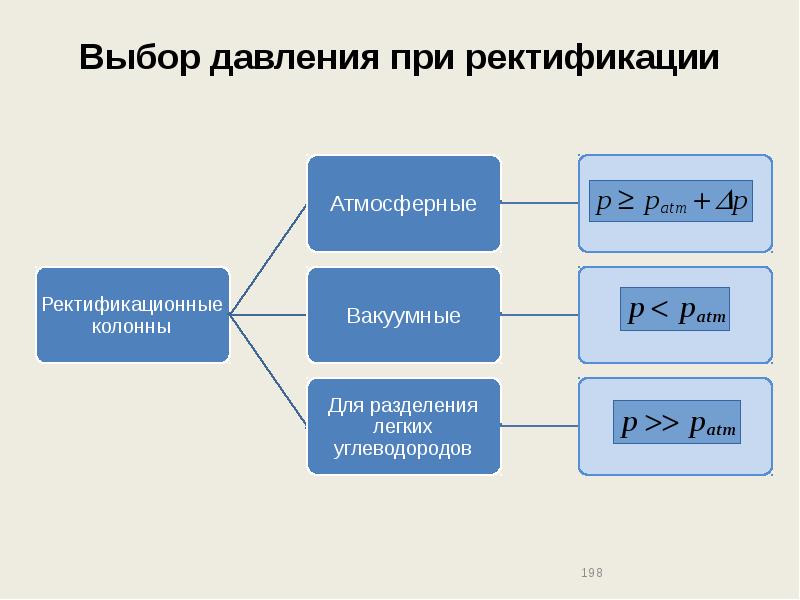
- 198. Выбор давления при ректификации
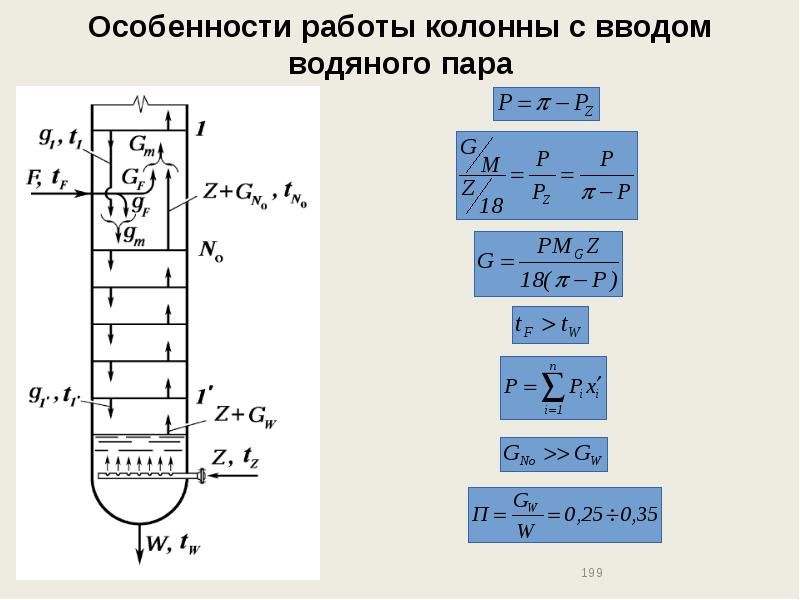
- 199. Особенности работы колонны с вводом водяного пара
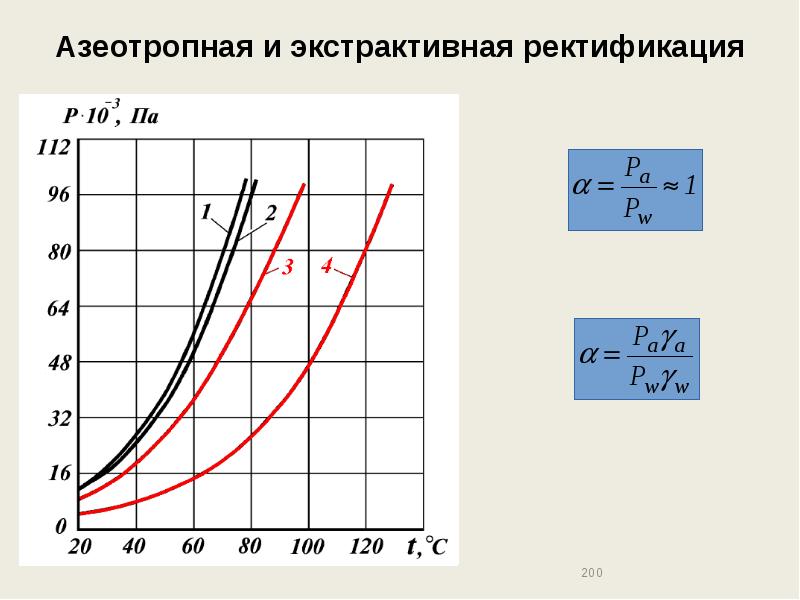
- 200. Азеотропная и экстрактивная ректификация
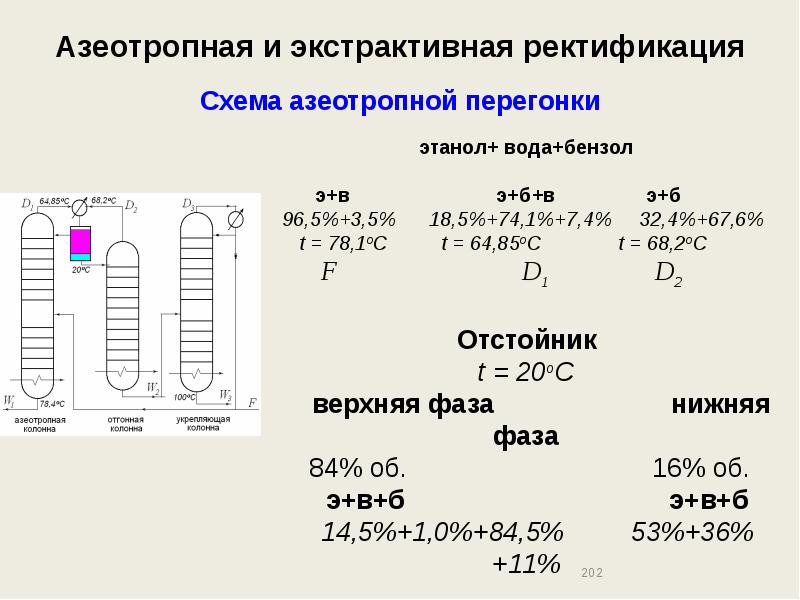
- 201. Азеотропная и экстрактивная ректификация Схема азеотропной перегонки
- 202. Азеотропная и экстрактивная ректификация Схема азеотропной перегонки
- 203. Азеотропная и экстрактивная ректификация Схема азеотропной перегонки
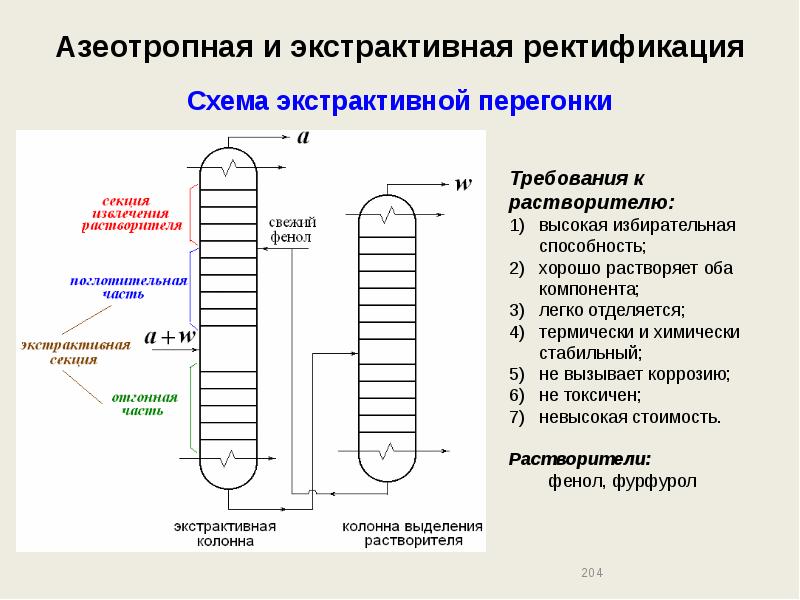
- 204. Азеотропная и экстрактивная ректификация Схема экстрактивной перегонки
- 205. Ректификация многокомпонентных смесей Лекция 15.
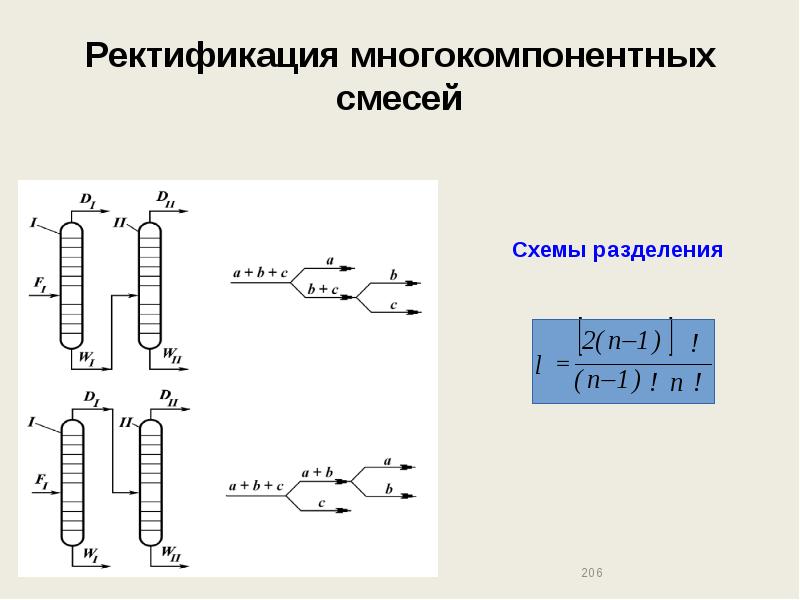
- 206. Ректификация многокомпонентных смесей Схемы разделения
- 207. Ректификация многокомпонентных смесей Особенности расчета
- 208. Ректификация многокомпонентных смесей Расчет процесса однократного испарения
- 209. Ректификация многокомпонентных смесей Расчет процесса однократного испарения
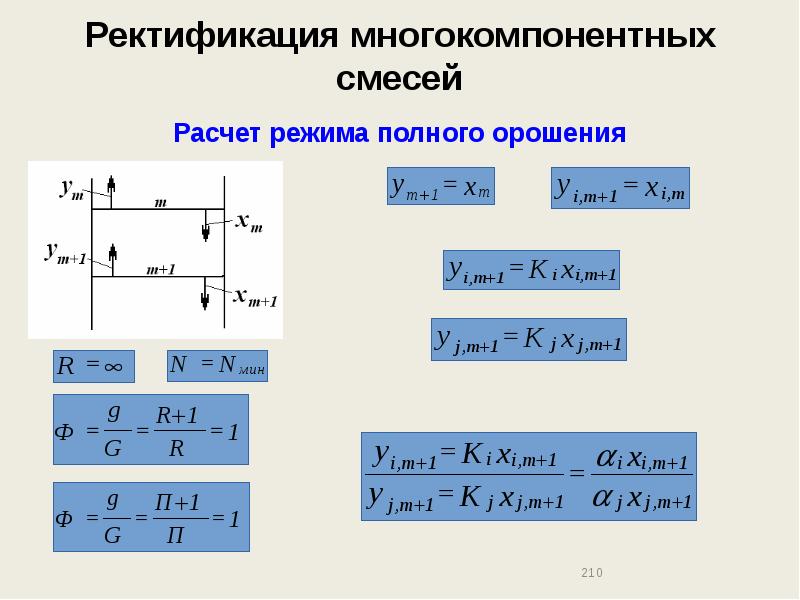
- 210. Ректификация многокомпонентных смесей Расчет режима полного орошения
- 211. Ректификация многокомпонентных смесей Расчет режима полного орошения
- 212. Ректификация многокомпонентных смесей Расчет режима полного орошения
- 213. Ректификация многокомпонентных смесей Расчет режима полного орошения
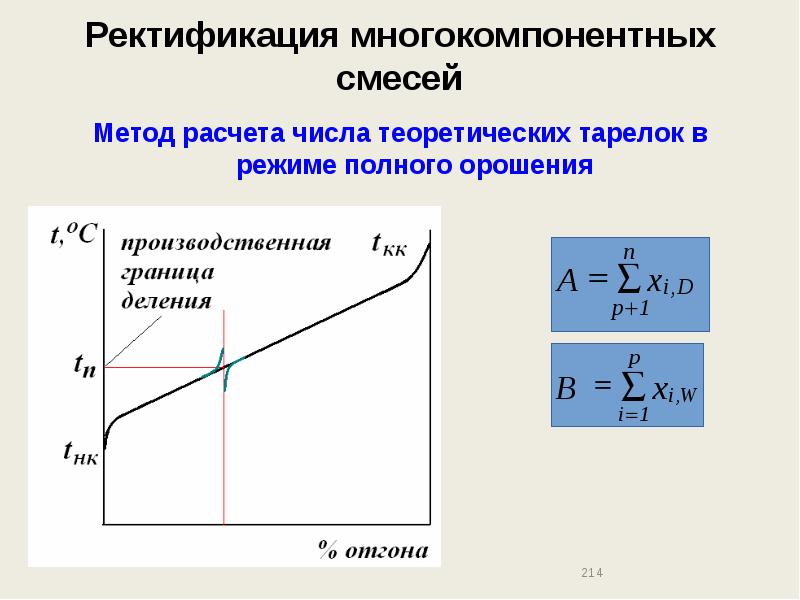
- 214. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
- 215. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
- 216. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
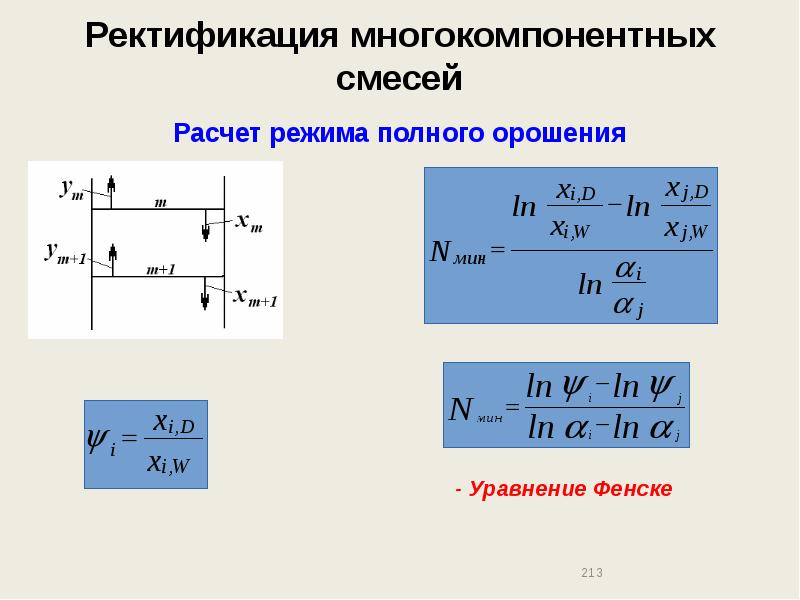
- 217. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
- 218. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
- 219. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
- 220. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
- 221. Ректификация многокомпонентных смесей (продолжение) Лекция 16.
- 222. Ректификация многокомпонентных смесей Метод расчета числа теоретических тарелок в режиме полного
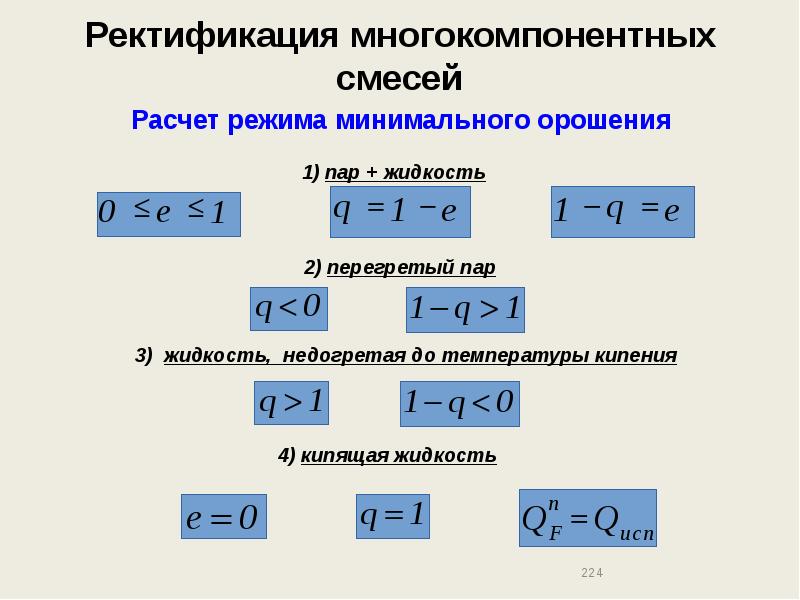
- 223. Ректификация многокомпонентных смесей Расчет режима минимального орошения
- 224. Ректификация многокомпонентных смесей Расчет режима минимального орошения
- 225. Ректификация многокомпонентных смесей Расчет режима минимального орошения
- 226. Ректификация многокомпонентных смесей Расчет минимального флегмового числа и состава дистиллята
- 227. Ректификация многокомпонентных смесей Расчет минимального флегмового числа и состава дистиллята
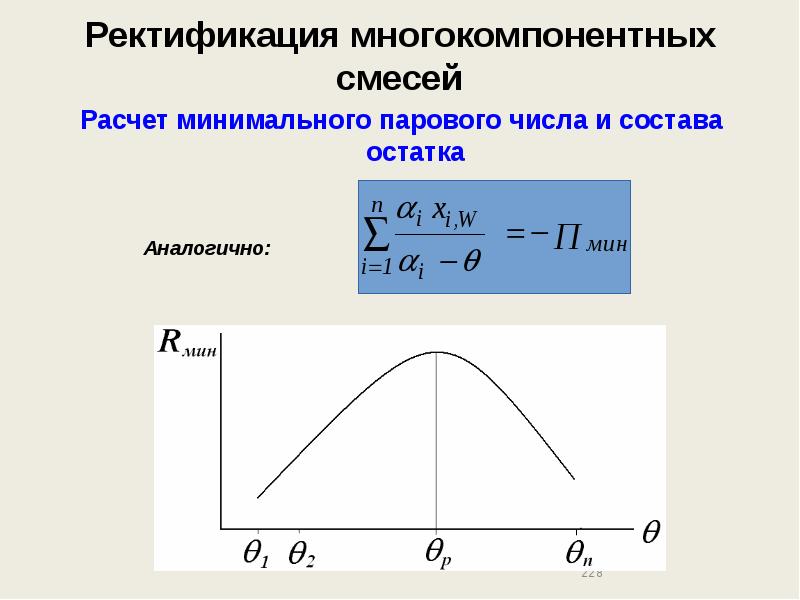
- 228. Ректификация многокомпонентных смесей Расчет минимального парового числа и состава остатка
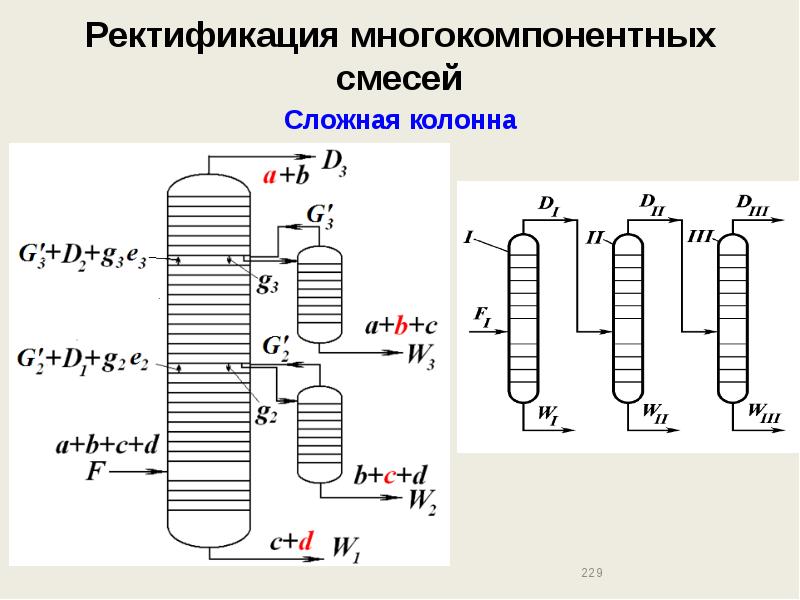
- 229. Ректификация многокомпонентных смесей Сложная колонна
- 230. Ректификация многокомпонентных смесей Сложная колонна
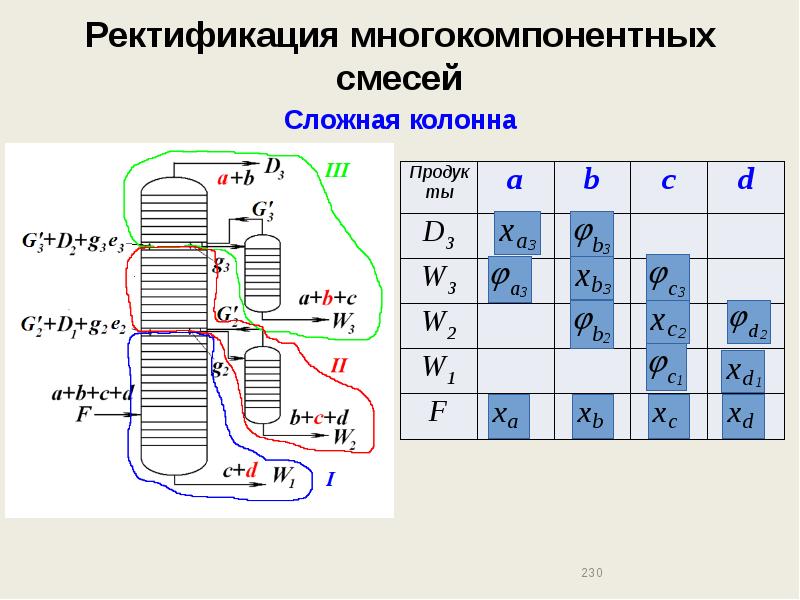
- 231. Ректификация многокомпонентных смесей Сложная колонна
- 232. Ректификация многокомпонентных смесей Сложная колонна
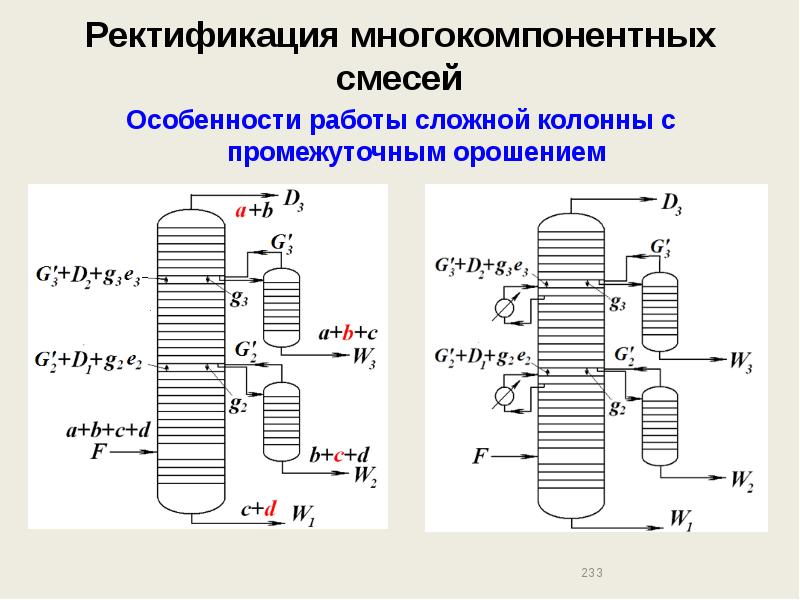
- 233. Ректификация многокомпонентных смесей Особенности работы сложной колонны с промежуточным орошением
- 234. Ректификация многокомпонентных смесей Особенности работы сложной колонны с промежуточным орошением
- 235. Скачать презентацию






























































































































Слайды и текст этой презентации
Скачать презентацию на тему Процессы и аппараты нефтегазопереработки и нефтехимии можно ниже:
Похожие презентации





























