Строение атома пз и пс Д.И. Менделеева в свете квантовомеханической теории строения атома презентация
Содержание
- 2. Ученые древности о строении вещества Древнегреческий ученый Демокрит 2500 лет назад
- 3. Атом
- 6. Модель атома Томсона Внутри положительно заряженного шара диаметром около 10 м
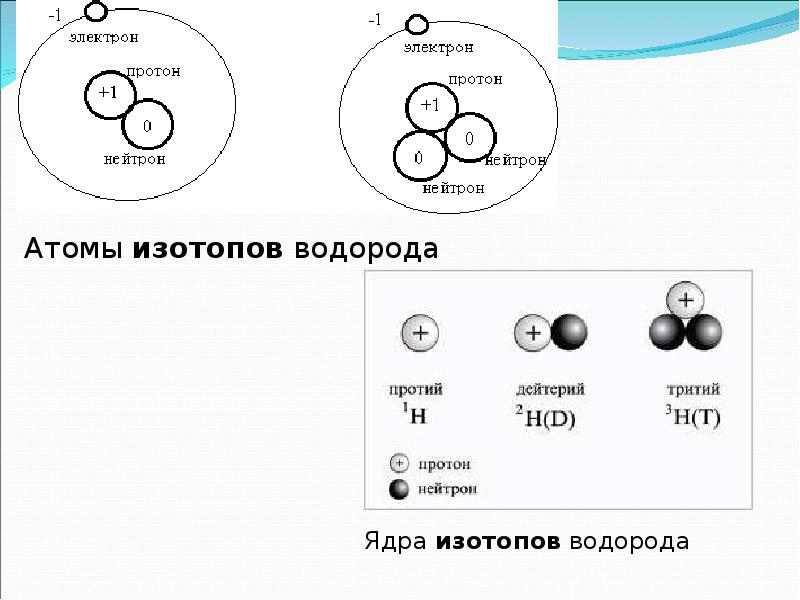
- 11. Изотопы. Так называются атомы, имеющие одинаковый заряд ядра , но различную
- 12. Атомы изотопов водорода Атомы изотопов водорода
- 30. Атом хлора +17 Cl )2 )8 )7 схема строения атома. 1s2
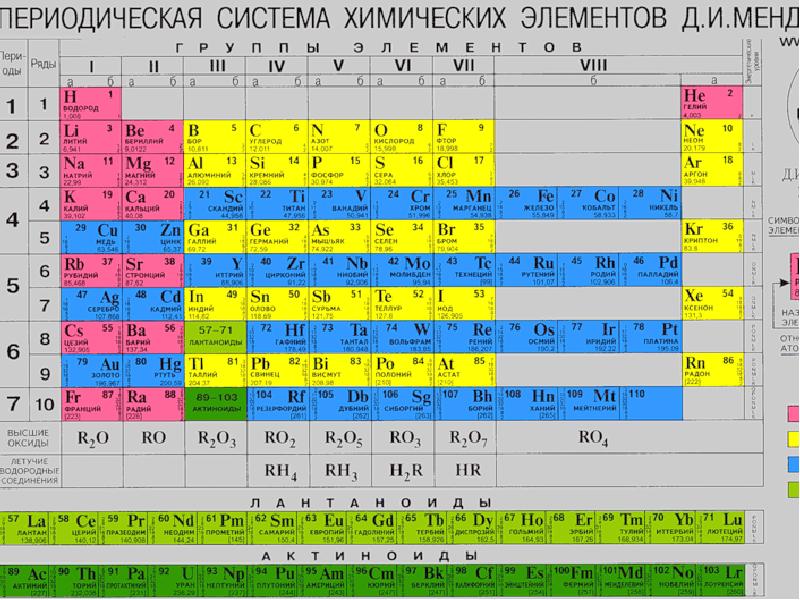
- 33. Первым вариантом системы элементов, предложенным Д. И. Менделеевым 1 марта 1869
- 48. СПАСИБО СПАСИБО за ВНИМАНИЕ!
- 49. Скачать презентацию



































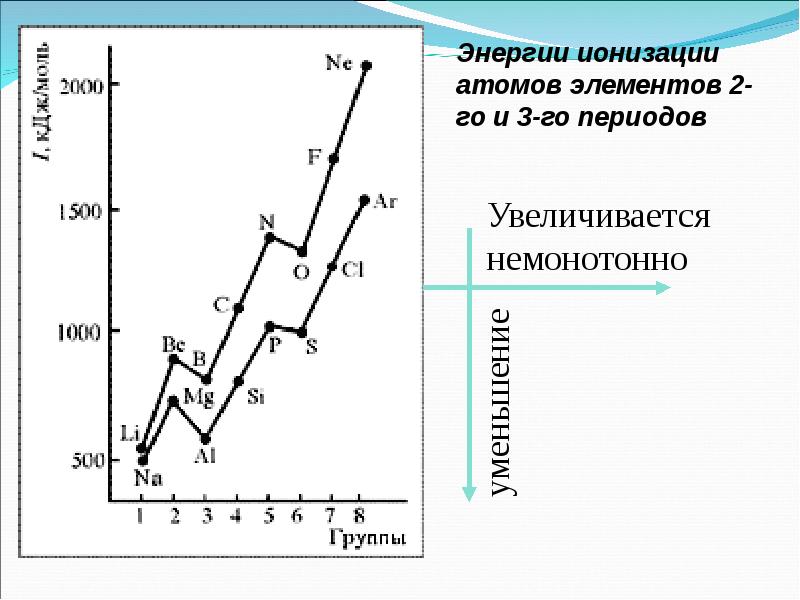
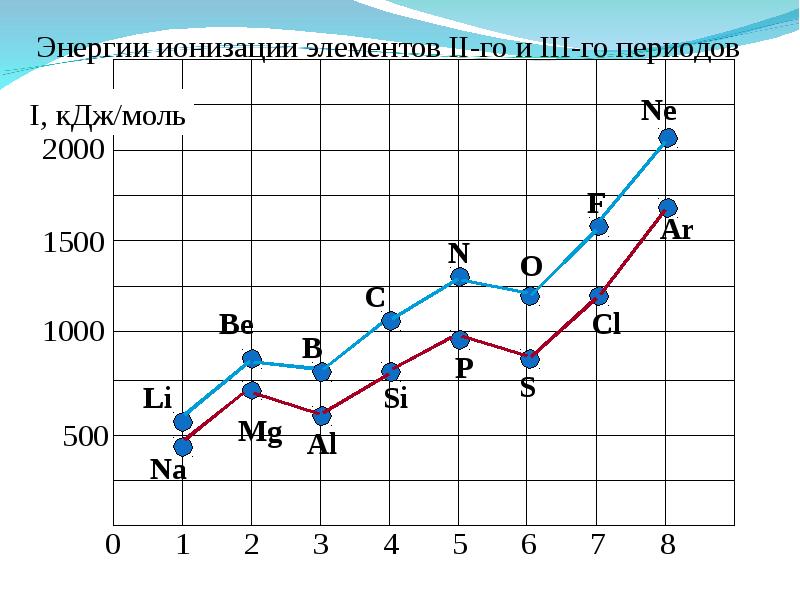


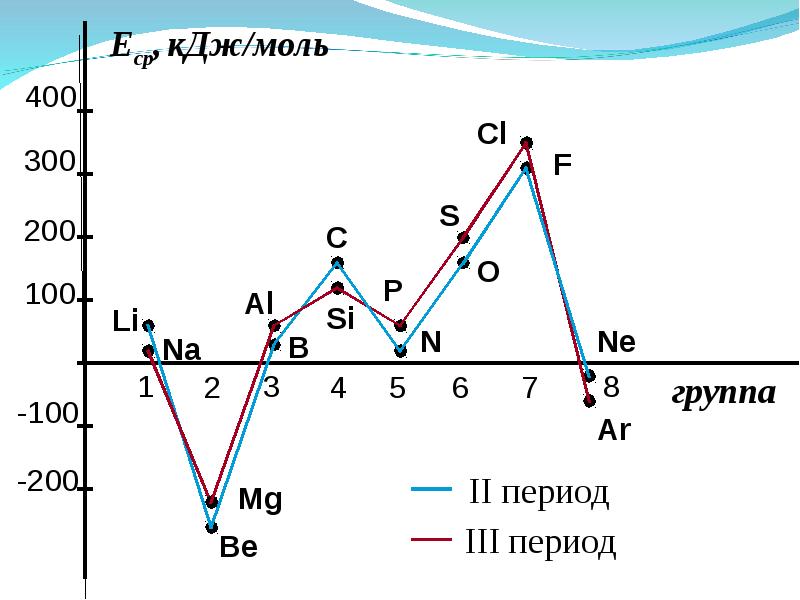


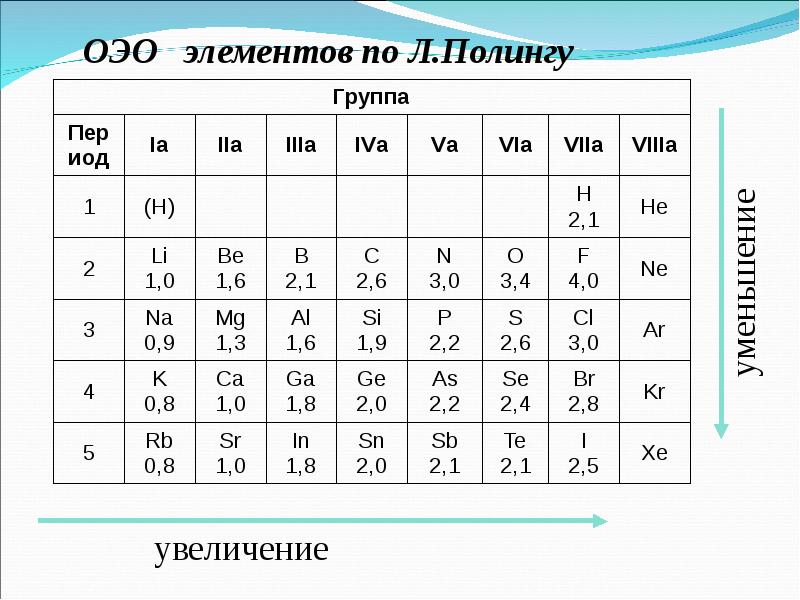

Слайды и текст этой презентации
Скачать презентацию на тему Строение атома пз и пс Д.И. Менделеева в свете квантовомеханической теории строения атома можно ниже:
Похожие презентации





























