Теплота згоряння. Температура горіння презентация
Содержание
- 2. План лекції 1. Тепловий ефект хімічної реакції. 2. Теплота згоряння.
- 3. 1. ТЕПЛОВИЙ ЕФЕКТ ХІМІЧНОЇ РЕАКЦІЇ Тепловий ефект реакції - кількість теплоти,
- 4. Якщо Eкін <Eпоч, то Q > 0, реакція супроводжу-ється виділенням тепла
- 5. Стандартна теплота реакції - різниця між стандартними теплотами утворення продуктів реакції
- 6. 2. ТЕПЛОТА ЗГОРЯННЯ Теплота згоряння - кількість тепла, що виділяється під
- 7. 2.1. Види теплоти згоряння 2.1. Види теплоти згоряння Залежно від того,
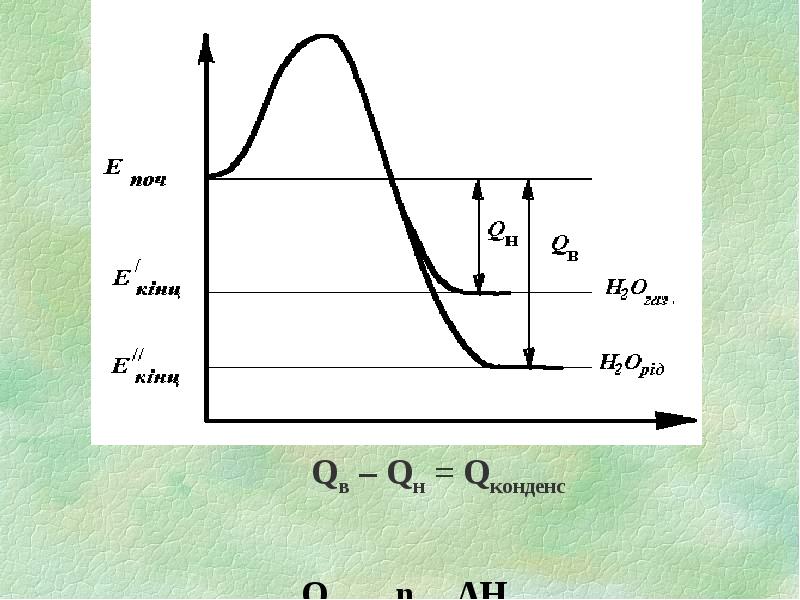
- 8. Залежно від агрегатного стану Н2О, яка утворилася під час горіння і
- 10. При урахуванні хімічного недопалу, вологості матеріалу, втрати на теплове випромінювання, визначають
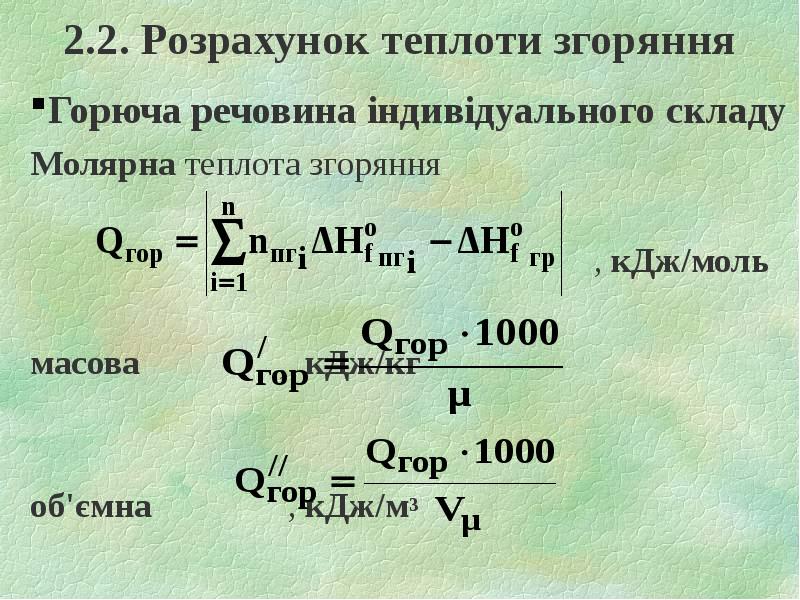
- 11. 2.2. Розрахунок теплоти згоряння Горюча речовина індивідуального складу Молярна теплота згоряння
- 12. Горючі матеріали складного хімічного складу Горючі матеріали складного хімічного складу суміш
- 13. Внесок кожного елементу в масову теплоту згоряння: Внесок кожного елементу в
- 14. ФОРМУЛА МЕНДЄЛЄЄВА Враховує наявність в ГР оксигену, нітрогену та вологи. Вища
- 15. ПРАКТИЧНЕ ЗНАЧЕННЯ ТЕПЛОТИ ЗГОРЯННЯ 1) Використовують для розрахунку пожежної навантаги, що
- 16. 2) Використовують для визначення горючості речовини. 2) Використовують для визначення
- 17. 3. ПОНЯТТЯ ТА ВИДИ ТЕМПЕРАТУРИ ГОРІННЯ РЕЧОВИН Температура горіння - температура,
- 18. Калориметрична температура горіння - температура, до якої нагріваються ПГ, якщо виконуються
- 19. Через відсутність тепловтрат і недопалу вважаємо, що все тепло, що виділилося
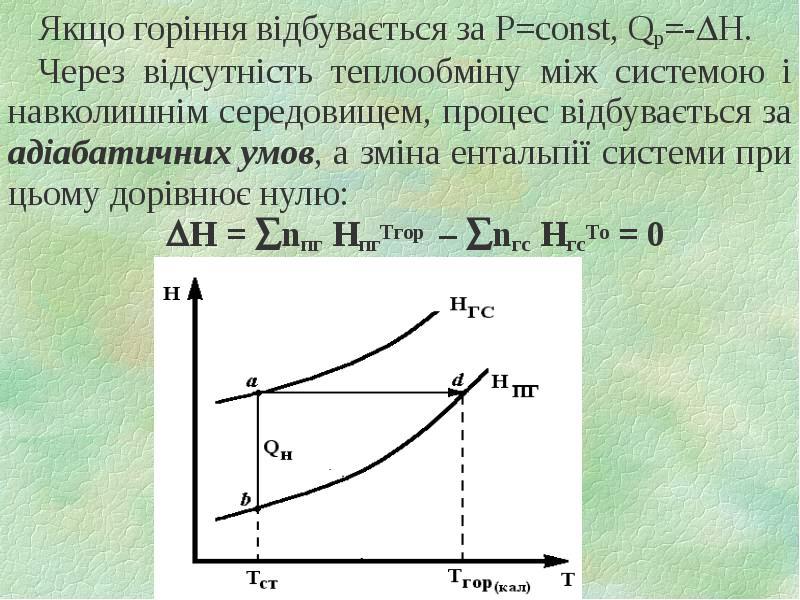
- 20. Якщо горіння відбувається за P=const, Qр=-H. Якщо горіння відбувається за
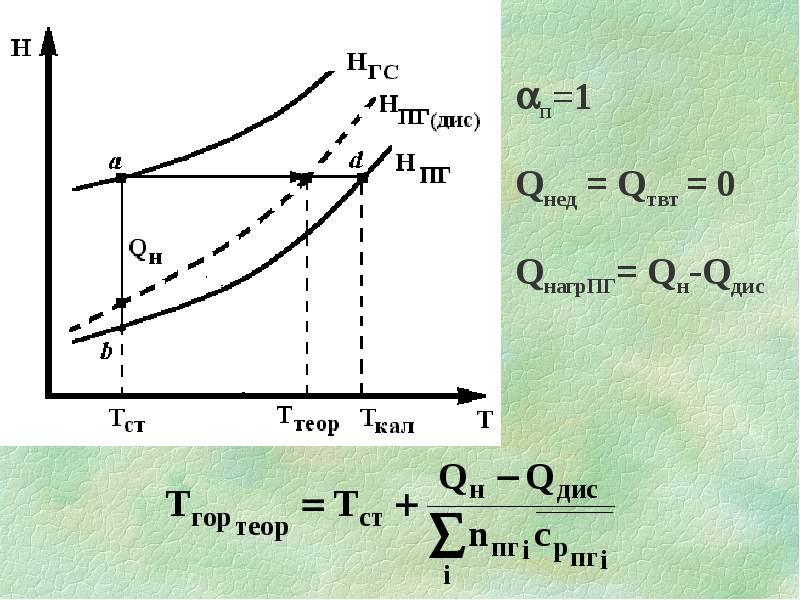
- 21. Якщо Тгор достатньо висока, то ПГ можуть дисоціювати з витратою значної
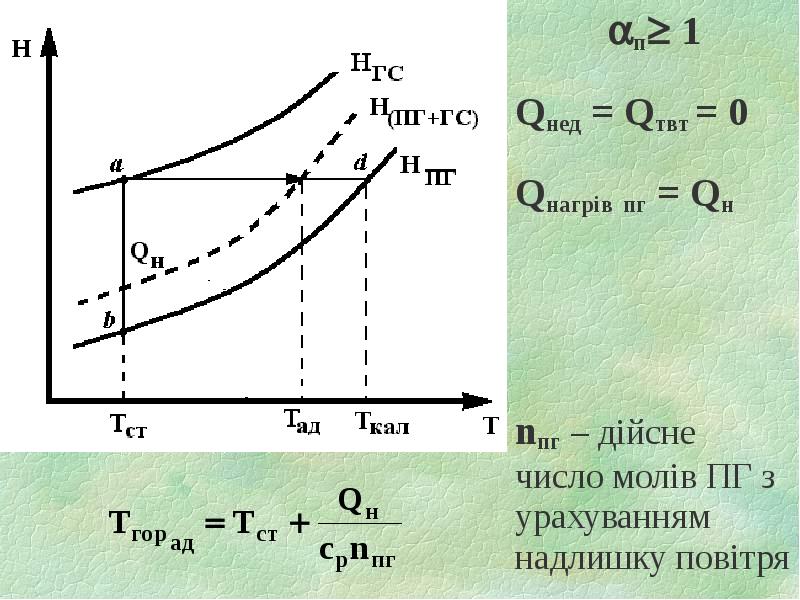
- 23. Адіабатична температура горіння - температура, до якої нагріваються продукти горіння за
- 24. п 1 п 1 Qнед = Qтвт = 0 Qнагрів пг
- 25. Дійсна температура горіння – температура, до якої нагріваються продукти горіння за
- 26. де Qнедоп - кількість тепла, яка не реалізується в зоні горіння
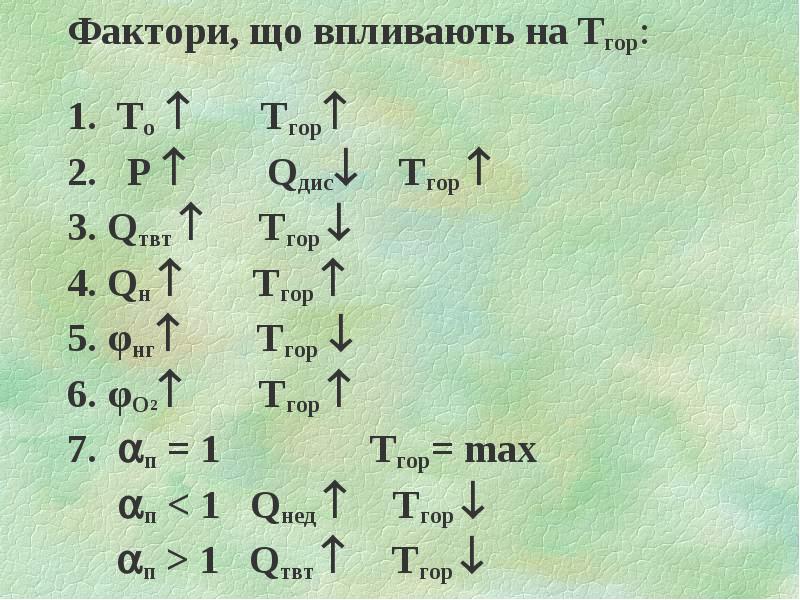
- 27. Фактори, що впливають на Тгор: Фактори, що впливають на Тгор: 1.
- 28. Завдання на самопідготовку 1. Вивчити матеріал Демидов, Шандыба, Щеглов, Горение и
- 29. Скачать презентацию










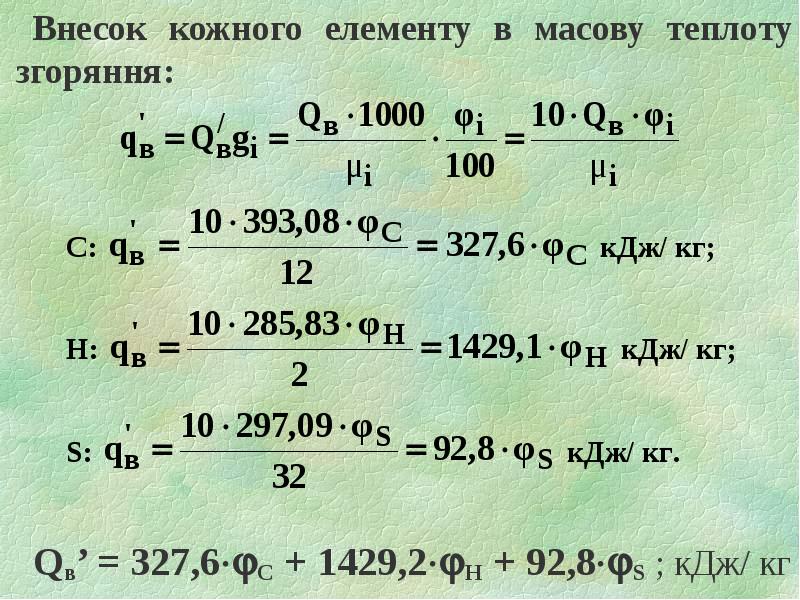











Слайды и текст этой презентации
Скачать презентацию на тему Теплота згоряння. Температура горіння можно ниже:
Похожие презентации





























