Устойчивость и коагуляция коллоидных растворов презентация
Содержание
- 2. План лекции Устойчивость коллоидных растворов, ее виды Коагуляция коллоидных растворов электролитами
- 3. Гидрофобные коллоидные растворы Обладают большой удельной поверхностью раздела между дисперсной фазой
- 4. Кинетическая устойчивость Способность дисперсных частиц удерживаться во взвешенном состоянии под влиянием
- 5. Агрегативная устойчивость Способность частиц дисперсной фазы поддерживать определенную степень дисперсности (препятствовать
- 6. Теория устойчивости и коагуляции гидрофобных золей (Дерягин и Ландау) Силы межмолекулярного
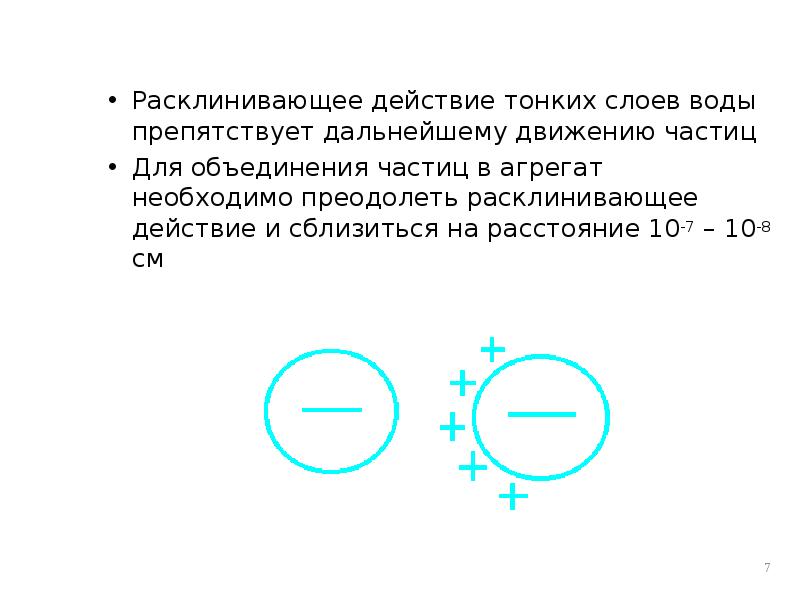
- 7. Расклинивающее действие тонких слоев воды препятствует дальнейшему движению частиц Расклинивающее действие
- 8. Коагуляция Процесс объединения частиц в более крупные агрегаты Скорость коагуляции тем
- 9. Факторы влияющие на скорость коагуляции Температура Концентрация золя Электрический ток
- 10. Коагуляция золей электролитами Коагулирующим действием в электролите обладают те ионы, которые
- 11. Правило значности Шульце-Гарди Коагулирующая сила иона тем больше, чем больше
- 12. Коагулирующая способность ионов зависит От способности ионов адсорбироваться на коллоидных частицах
- 13. Механизм коагулирующего действия ионов Сжатие диффузного слоя противоионов Избирательная адсорбция ионов
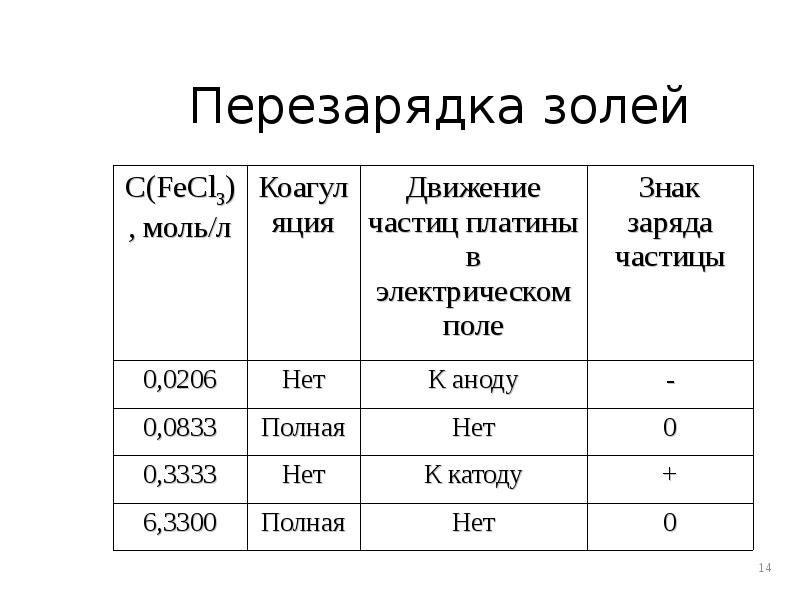
- 14. Перезарядка золей
- 15. Перезарядка наблюдается при добавлении, как правило, многозарядных ионов. Они обладают большой
- 16. Кинетика коагуляции Скрытая коагуляция – при увеличении концентрации электролита начинается образование
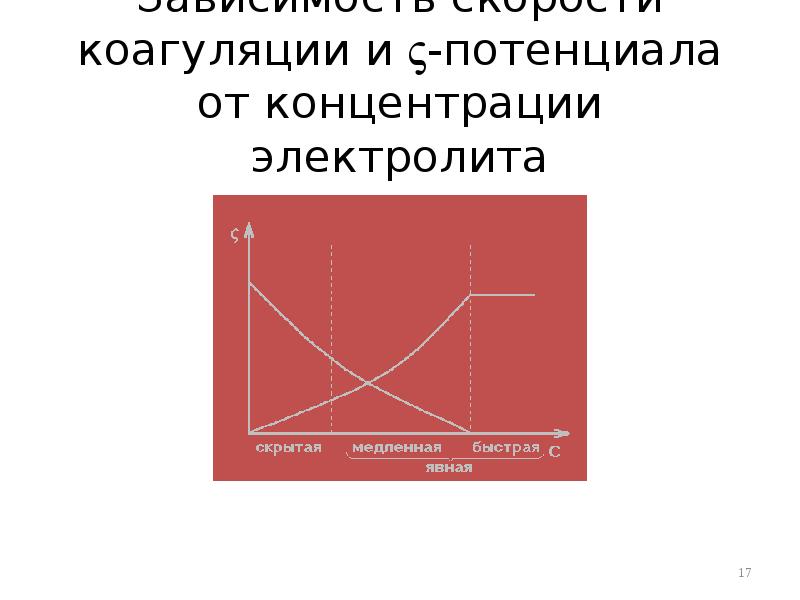
- 17. Зависимость скорости коагуляции и -потенциала от концентрации электролита
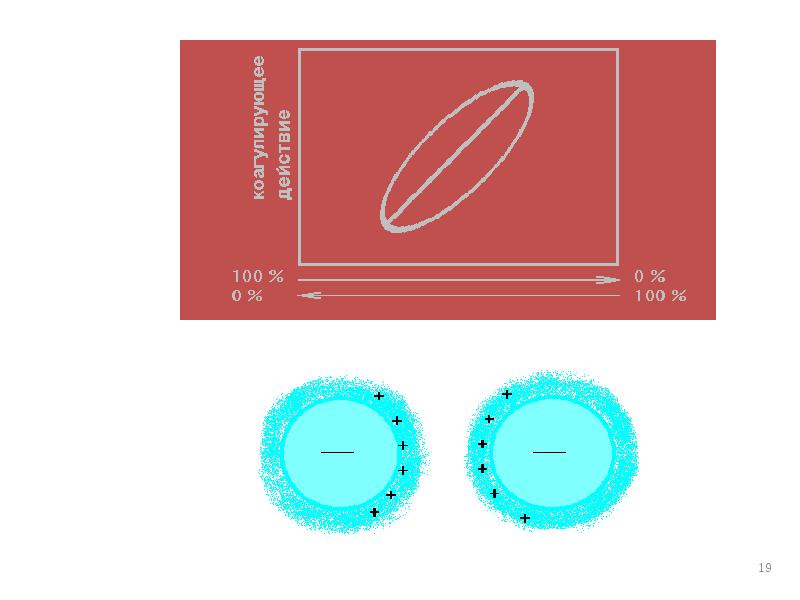
- 18. Коагуляция смесями электролитов Аддитивность (суммирование) – коагулирующий эффект от двух электролитов
- 20. Явление привыкания При медленном добавлении электролита, или порциями через большие промежутки
- 21. Взаимная коагуляция золей Происходит, если смешать два коллоидных раствора, у которых
- 22. Коллоидная защита При добавлении к гидрофобному золю высокомолекулярных веществ происходит их
- 23. «Золотое число» (железное, серебряное, рубиновое) Число мг сухого высокомолекулярного вещества, которое
- 24. Значение коллоидной защиты для живого организма При изготовлении лекарственных препаратов (колларгол
- 25. Скачать презентацию




















Слайды и текст этой презентации
Скачать презентацию на тему Устойчивость и коагуляция коллоидных растворов можно ниже:
Похожие презентации





























