Взаимодействие кислоты с основанием (реакция нейтрализации) презентация
Содержание
- 2. В точке эквивалентности число эквивалентов вещества А = числу эквивалентов вещества
- 3. Вычисления в титриметрическом анализе Концентрация растворов, способы выражения.
- 4. Форма записи: 0,1 М H2SO4 или С(H2SO4) = 1 моль/дм
- 5. Фактор эквивалентности рассчитывают по реакции:
- 6. Приготовление титрованных растворов Отметим следующие основные способы приготовления титрованных
- 7. Установочные вещества отвечают следующим требованиям: Установочные вещества отвечают следующим требованиям: 1)
- 8. Способы и методы титрования Различают два основных метода: метод
- 9. 2) Обратное титрование (титрование по избытку или титрование по остатку) 2)
- 10. но тогда и или В любом титровании
- 11. Графический метод изображения процесса нейтрализации Графическим выражением процесса кислотно-основного
- 12. 1) X=0 1) X=0 В колбе для титрования раствор сильной
- 13. 4) X>1 4) X>1 В колбе появляется свободная щелочь.
- 14. Следовательно, мы имеем право закончить титрование в интервале X=0,999÷1,001 (± 0,1%
- 15. Титрование слабой кислоты сильным основанием Схема титрования
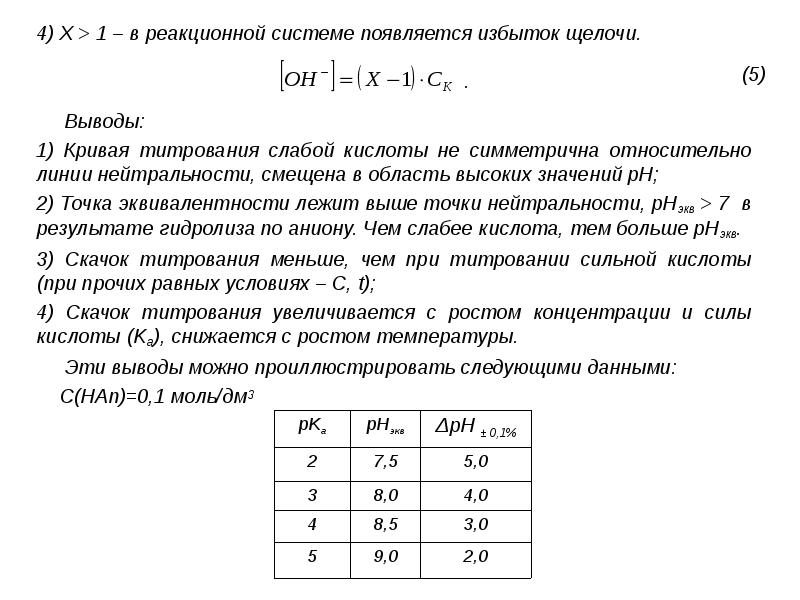
- 16. 4) X > 1 – в реакционной системе появляется избыток щелочи.
- 17. Рассмотрим титрование 0,1М HAn с рK=5. Область скачка ΔрН±0,1%=8÷10. Рассмотрим
- 18. 3) X=1 В колбе для титрования соль, но она подвергается гидролизу
- 19. Выбор индикатора: Выбор индикатора: рНэкв=5. ΔрН±0,1%=4÷6. метилоранж
- 20. Скачать презентацию


















Слайды и текст этой презентации
Скачать презентацию на тему Взаимодействие кислоты с основанием (реакция нейтрализации) можно ниже:
Похожие презентации





























