Составление уравнений окислительно-восстановительных реакций
Содержание
- 2. Окислительно–восстановительные реакции – это реакции протекающие с изменением степеней окисления
- 3. При составлении уравнений окислительно- восстановительных реакций следует учесть, что число электронов,
- 4. Метод электронного баланса
- 5. 1. Составьте химическое уравнение Al + H2SO4 Al2(SO4)3
- 6. 2. Определите и поставьте степени окисления всех элементов в формулах веществ
- 7. 3. Подчеркните знаки элементов, у которых степень окисления изменяется в процессе
- 8. 4. Определите, сколько электронов отдают или присоединяют соответствующие атомы или ионы.
- 9. 5. Составив электронный баланс, мы определим коэффициенты при окислителе и восстановителе.
- 10. 6. Проверьте, правильно ли расставлены коэффициенты с учетом общей суммы атомов
- 11. Попробуй сам 1 вариант А) Fe2O3 + HCl = FeCl3
- 12. Проверь себя 1 вариант А) Fe2O3 + HCl = FeCl3
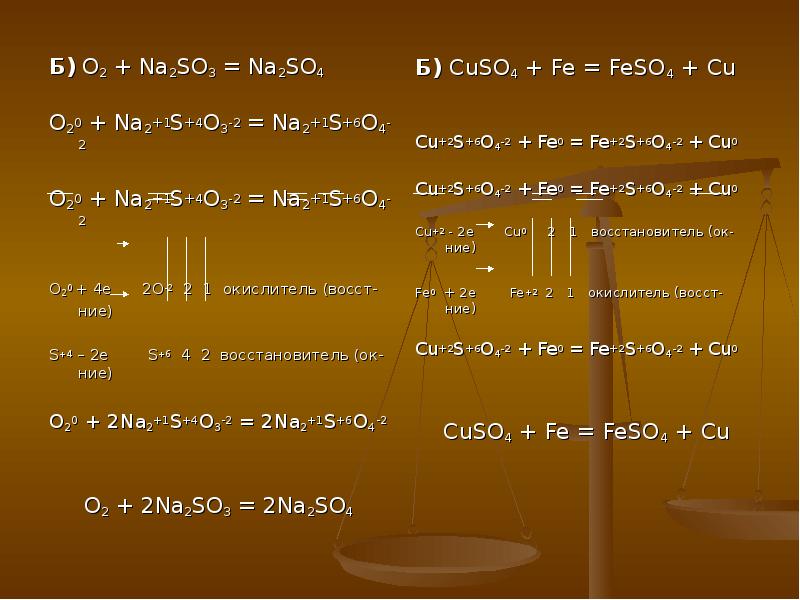
- 13. Б) O2 + Na2SO3 = Na2SO4 Б) O2 + Na2SO3 =
- 14. Скачать презентацию












Слайды и текст этой презентации
Презентация на тему Составление уравнений окислительно-восстановительных реакций доступна для скачивания ниже:
Похожие презентации





























