ЭЛЕКТРОЛИЗ презентация
Содержание
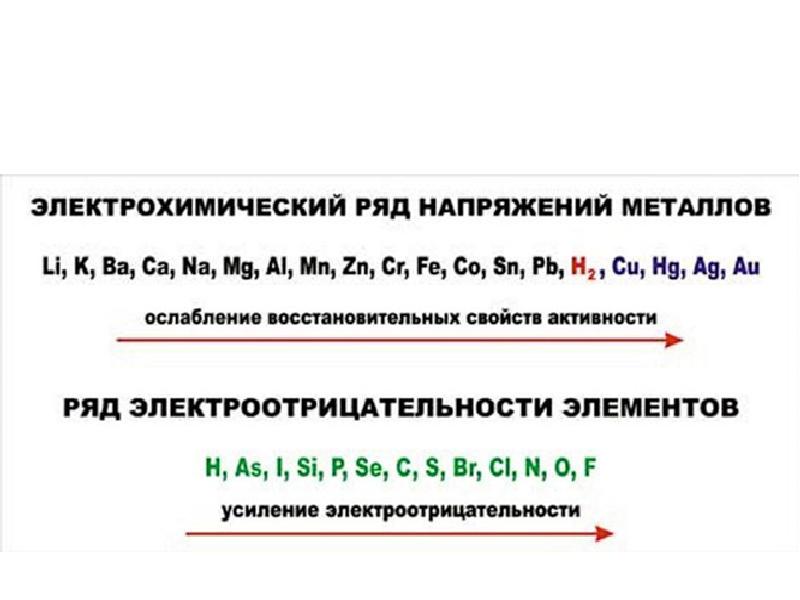
- 5. Виды электролиза Различают Электролиз расплавов и растворов веществ Электролиз с инертными
- 6. Факторы, влияющие на электролиз Состав электролита Материал электрода Температура Напряжение Сила
- 7. Электролиз расплавов с инертным анодом При электролизе расплавов соли и щелочи
- 8. Электролиз расплава соли
- 10. Электролиз воды
- 11. Электролиз водных растворов с инертным анодом При электролизе водных растворов электролитов
- 13. При электролизе растворов солей с инертным анодом используют правила: Катод: 1.
- 17. Примеры электролиза водных растворов солей с инертными графитовыми электродами
- 20. Электролиз с растворимым анодом На аноде происходит окисление металла. На катоде
- 21. Если в системе присутствуют несколько различных ионов: На катоде в первую
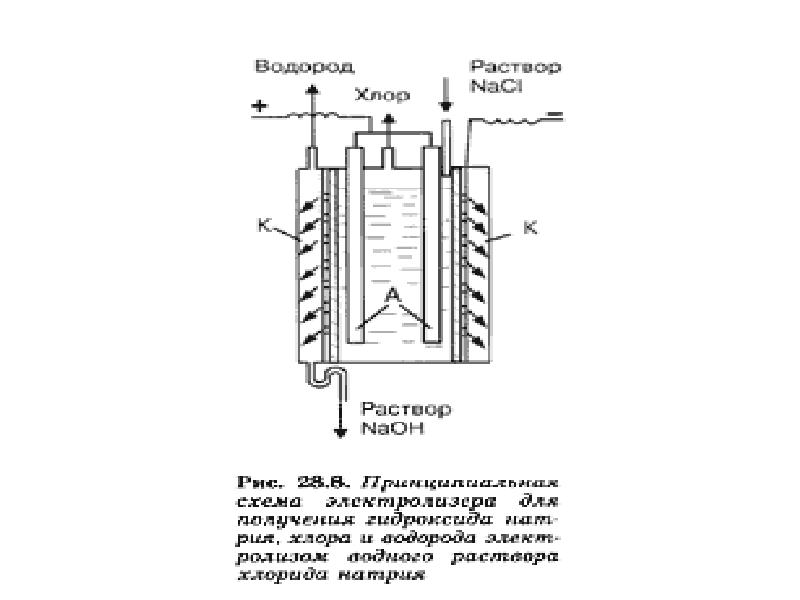
- 28. ПРИМЕНЕНИЕ ЭЛЕКТРОЛИЗА Электролиз нашел широкое применение в технике, например в металлургии,
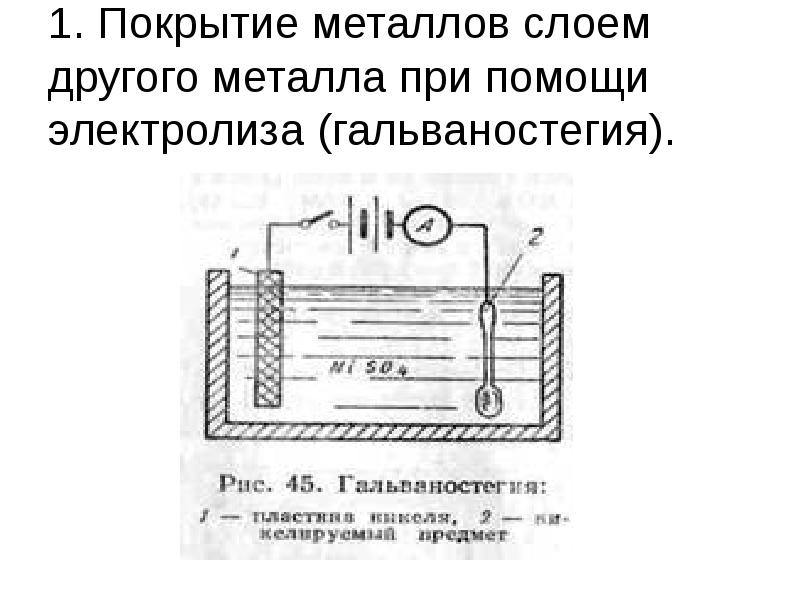
- 29. 1. Покрытие металлов слоем другого металла при помощи электролиза (гальваностегия).
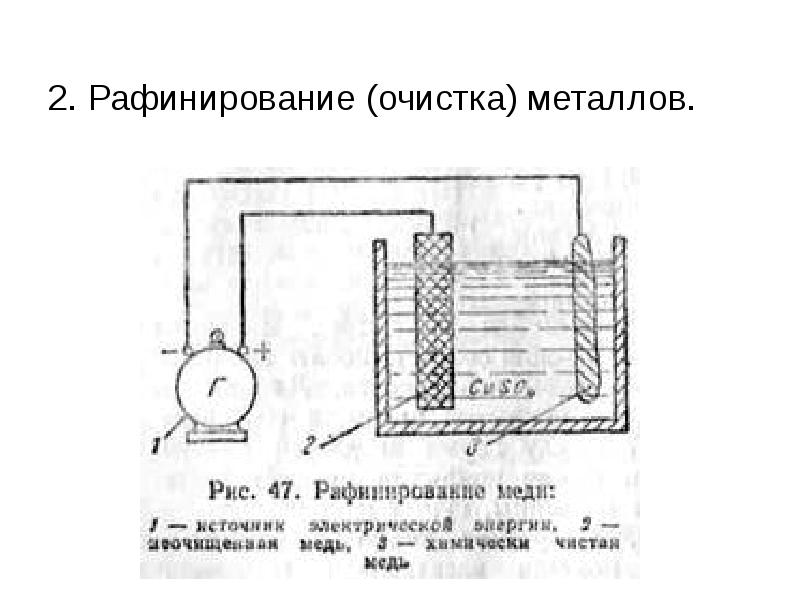
- 30. 2. Рафинирование (очистка) металлов.
- 32. Скачать презентацию

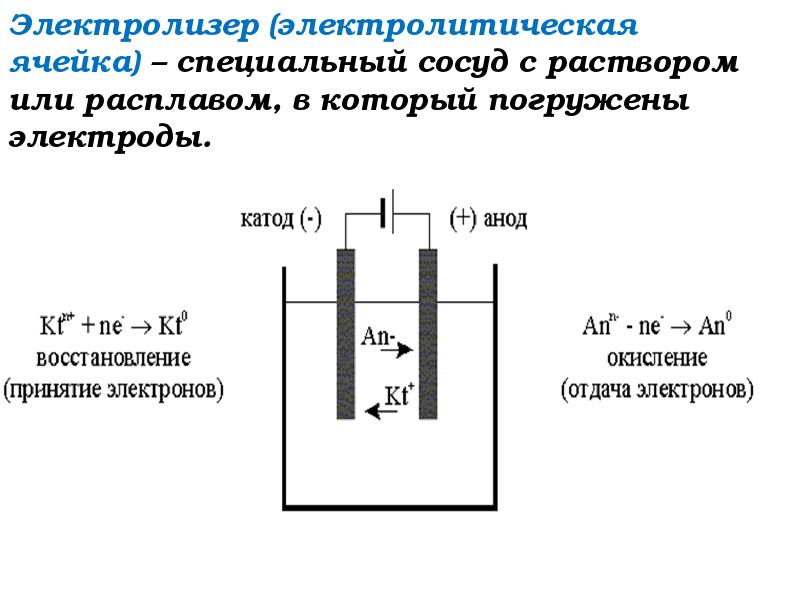








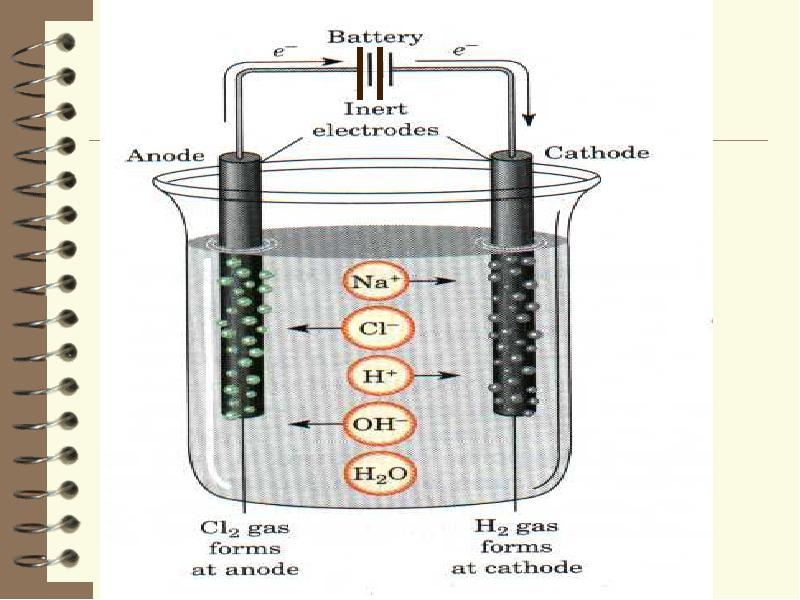



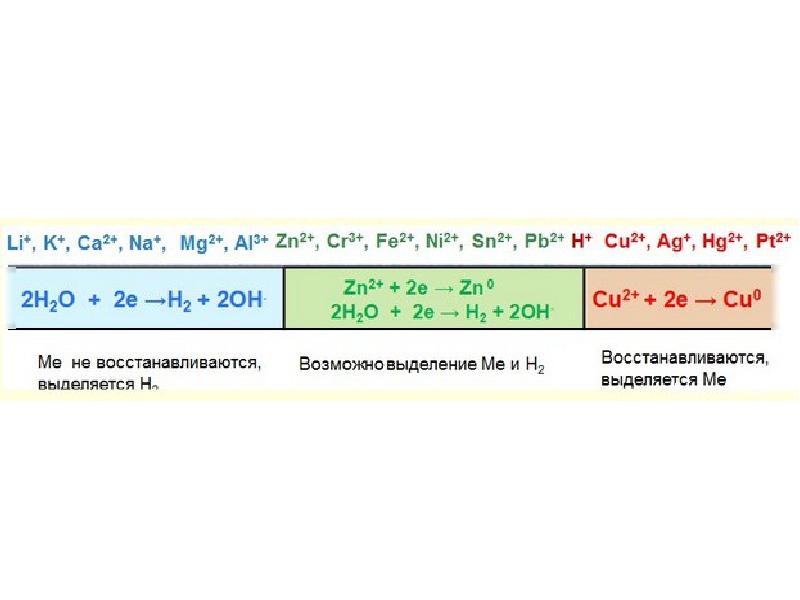











Слайды и текст этой презентации
Похожие презентации





























