Электролитическая диссоциация. Электролиты и неэлектролиты
Содержание
- 2. Тест 1. Выберите вещество с ковалентной неполярной связью: А) NaCl;
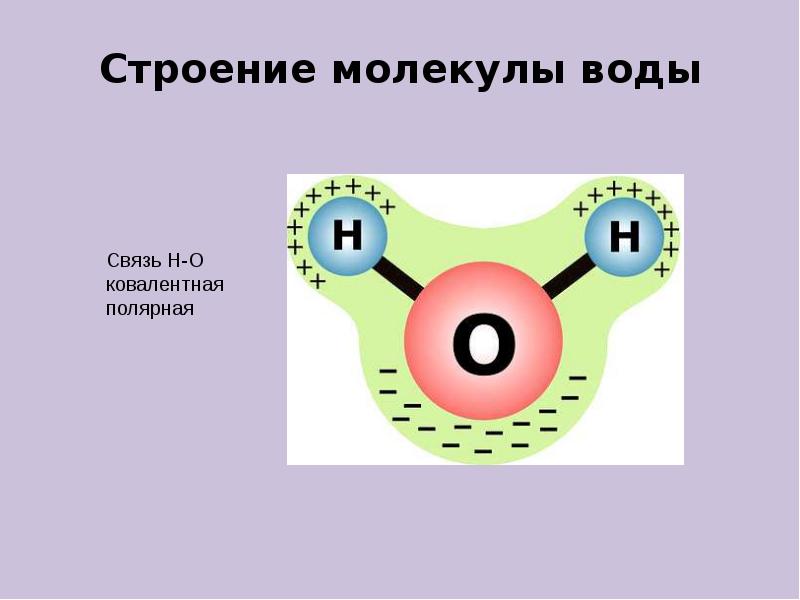
- 4. Строение молекулы воды Строение молекулы воды
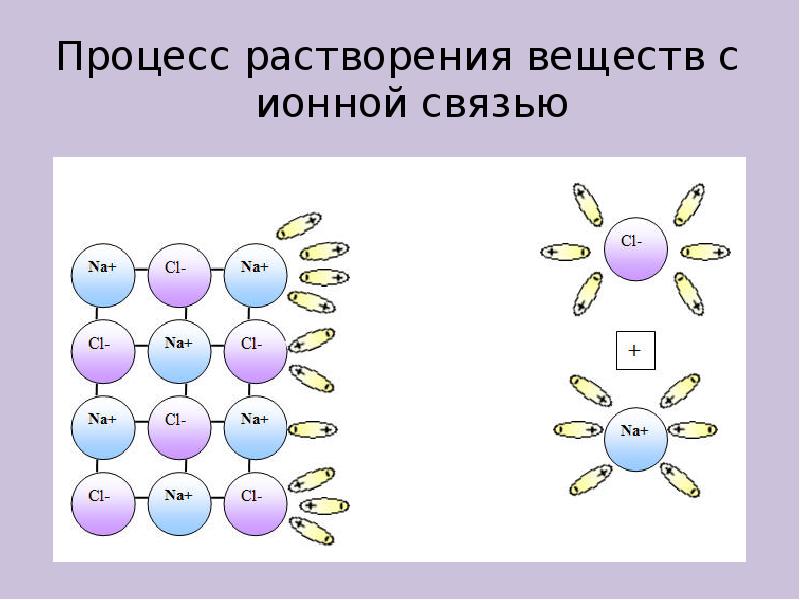
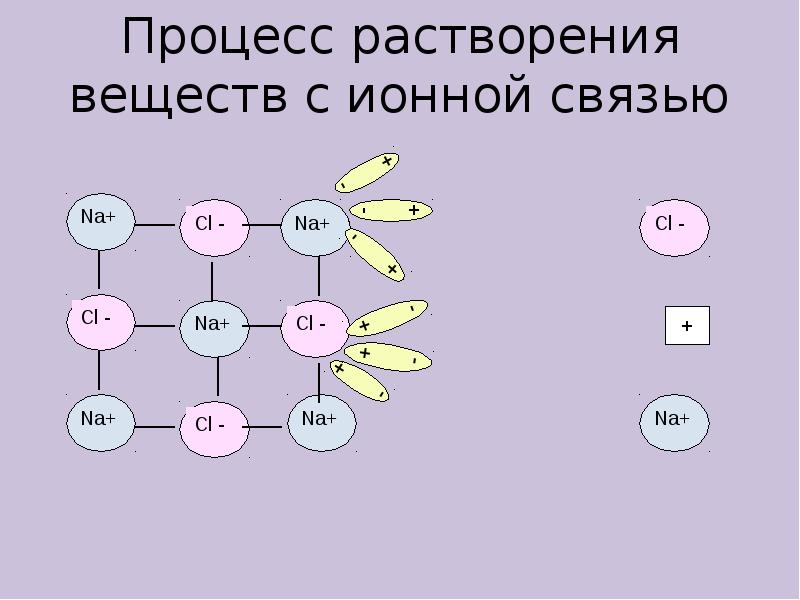
- 6. Процесс растворения веществ с ионной связью Процесс растворения веществ с ионной
- 7. Процесс растворения веществ с ионной связью
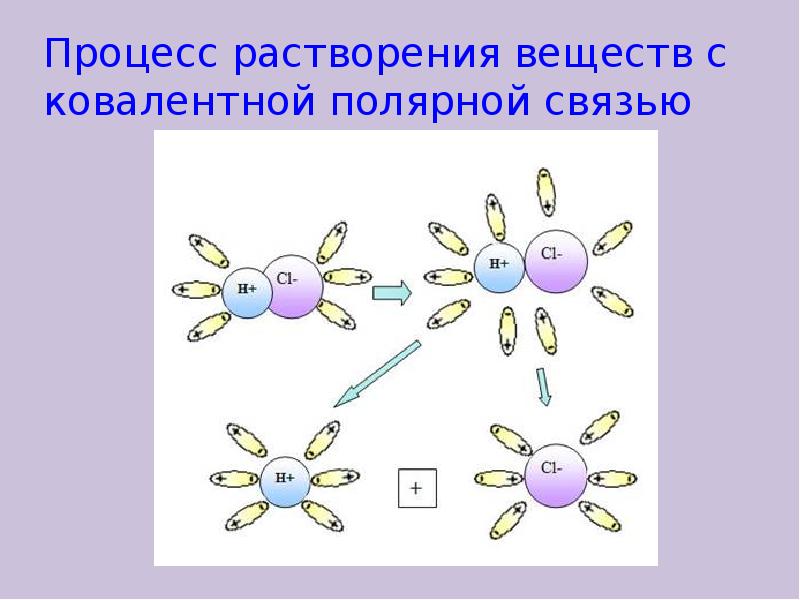
- 8. Процесс растворения веществ с ковалентной полярной связью Процесс растворения веществ с
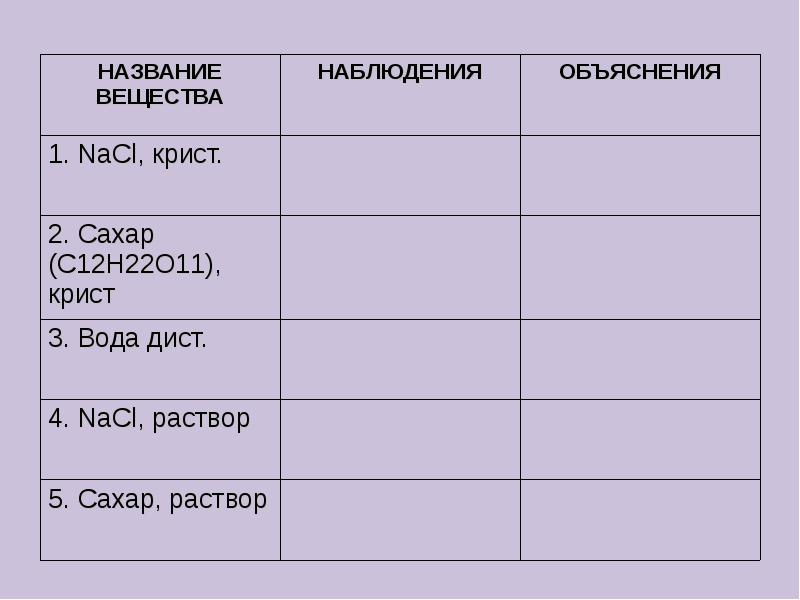
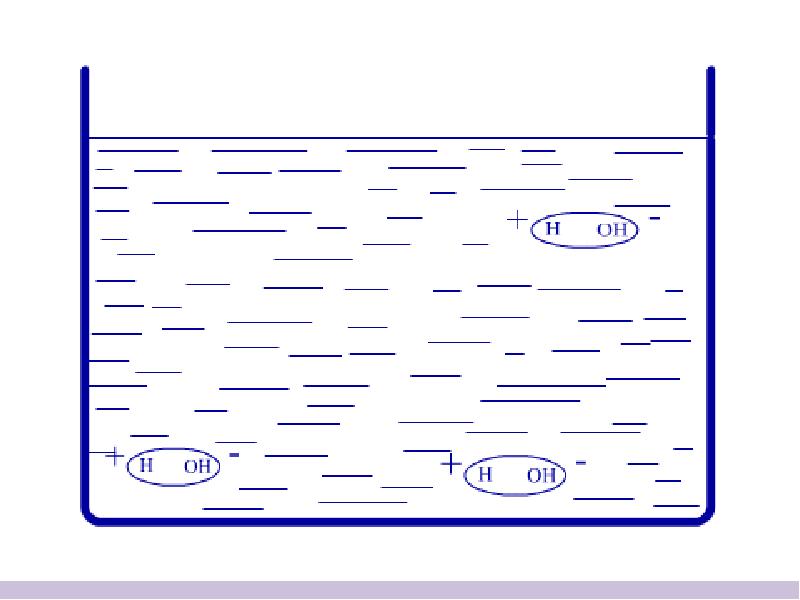
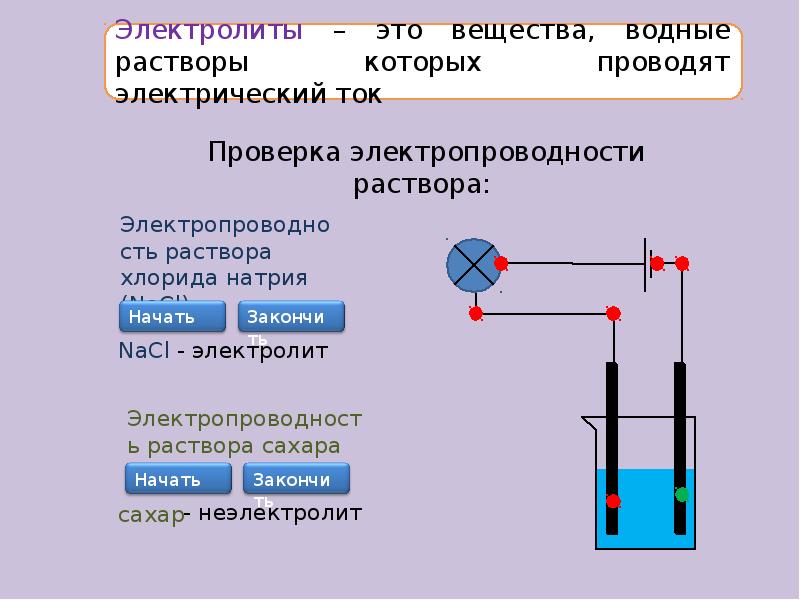
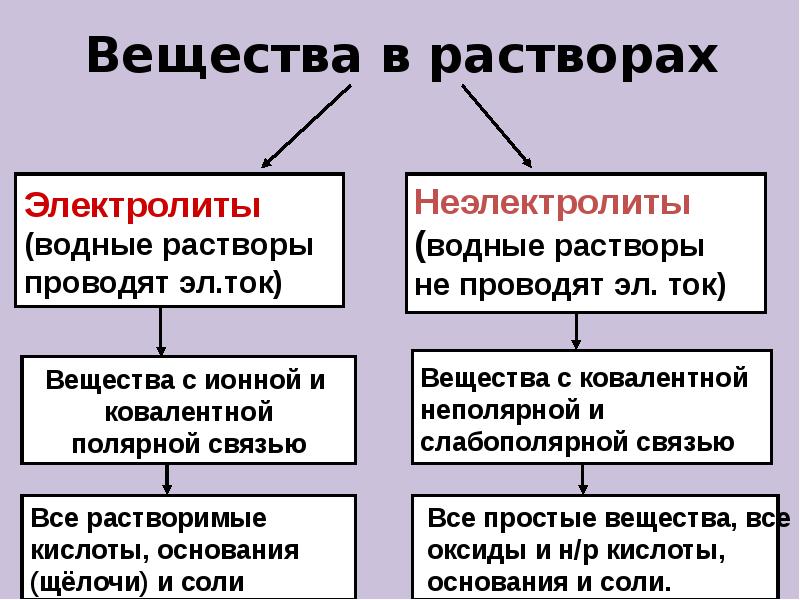
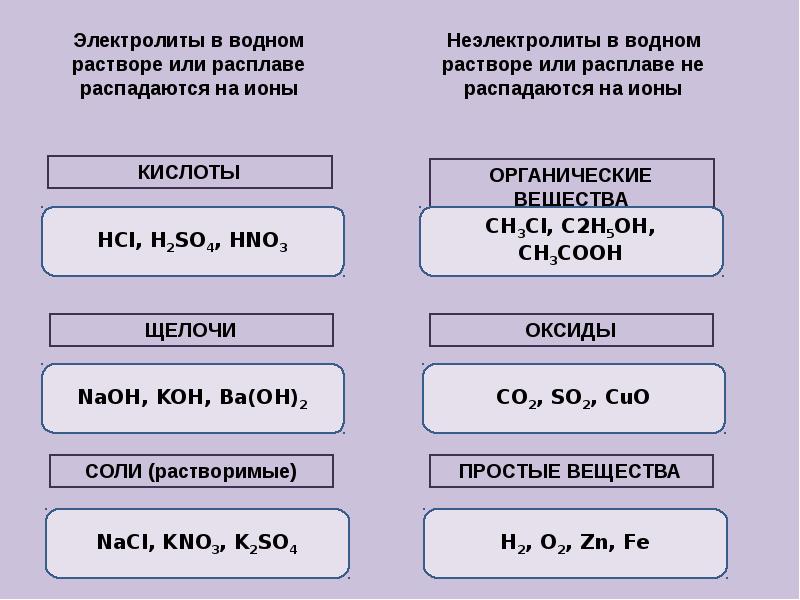
- 11. Вещества в растворах
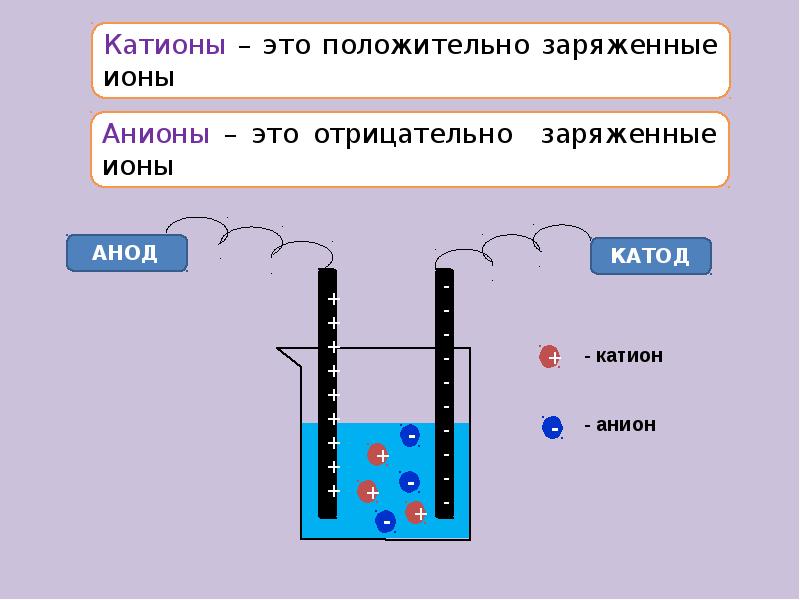
- 14. Типы ионов По заряду: катионы (положительные) и анионы (отрицательные); По отношению
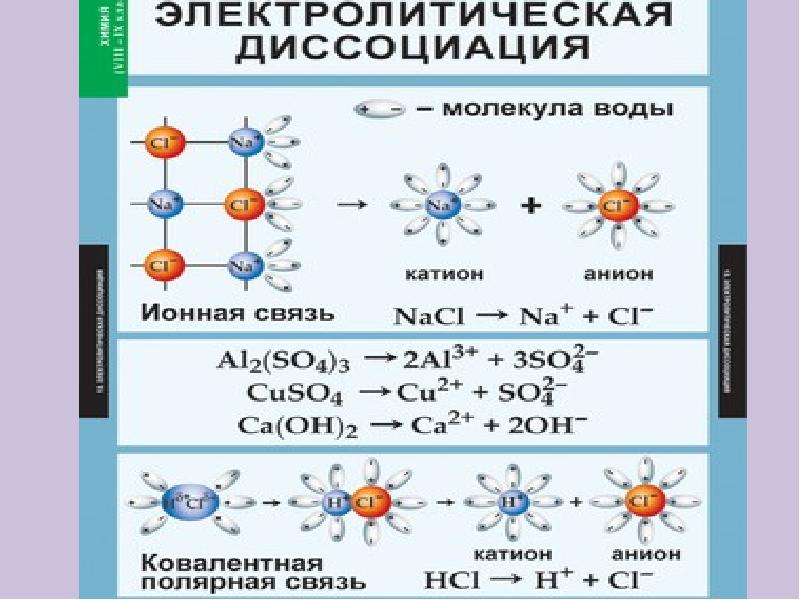
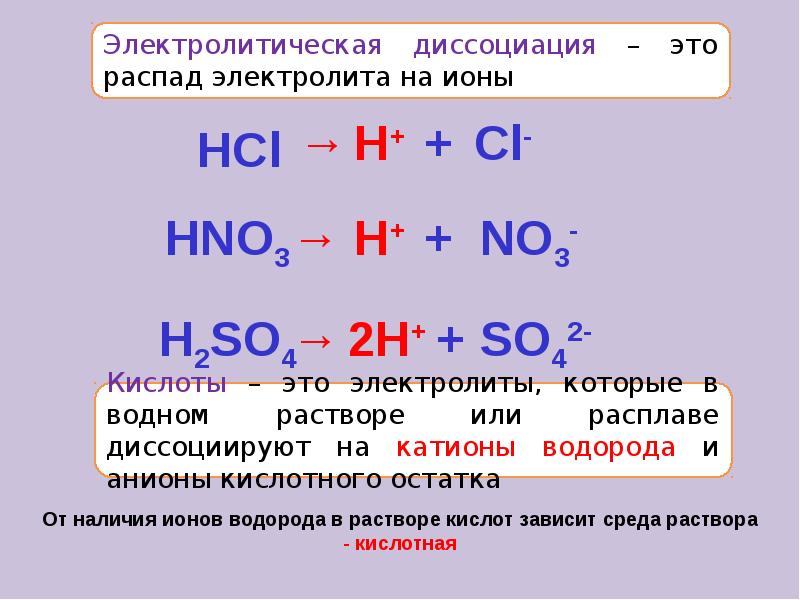
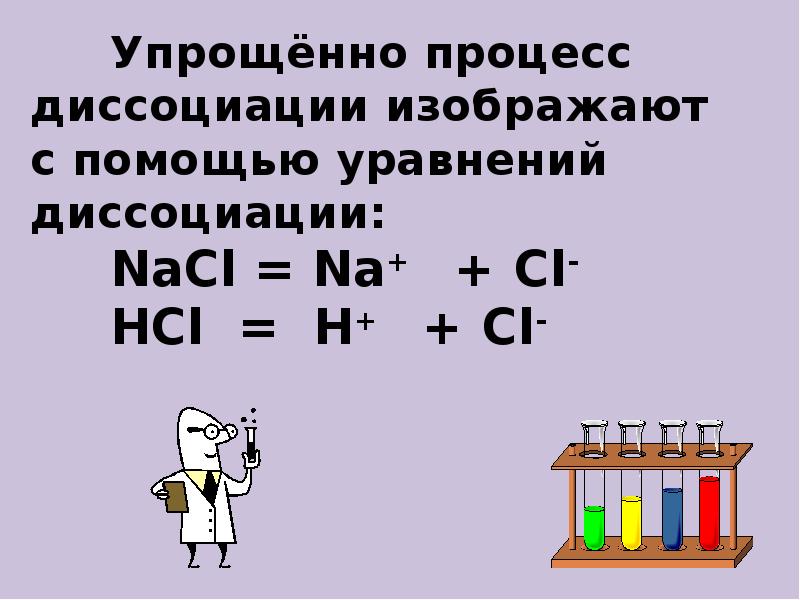
- 18. Упрощённо процесс диссоциации изображают с помощью уравнений диссоциации: NaCl = Na+
- 19. «Третий лишний» «Третий лишний»
- 20. Скачать презентацию






Слайды и текст этой презентации
Презентация на тему Электролитическая диссоциация. Электролиты и неэлектролиты доступна для скачивания ниже:
Похожие презентации





























