Метаболизм липидов презентация
Содержание
- 2. Вопросы устного экзамена по метаболизму липидов Транспорт липидов в организме. Липопротеины
- 3. Структура темы Классификация липидов ВЖК Ацилглицеролы (МАГ, ДАГ, ТАГ) Глицерофосфолипиды (фосфатидилхолин,
- 4. Бета-окисление вжк
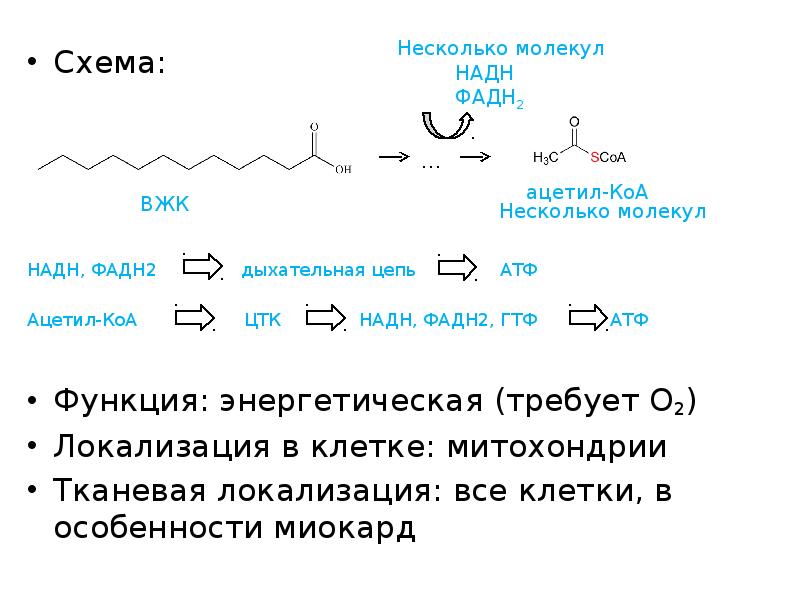
- 5. Схема: Схема: НАДН, ФАДН2 дыхательная цепь
- 6. Этапы Попадание ВЖК внутрь клетки из крови, и активация ВЖК в
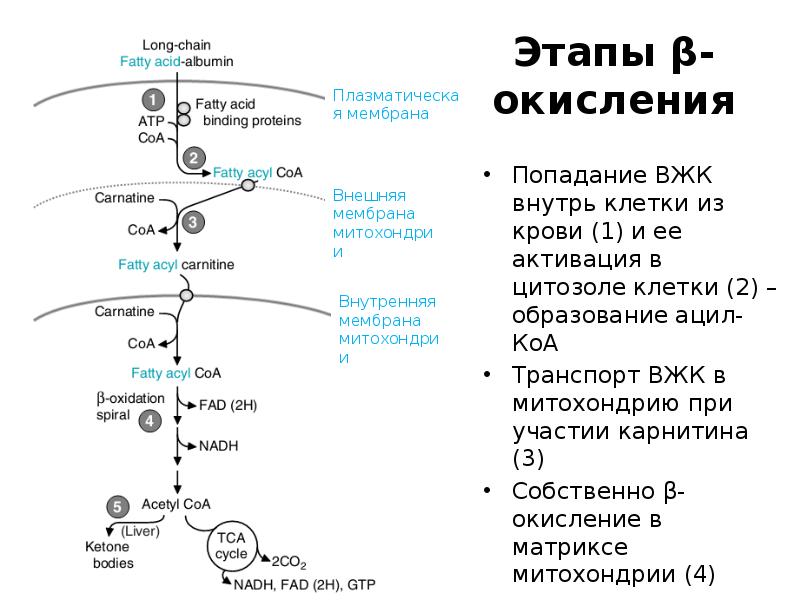
- 7. Этапы β-окисления Попадание ВЖК внутрь клетки из крови (1) и ее
- 8. Попадание ВЖК внутрь клетки из крови, и активация ВЖК в цитозоле
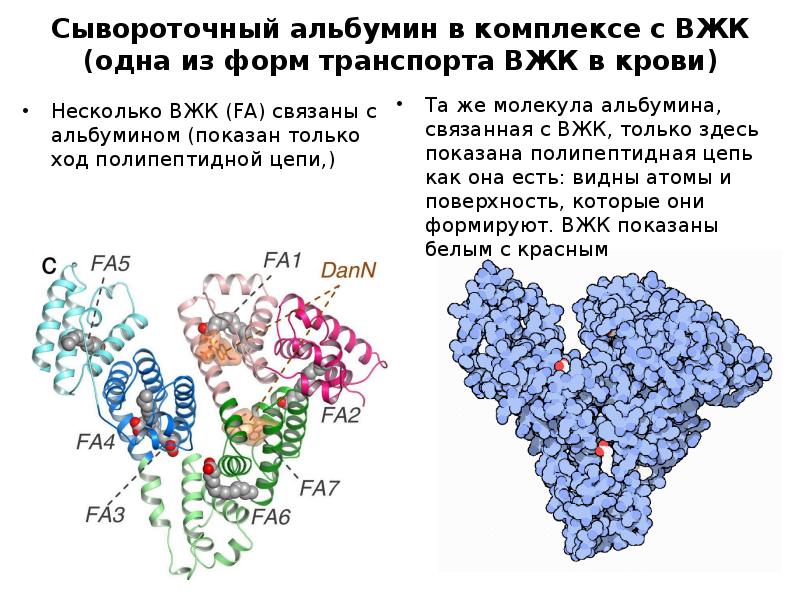
- 9. Сывороточный альбумин в комплексе с ВЖК (одна из форм транспорта ВЖК
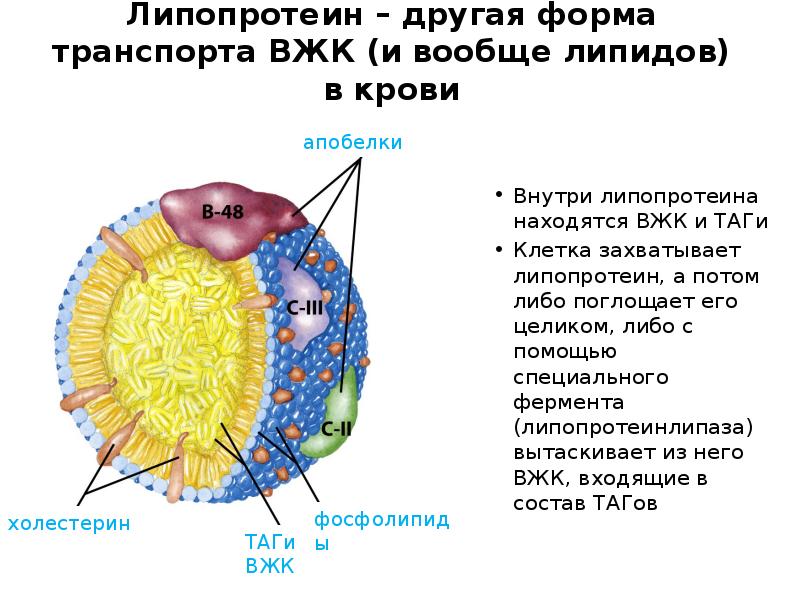
- 10. Липопротеин – другая форма транспорта ВЖК (и вообще липидов) в крови
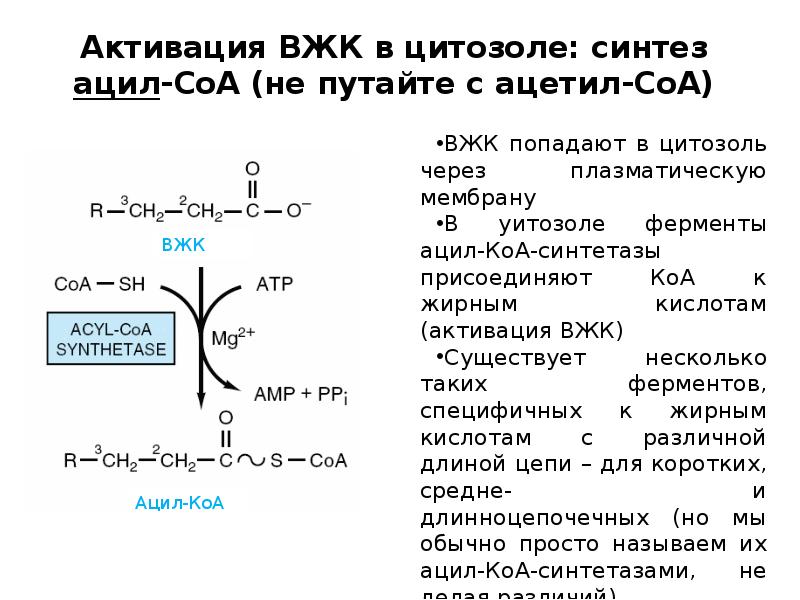
- 11. Активация ВЖК в цитозоле: синтез ацил-СоА (не путайте с ацетил-СоА)
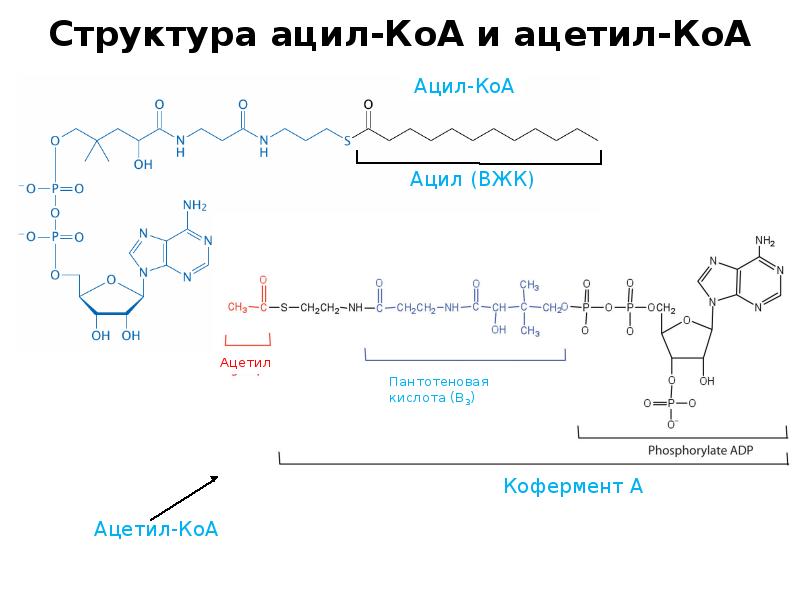
- 12. Структура ацил-КоА и ацетил-КоА
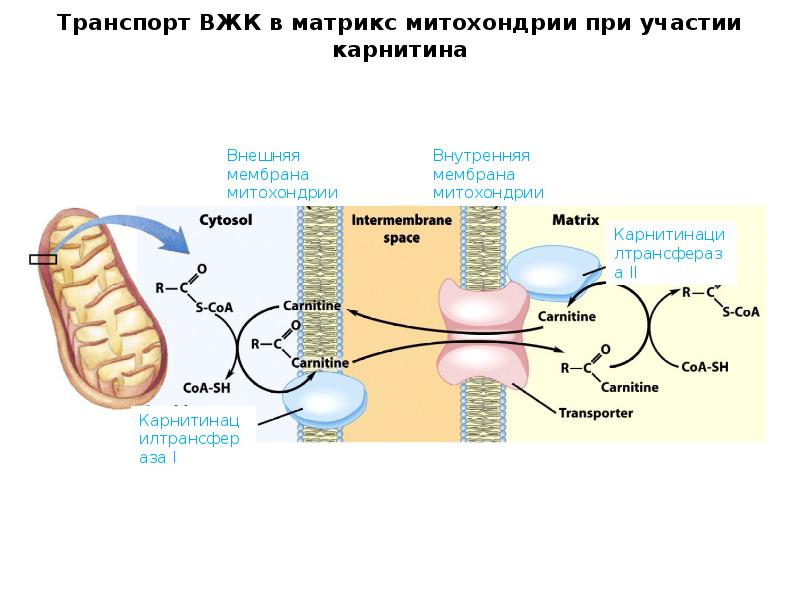
- 13. Транспорт ВЖК в митохондрию при участии карнитина Ферменты: карнитин-ацилтрансфераза 1 и
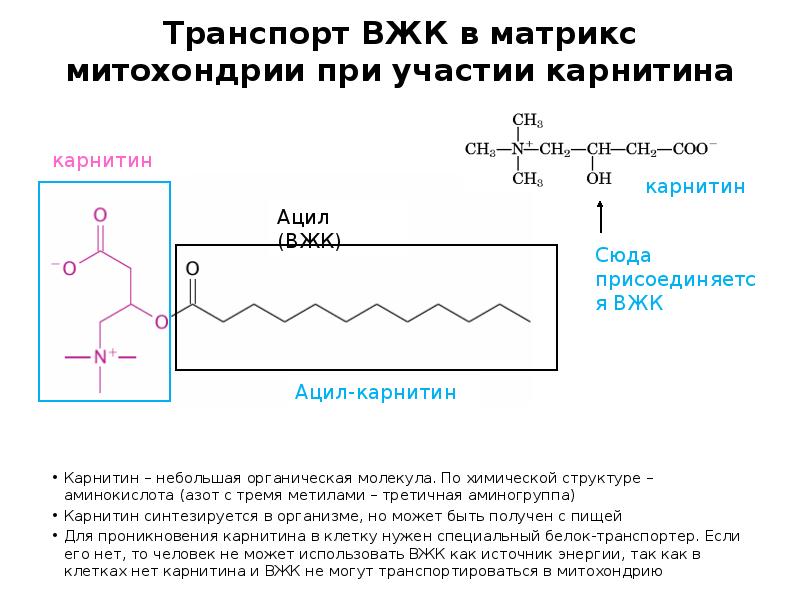
- 14. Транспорт ВЖК в матрикс митохондрии при участии карнитина Карнитин – небольшая
- 15. Транспорт ВЖК в матрикс митохондрии при участии карнитина
- 16. Собственно β-окисление в матриксе митохондрии Последовательное отщепление 2С-фрагмента (ацетил-КоА) от ацил-КоА
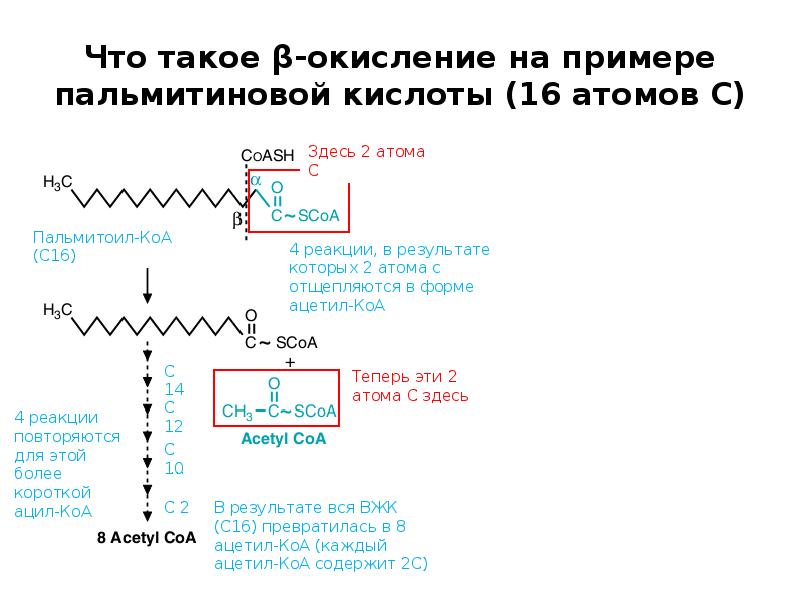
- 17. Что такое β-окисление на примере пальмитиновой кислоты (16 атомов С)
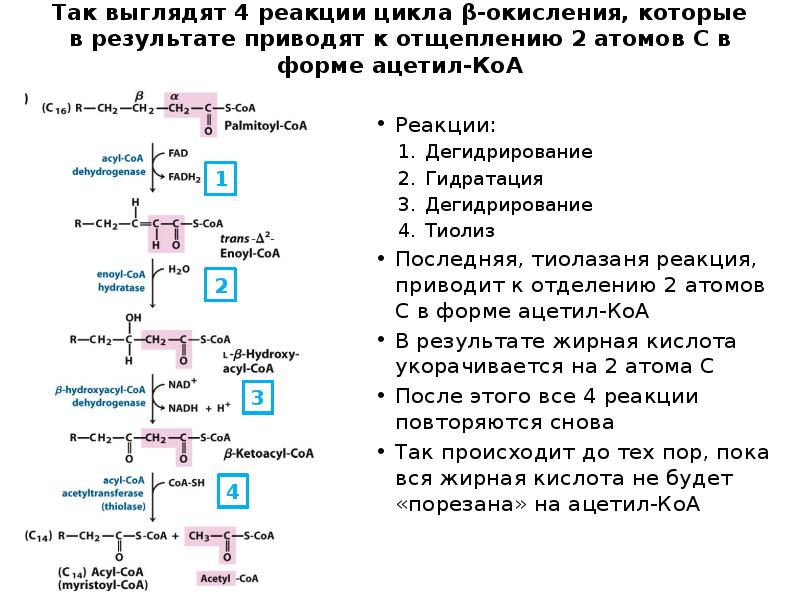
- 18. Так выглядят 4 реакции цикла β-окисления, которые в результате приводят к
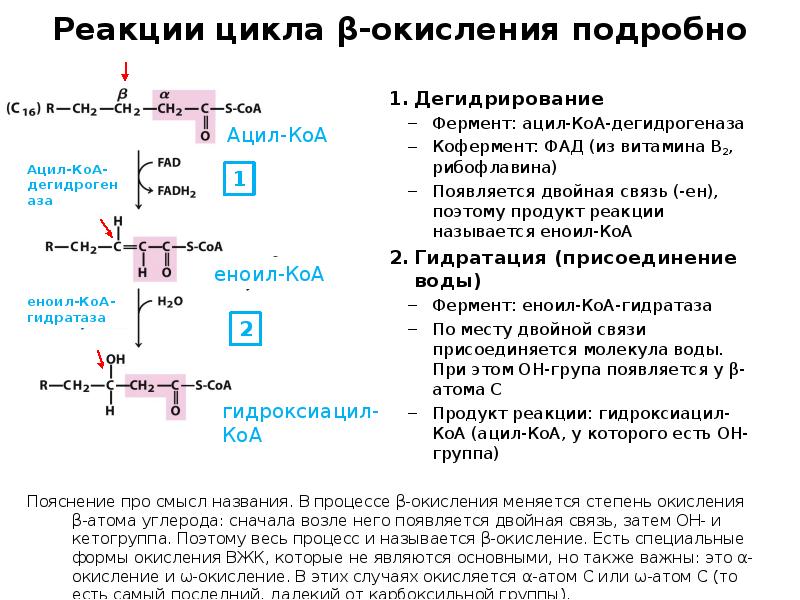
- 19. Реакции цикла β-окисления подробно Дегидрирование Фермент: ацил-КоА-дегидрогеназа Кофермент: ФАД (из витамина
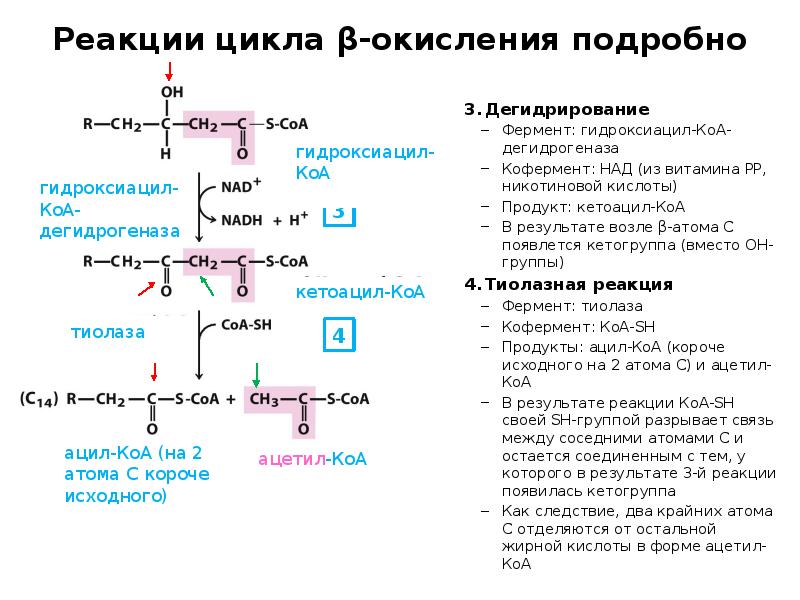
- 20. Реакции цикла β-окисления подробно Дегидрирование Фермент: гидроксиацил-КоА-дегидрогеназа Кофермент: НАД (из витамина
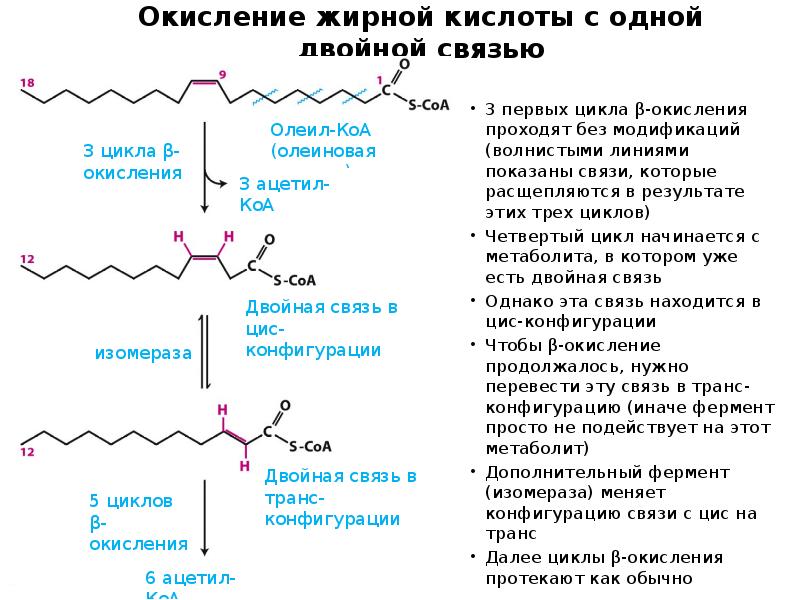
- 21. Особенности β-окисления ненасыщенных ВЖК β-окисление происходит как обычно до тех пор,
- 22. Окисление жирной кислоты с одной двойной связью 3 первых цикла β-окисления
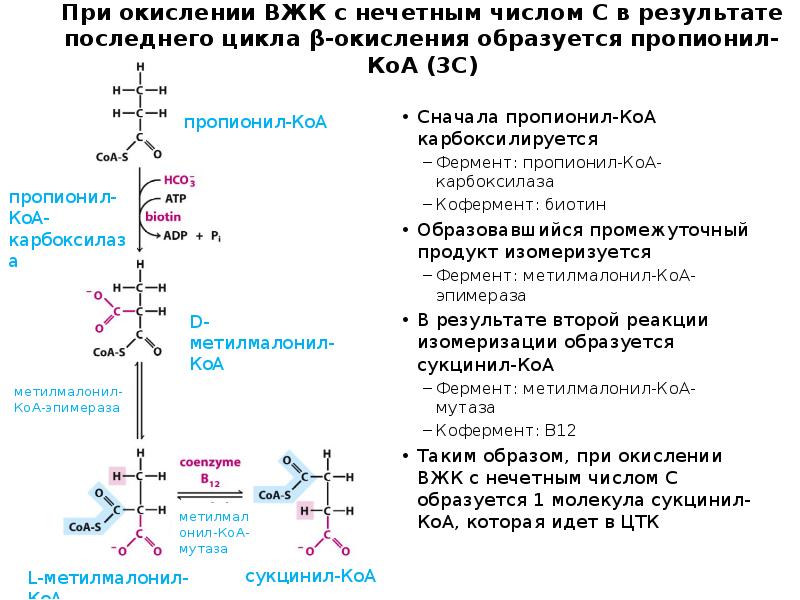
- 23. Особенности β-окисления ВЖК с нечетным числом С При β-окислении ВЖК с
- 24. При окислении ВЖК с нечетным числом С в результате последнего цикла
- 25. Синтез вжк
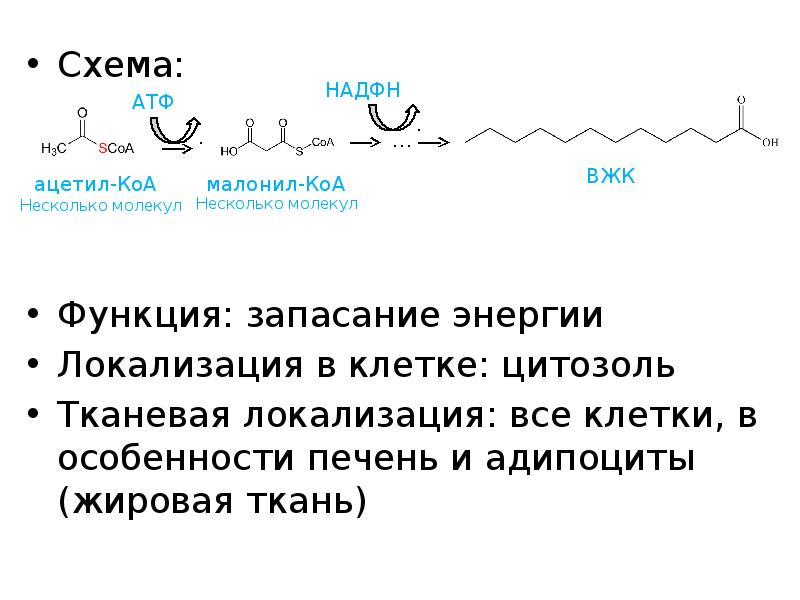
- 26. Схема: Схема: Функция: запасание энергии Локализация в клетке: цитозоль Тканевая локализация:
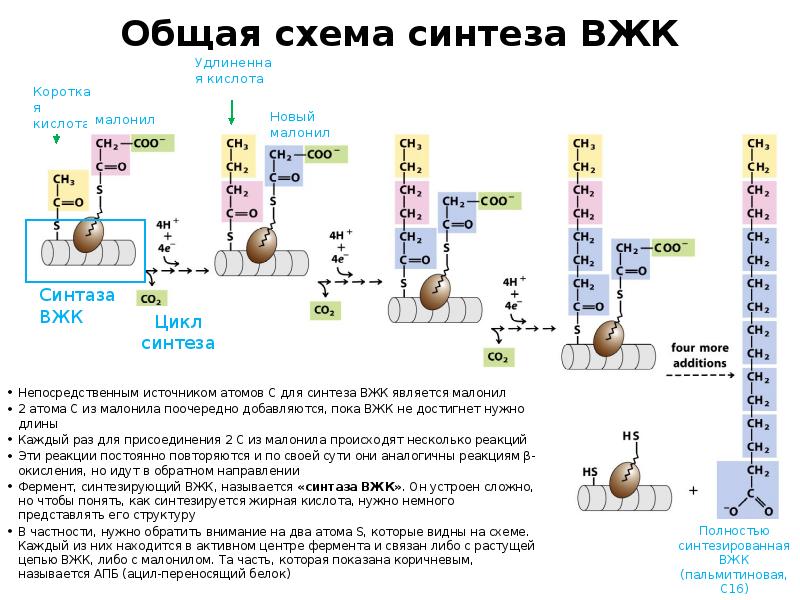
- 27. Общая схема синтеза ВЖК Непосредственным источником атомов С для синтеза ВЖК
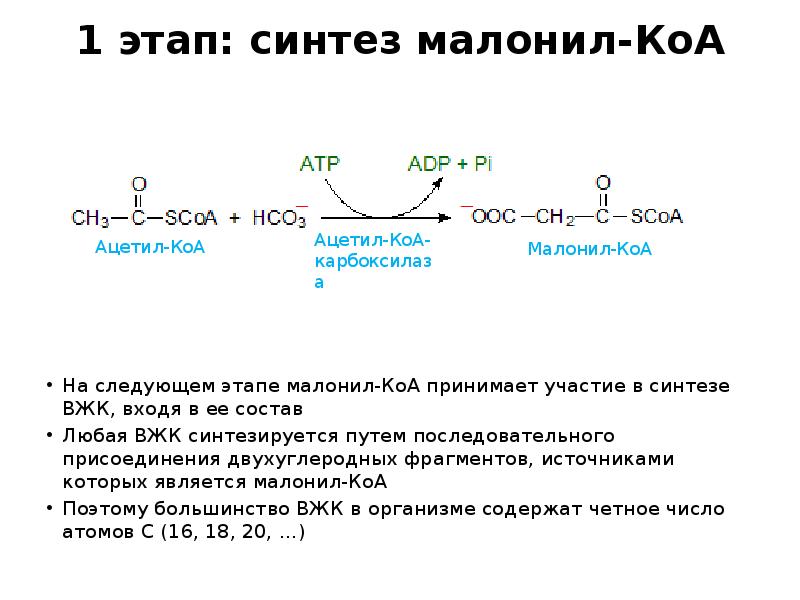
- 28. Этапы Превращение ацетил-КоА в малонил-КоА (карбоксилирование = присоединение карбоксильной группы): Фермент:
- 29. 1 этап: синтез малонил-КоА На следующем этапе малонил-КоА принимает участие в
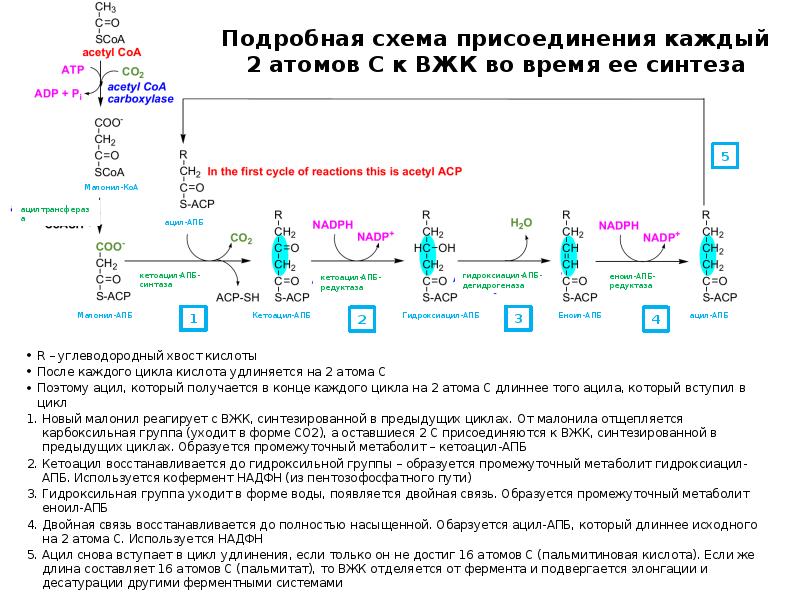
- 30. Присоединение малонил-КоА к растущей цепи жирной кислоты и дальнейшие реакции Фермент:
- 31. Подробная схема присоединения каждый 2 атомов С к ВЖК во время
- 32. Элонгация и десатурация (синтез более длинных и ненасыщенных ВЖК) Элонгация (удлинение)
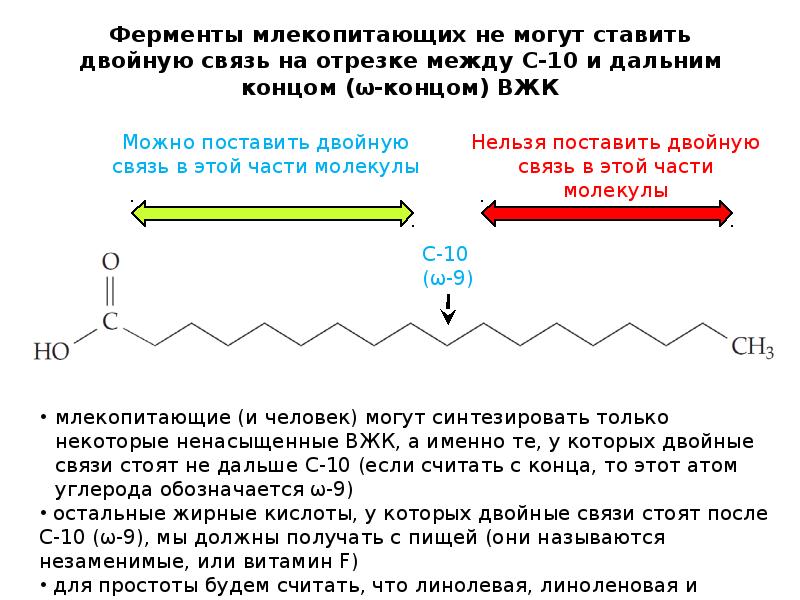
- 33. Ферменты млекопитающих не могут ставить двойную связь на отрезке между С-10
- 34. Дополнение Источники ацетил-КоА для синтеза ВЖК Источники НАДФ (и сравнение НАДФН
- 35. Источники ацетил-КоА для синтеза ВЖК Откуда такой вопрос? Дело в том,
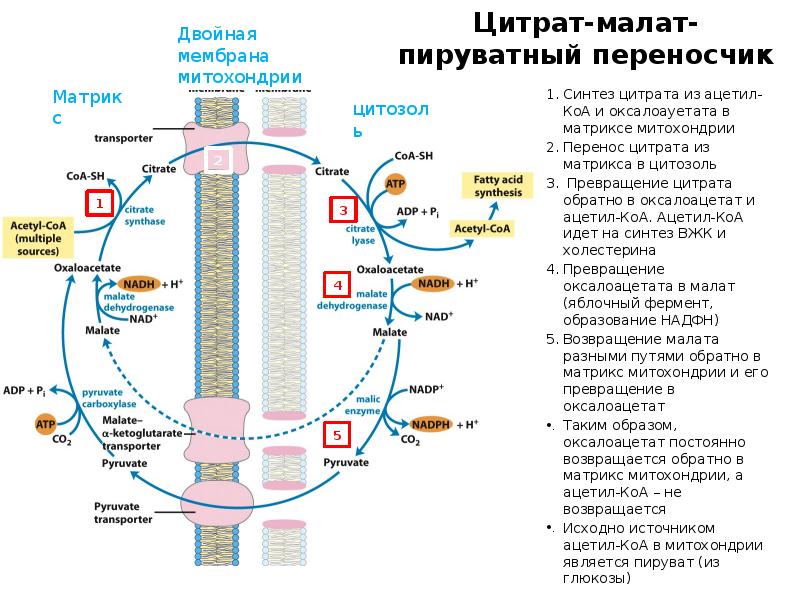
- 36. Цитрат-малат-пируватный переносчик Синтез цитрата из ацетил-КоА и оксалоауетата в матриксе митохондрии
- 37. Источники НАДФ (и сравнение НАДФН и НАДН) Что такое: НАДФН =
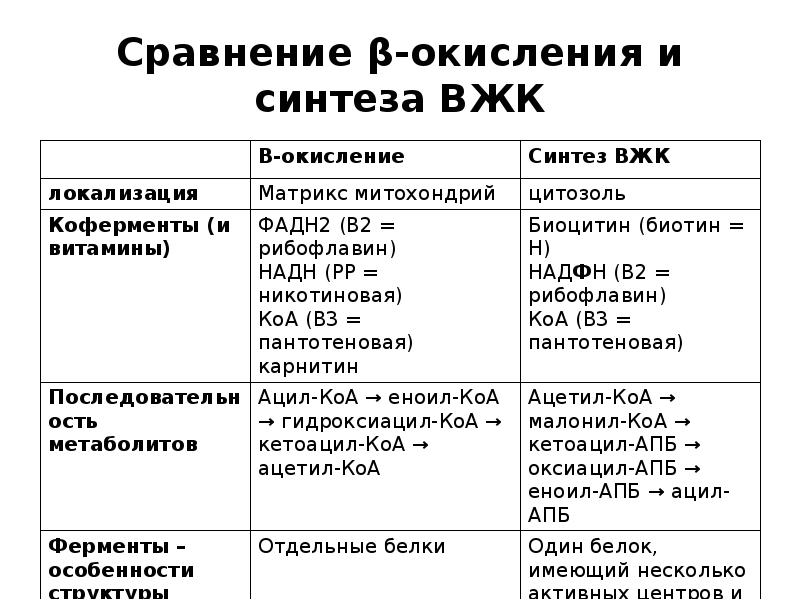
- 38. Сравнение β-окисления и синтеза ВЖК
- 39. Синтез холестерина
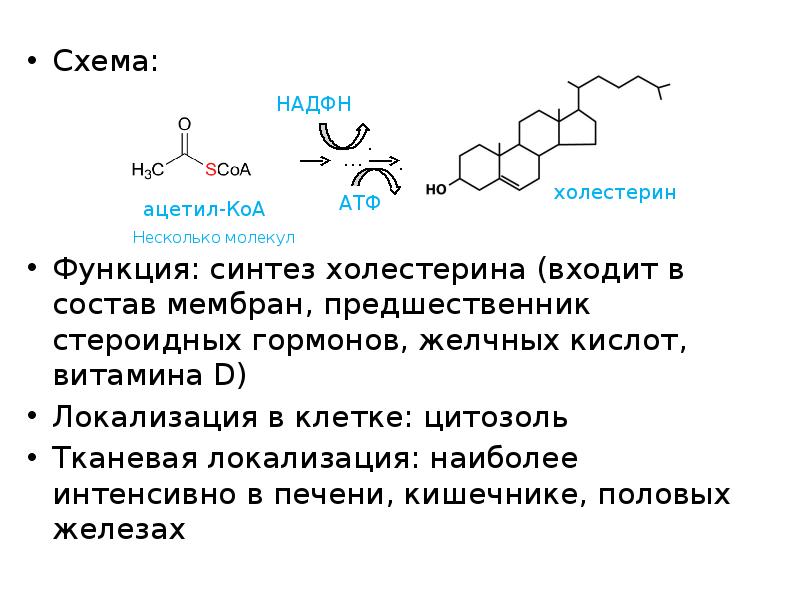
- 40. Схема: Схема: Функция: синтез холестерина (входит в состав мембран, предшественник стероидных
- 41. Основной принцип Последовательное соединение молекул, содержащих небольшое количество атомов С На
- 42. 4 этапа синтеза холестерина Синтез мевалоновой кислоты Исходное вещество – ацетил-КоА
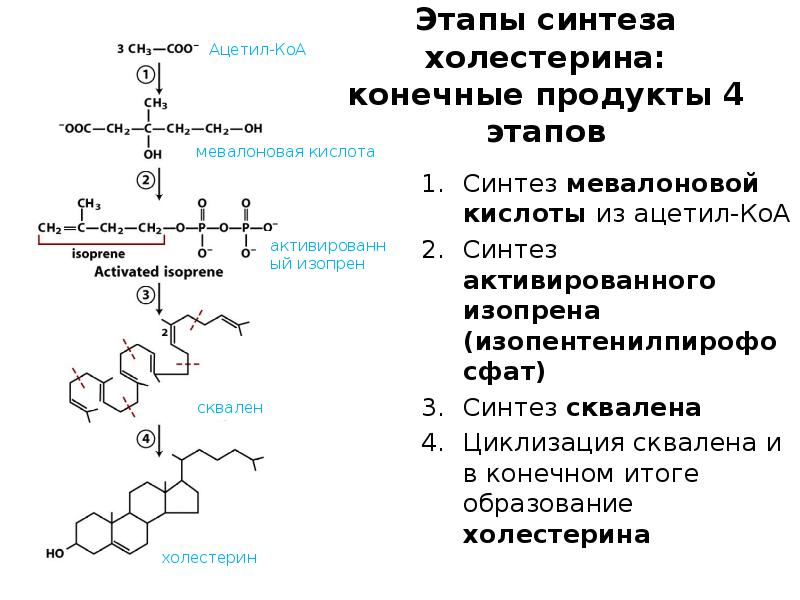
- 43. Этапы синтеза холестерина: конечные продукты 4 этапов Синтез мевалоновой кислоты из
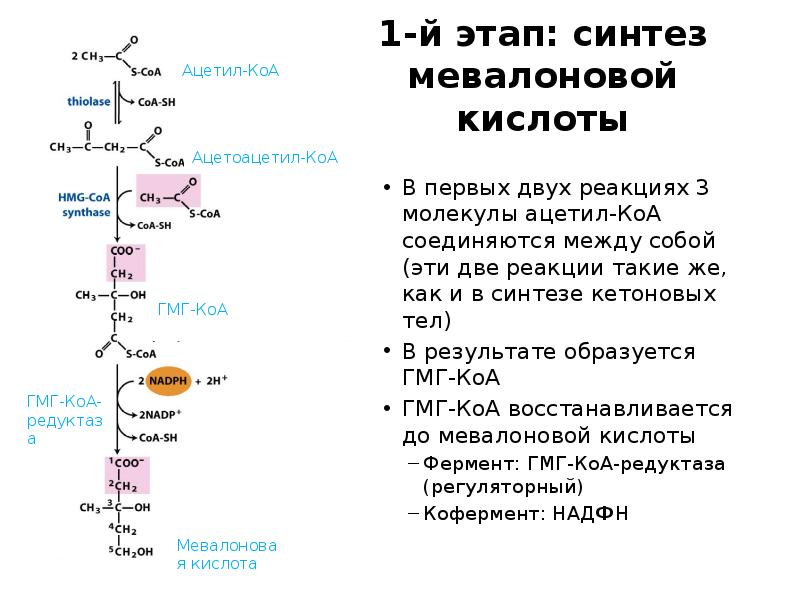
- 44. 1-й этап: синтез мевалоновой кислоты В первых двух реакциях 3 молекулы
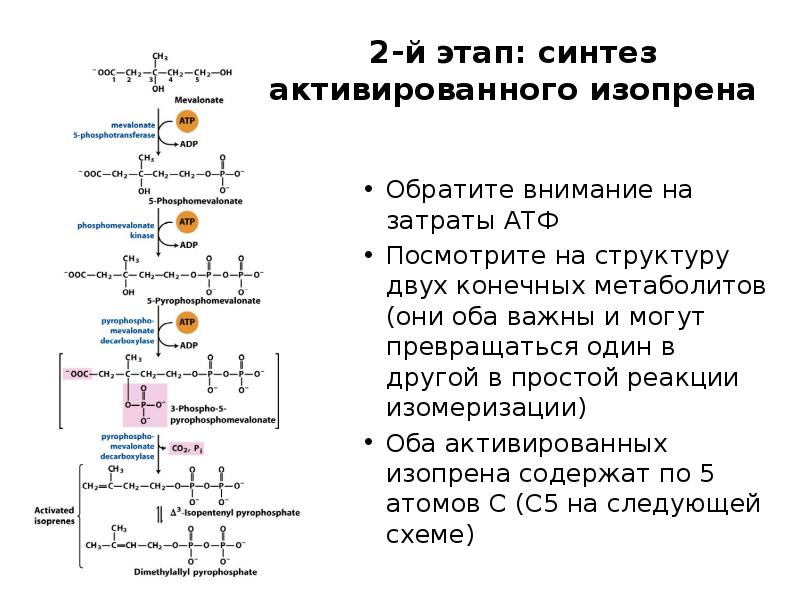
- 45. 2-й этап: синтез активированного изопрена Обратите внимание на затраты АТФ Посмотрите
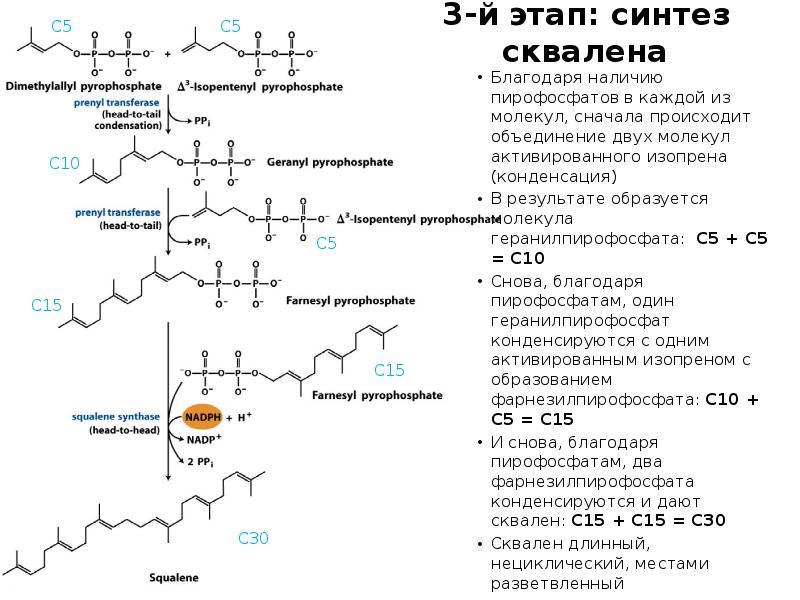
- 46. 3-й этап: синтез сквалена Благодаря наличию пирофосфатов в каждой из молекул,
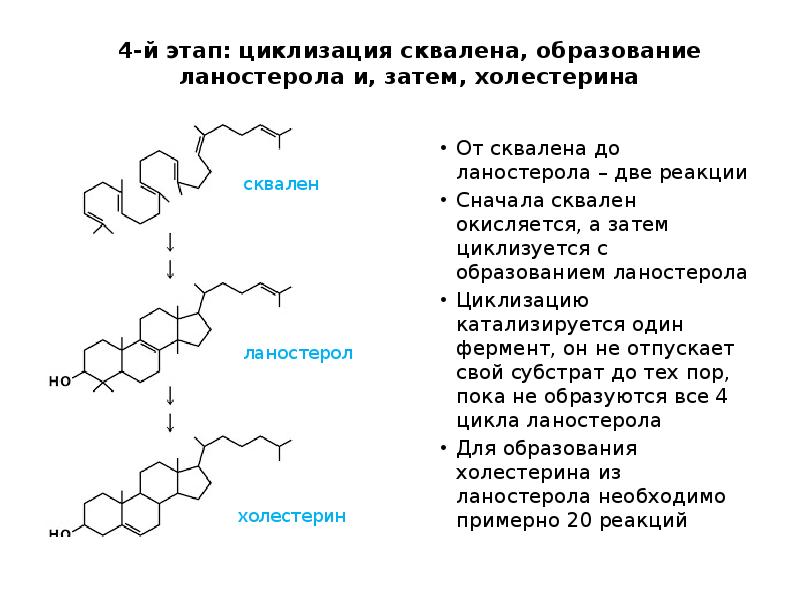
- 47. 4-й этап: циклизация сквалена, образование ланостерола и, затем, холестерина От сквалена
- 48. Кетоновые (ацетоновые) тела
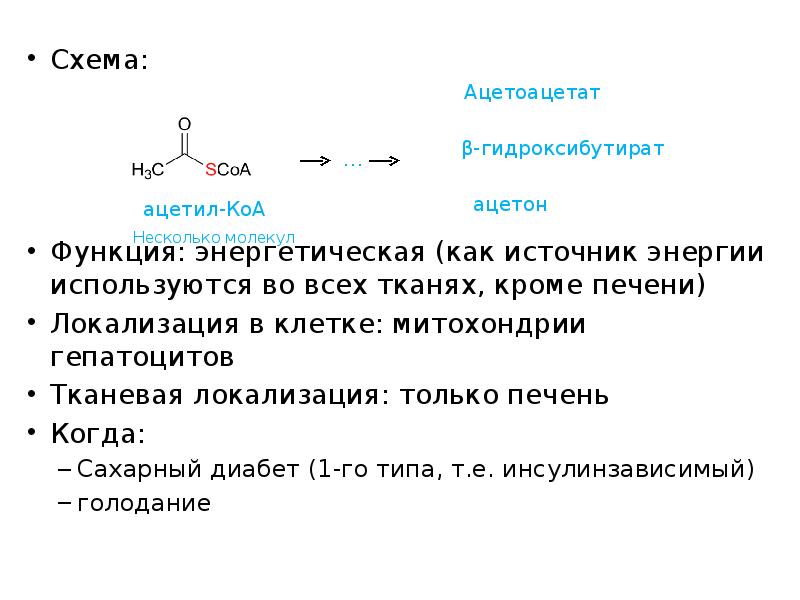
- 49. Схема: Схема: Функция: энергетическая (как источник энергии используются во всех тканях,
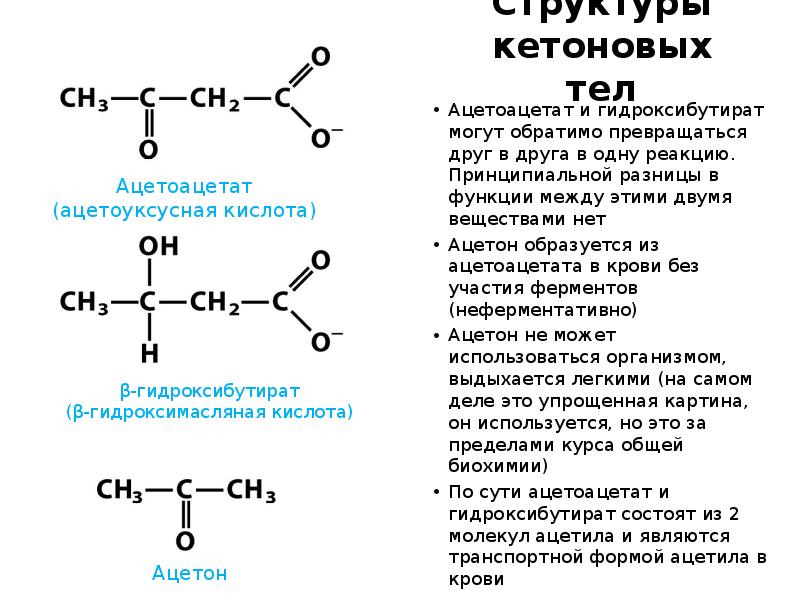
- 50. Структуры кетоновых тел Ацетоацетат и гидроксибутират могут обратимо превращаться друг в
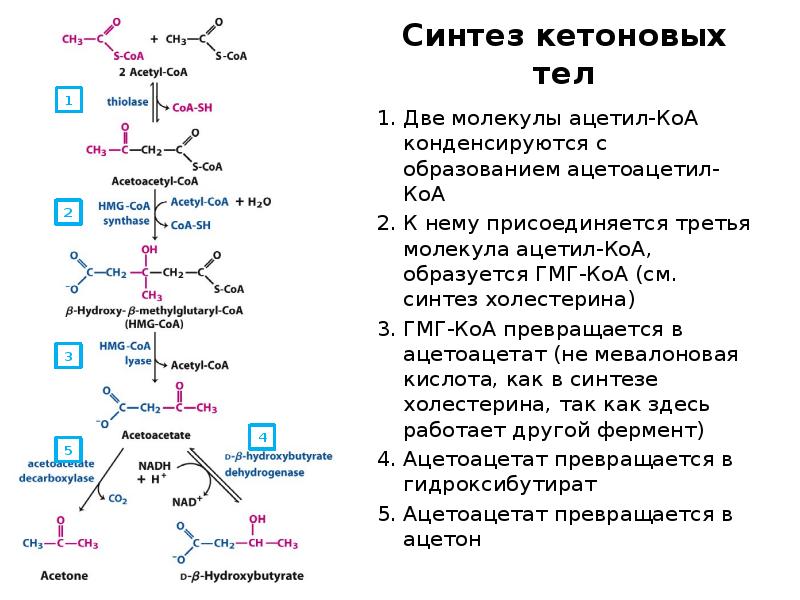
- 51. Синтез кетоновых тел Две молекулы ацетил-КоА конденсируются с образованием ацетоацетил-КоА К
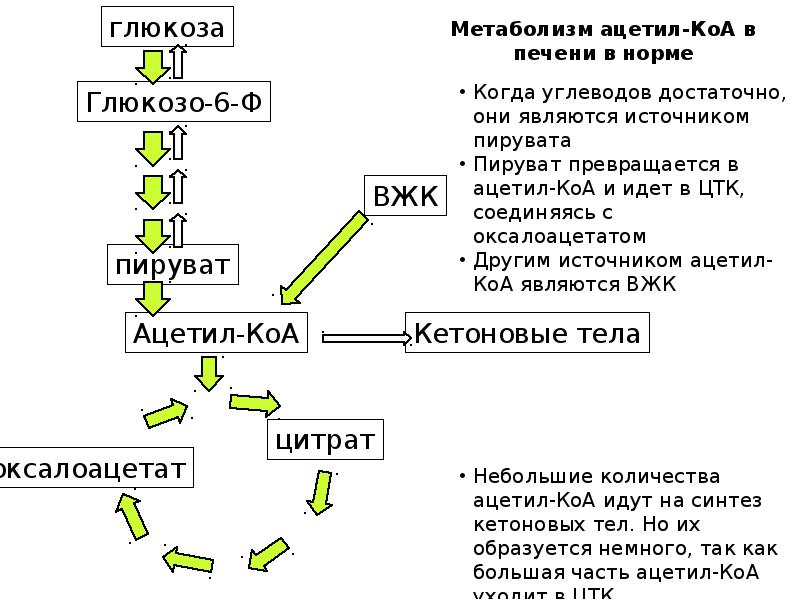
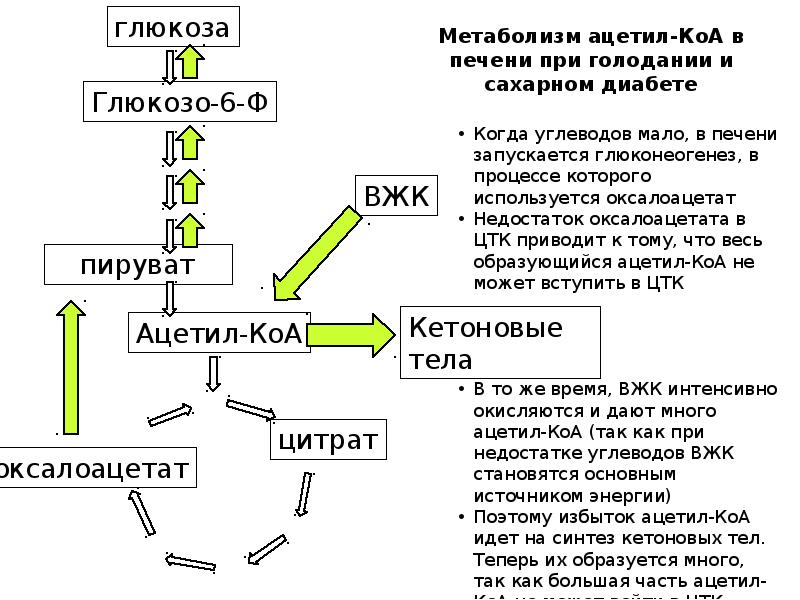
- 52. Условия образования кетоновых тел в печени Усиление β-окисления приводит к образованию
- 55. Использование кетоновых тел Из печени кетоновые тела (ацетоацетат и β-гидроксибутират) выделяются
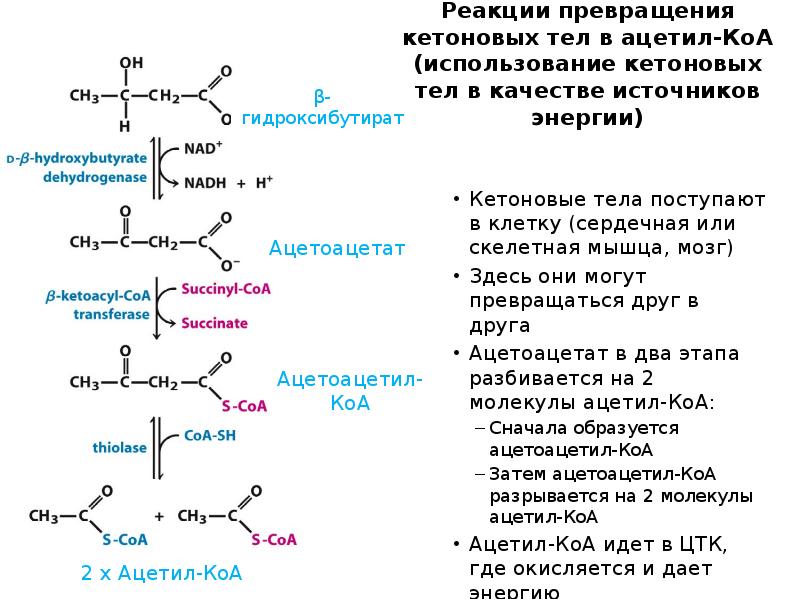
- 56. Реакции превращения кетоновых тел в ацетил-КоА (использование кетоновых тел в качестве
- 57. Синтез глицерофосфолипидов и триацилглицеролов
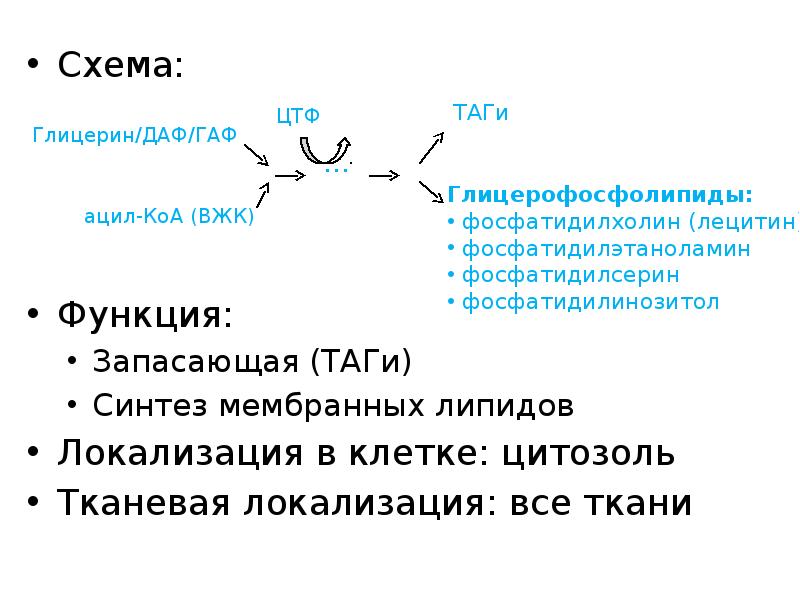
- 58. Схема: Схема: Функция: Запасающая (ТАГи) Синтез мембранных липидов Локализация в
- 59. Источники глицериновой части в молекулах глицеролипидов: Источники глицериновой части в молекулах
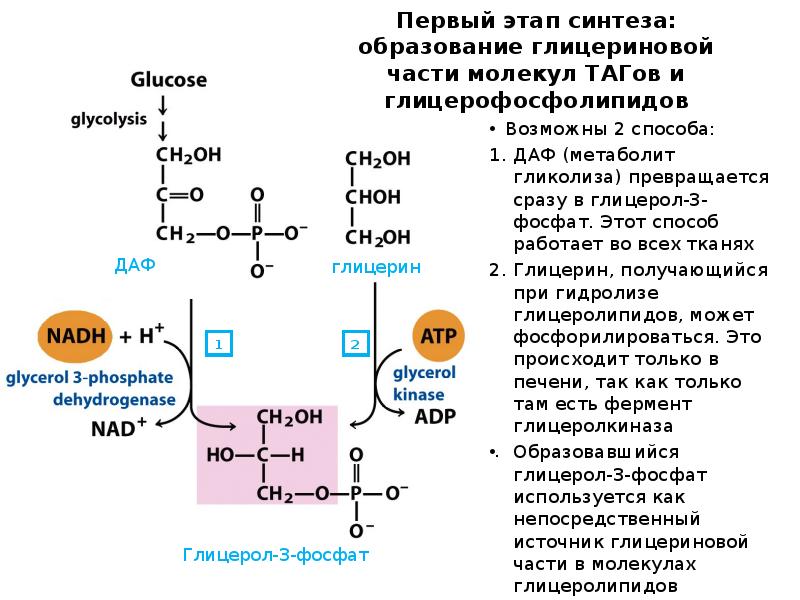
- 60. Первый этап синтеза: образование глицериновой части молекул ТАГов и глицерофосфолипидов Возможны
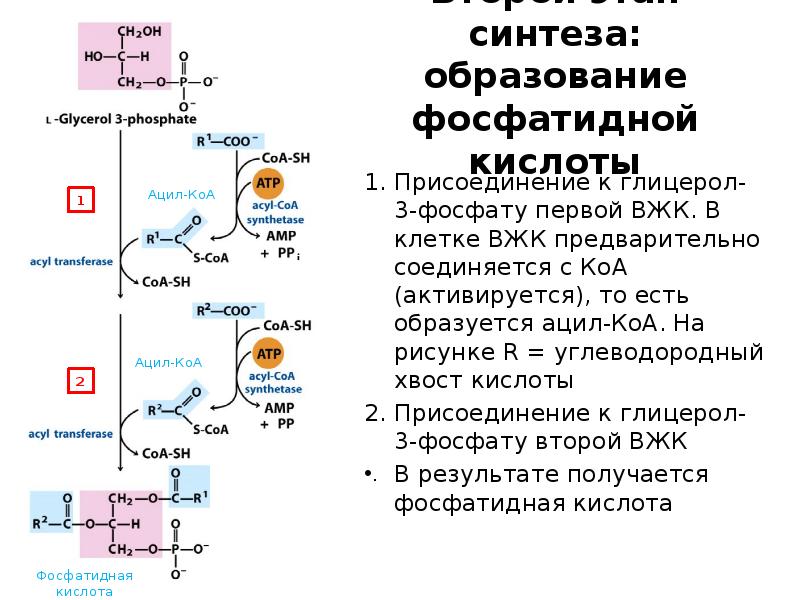
- 61. Второй этап синтеза: образование фосфатидной кислоты Присоединение к глицерол-3-фосфату первой ВЖК.
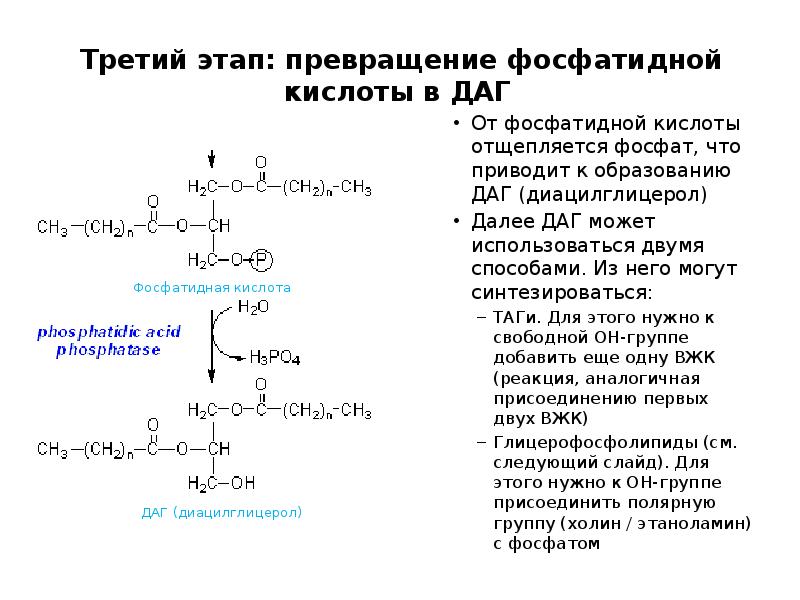
- 62. Третий этап: превращение фосфатидной кислоты в ДАГ От фосфатидной кислоты
- 63. Раздвоение метаболического пути: синтез ТАГов и глицерофосфолипидов Для того, чтобы полярная
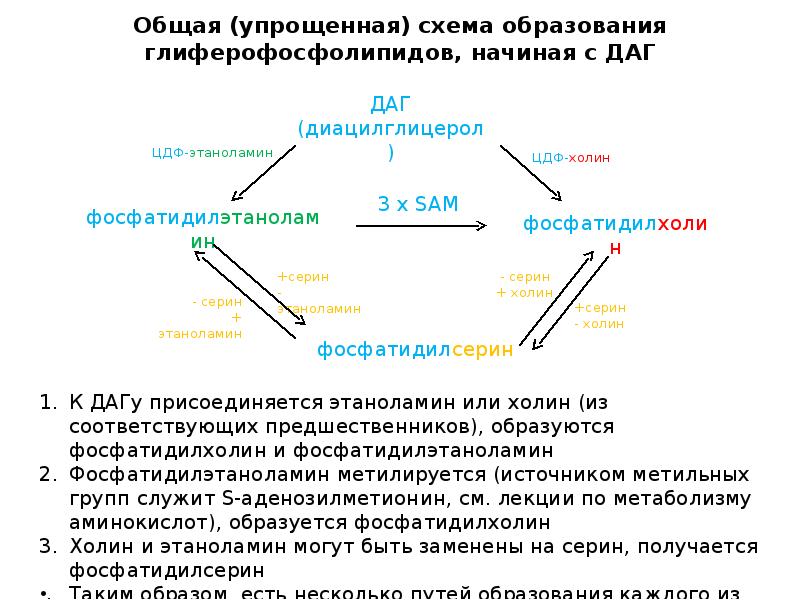
- 64. Общая (упрощенная) схема образования глиферофосфолипидов, начиная с ДАГ
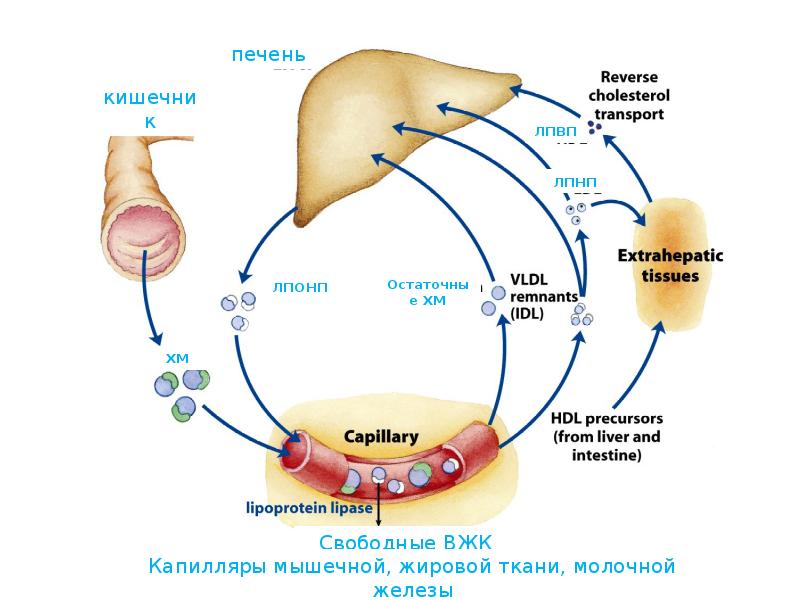
- 65. Транспорт липидов в организме
- 66. Липопротеины (ЛП) Простые липиды, например ВЖК, могут транспортироваться в крови в
- 67. Структура ЛП По форме – везикулы (пузырьки, шарики) Снаружи – оболочка
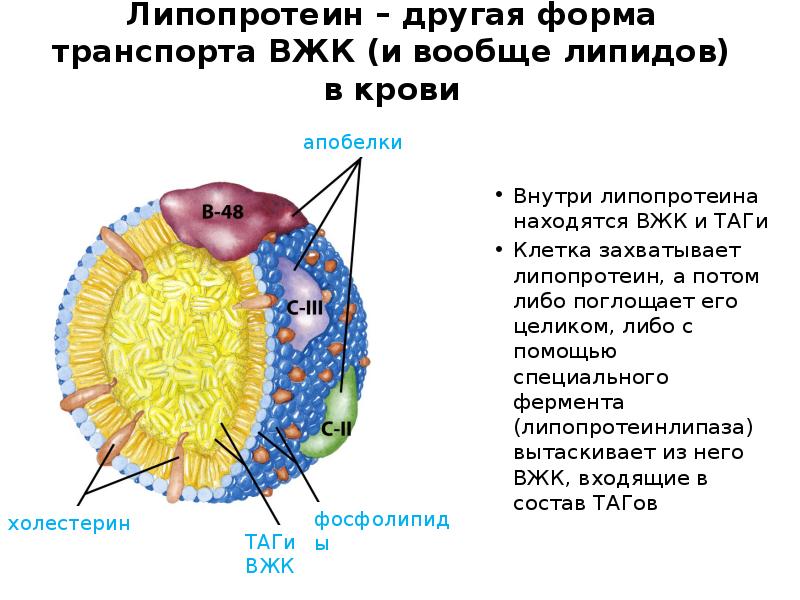
- 68. Липопротеин – другая форма транспорта ВЖК (и вообще липидов) в крови
- 69. Типы ЛП ХМ (хиломикроны): транспорт липидов из кишечника в ткани (прежде
- 71. Роль в развитии атеросклероза Атерогенные («плохой холестерин»): ЛПОНП и ЛПНП. При
- 72. эйкозаноиды
- 73. Гормоноподобные вещества, синтезируемые из арахидоновой кислоты (С20:4). В структуре есть атом
- 74. Синтез Арахидоновая кислота не содержится в клетках в свободном виде, а
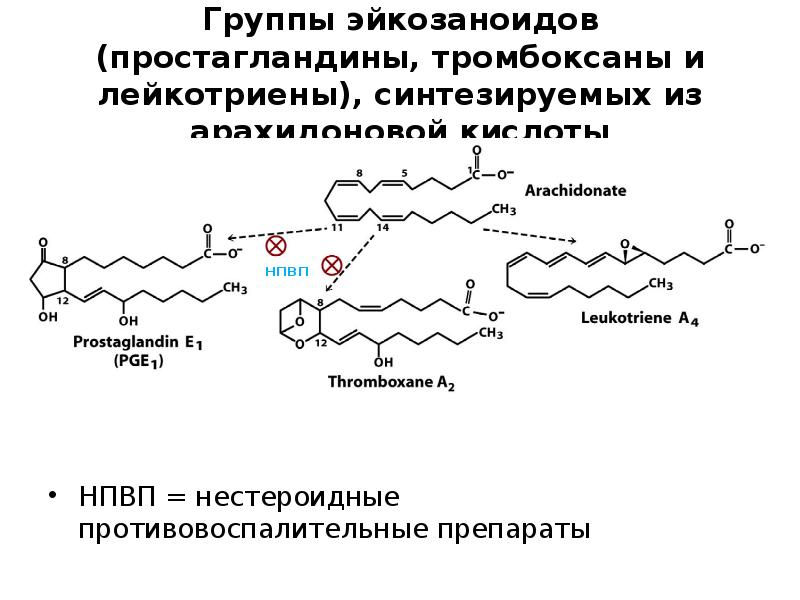
- 75. Группы эйкозаноидов (простагландины, тромбоксаны и лейкотриены), синтезируемых из арахидоновой кислоты НПВП
- 76. Скачать презентацию


































Слайды и текст этой презентации
Похожие презентации





























