Электрохимические методы анализа: Потенциометрия и полярография презентация
Содержание
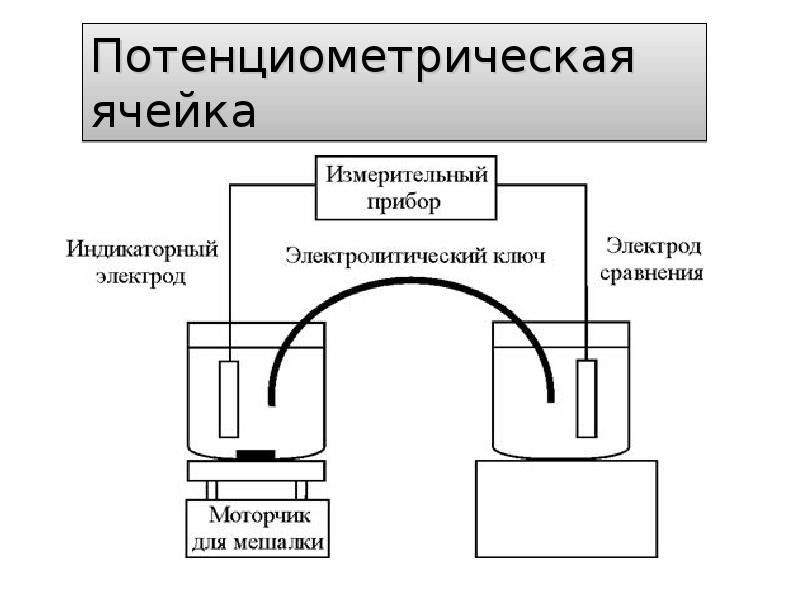
- 2. Потенциометрия Основана на измерении потенциала ячейки , т.е. разности потенциалов между
- 5. Е = (Еинд - Еср) + Еj Е = (Еинд -
- 6. Электрод первого рода – металл, погруженный в раствор соли этого же
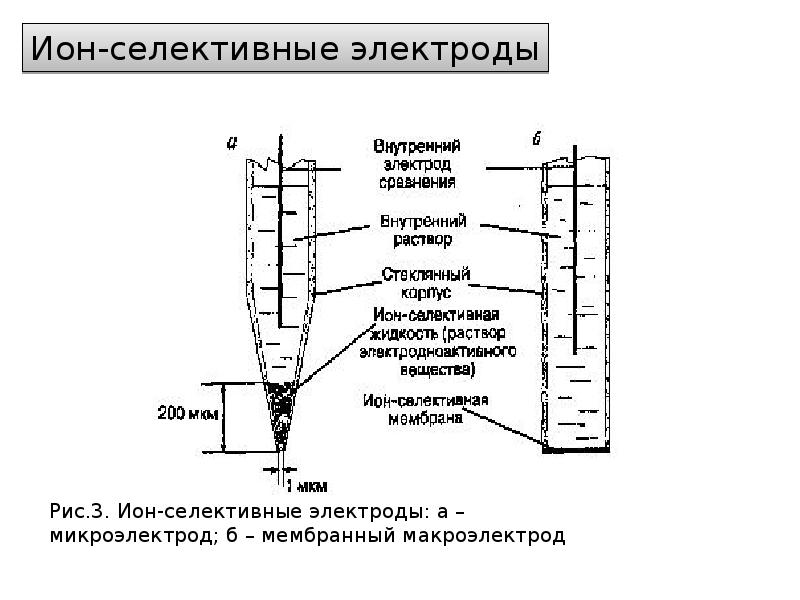
- 7. 1) Классические электроды: Класс 0. Инертные металлы; Класс 1. Обратимые: металл
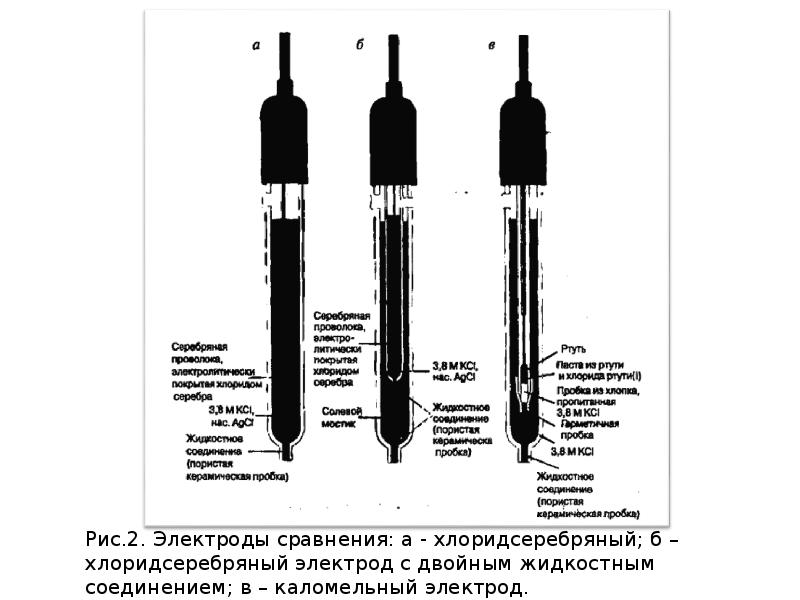
- 9. Хлоридсеребряный электрод (Ag│AgСl, KCl) AgСl (тв.) + е ↔ Ag(тв.) +
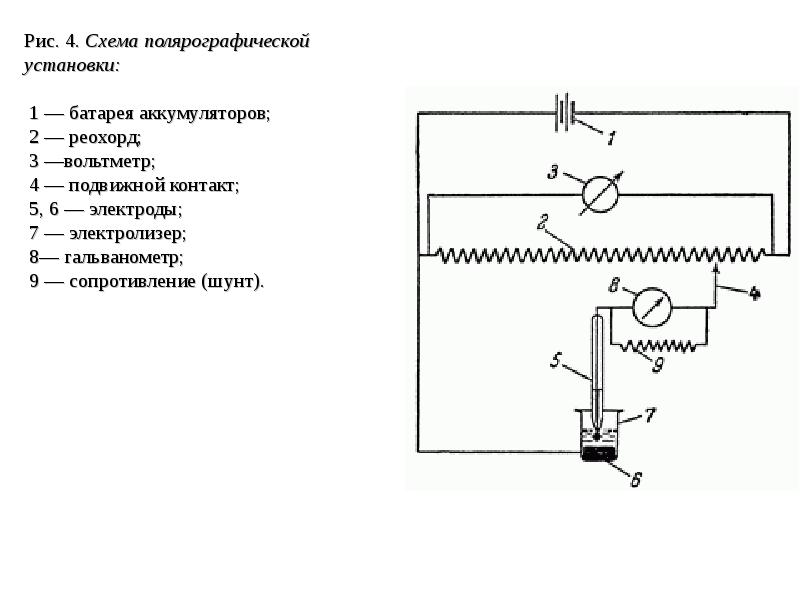
- 20. Особенности метода: Особенности метода: Быстрота аналитического определения, не превышающая
- 28. Скачать презентацию



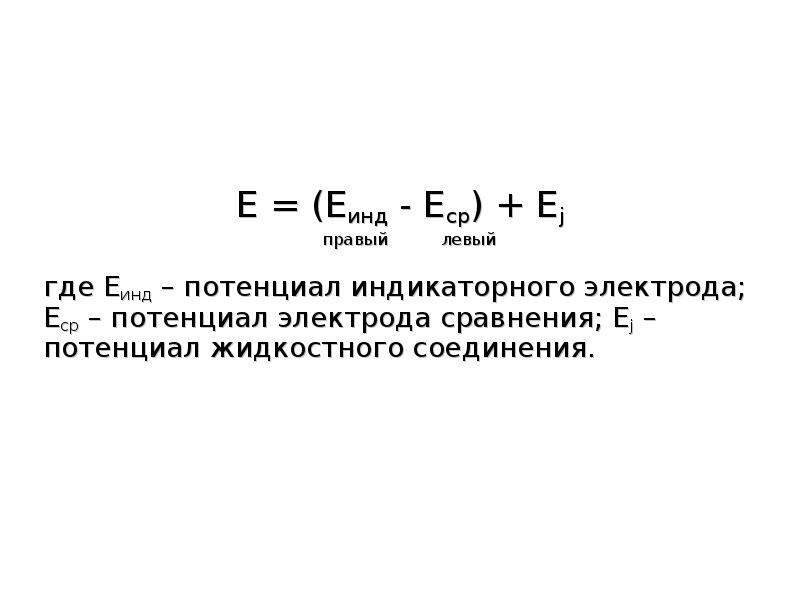







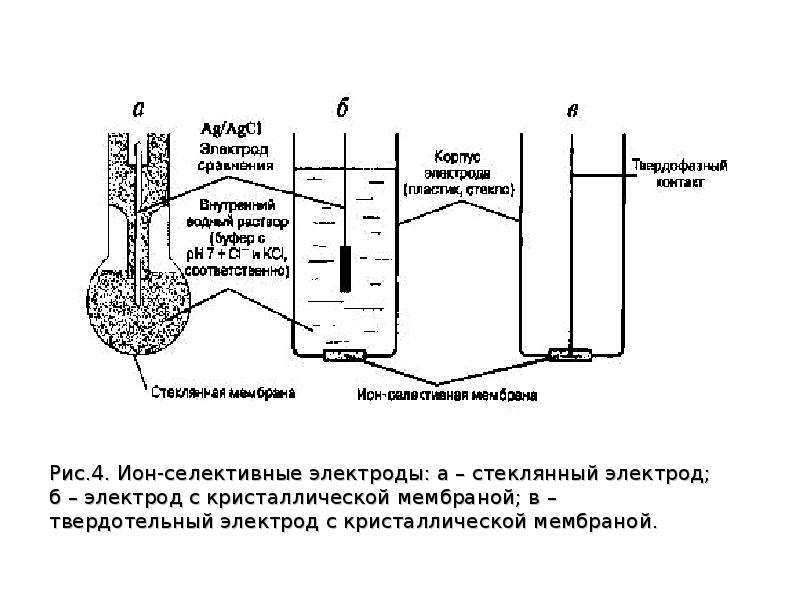
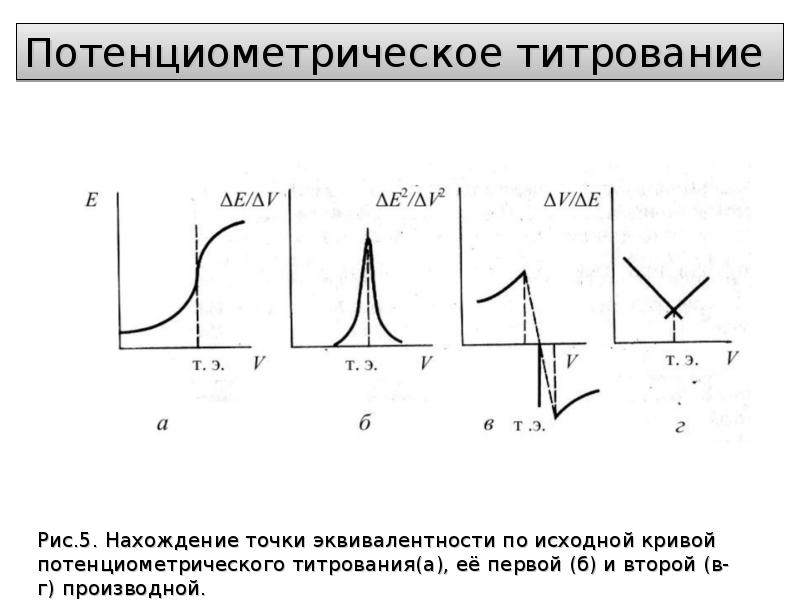




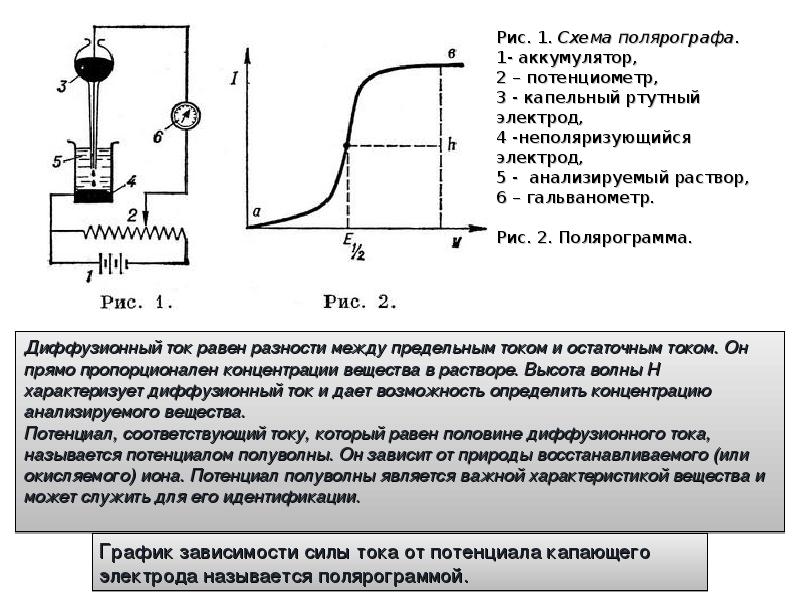
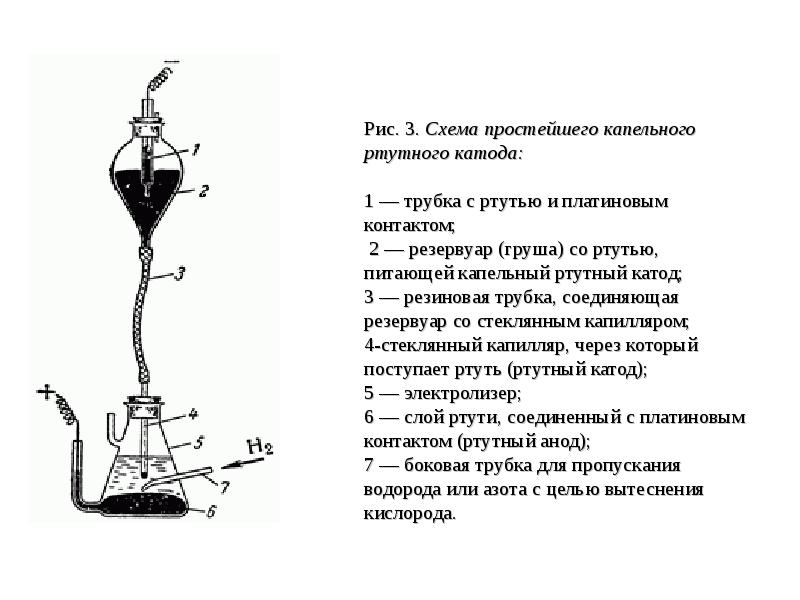




Слайды и текст этой презентации
Скачать презентацию на тему Электрохимические методы анализа: Потенциометрия и полярография можно ниже:
Похожие презентации





























