Опыты Резерфорда (9 класс) презентация
Содержание
- 2. Эрнест Резерфорд (Rutherford Ernst) 30.08.1871-19.10.1937 – английский физик, основоположник ядерной физики.
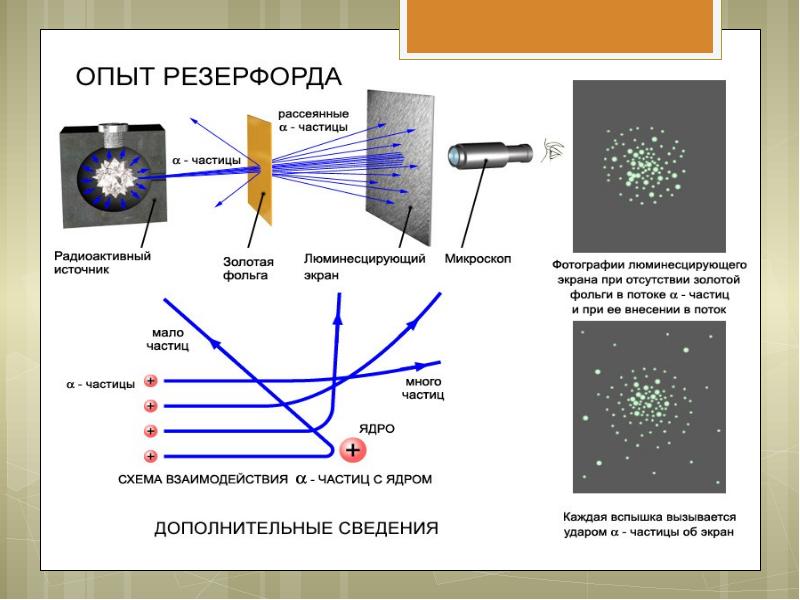
- 3. Опыт Резерфорда. Модель строения атома Томсона нуждалась в экспериментальной проверке.
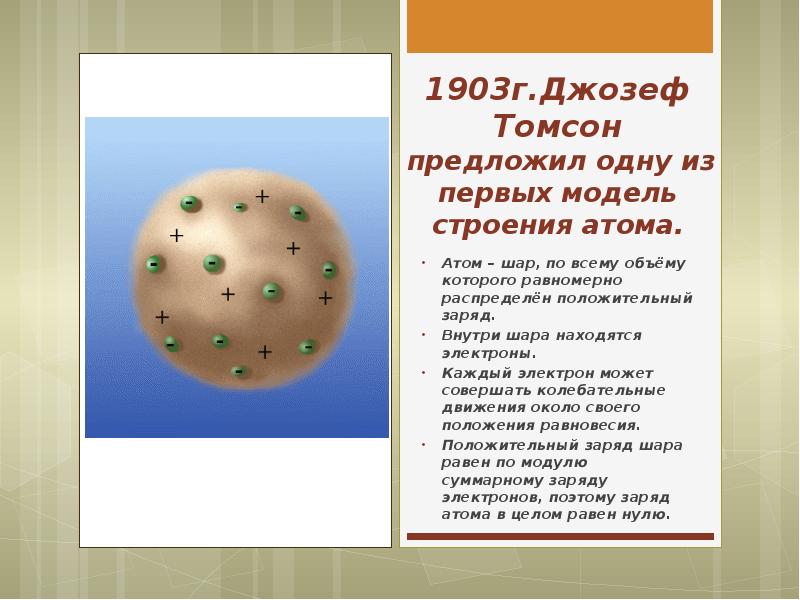
- 4. 1903г.Джозеф Томсон предложил одну из первых модель строения атома. Атом –
- 5. Идея опыта Резерфорда: Зондировать атом альфа–частицами. Альфа-частицы возникают при распаде радия.
- 7. В ходе эксперимента обнаружили: 1. В отсутствии фольги – на экране
- 8. Выводы из опыта Резерфорда
- 9. Выводы из опыта Резерфорда
- 10. Модель атома Резерфорда Резерфорд предложил ядерную («планетарную») модель атома: *
- 11. Скачать презентацию








Слайды и текст этой презентации
Похожие презентации





























