Тотығу-тотықсыздану реакциялары (1) презентация
Содержание
- 2. Сабақтың тақырыбы: § 64 Тотығу дәрежесі. Тотығу-тотықсыздану реакциялары. Сабақтың мақсаты:
- 3. Сабақтың жоспары: І. Ұйымдастыру кезеңі. Сабақтың жоспары: І. Ұйымдастыру кезеңі.
- 4. «Ой толғау»: 1. Электртерістілік деген не? 2. Тотығу дәрежесі деген
- 5. «Кім жылдам?» 1. Тотығу дәрежесі +4 ке тең а)
- 6. Жауаптары: 1.а, 2.ә, 3ә, 4.а, 5.б. Жауаптары: 1.а, 2.ә, 3ә, 4.а,
- 7. «Кім алғыр» №1 Мына қосылыстарды қай элементтің тотығу дәрежесі нольге
- 8. Қатесін тап а) ?-3 H3+1 ә) Ca3+2 P?-3 б) Ca?
- 9. Сабақтың тақырыбы: § 64 Тотығу дәрежесі. Тотығу-тотықсыздану реакциялары. ІІІ.
- 11. Электрондар беру процесі – тотығу, ал қосып алу процесі тотықсыздану деп
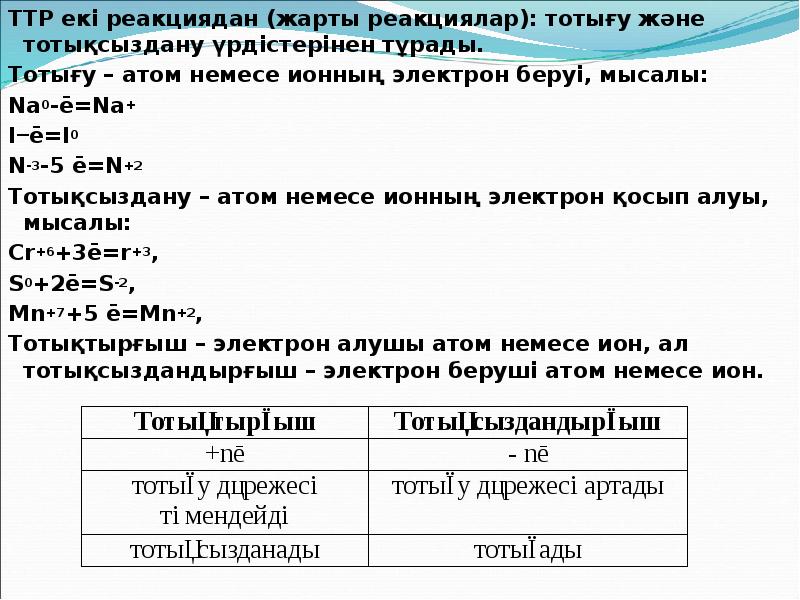
- 12. ТТР екі реакциядан (жарты реакциялар): тотығу және тотықсыздану үрдістерінен тұрады. ТТР
- 13. Ең маңызды тотықтырғыштар: күштілері – F2, O2, O3, H2O2, Cl2 (әсіресе
- 14. ТТР теңдеулерін құрастыру, яғни реакция өнімдерін анықтау және стехиометриялық коэффициенттерді табу
- 17. ТТР теңдеулері күрделірек болғанда мына реттілікті қолдану.
- 18. 4. Электрондық теңдеудің қасына тік сызық сызып, оның сыртына электрондардың алдында
- 19. ТТР-ның маңызы: ТТР-ның маңызы: ТТР өндірісте, тұрмыста жүзеге асып жататын процестер:
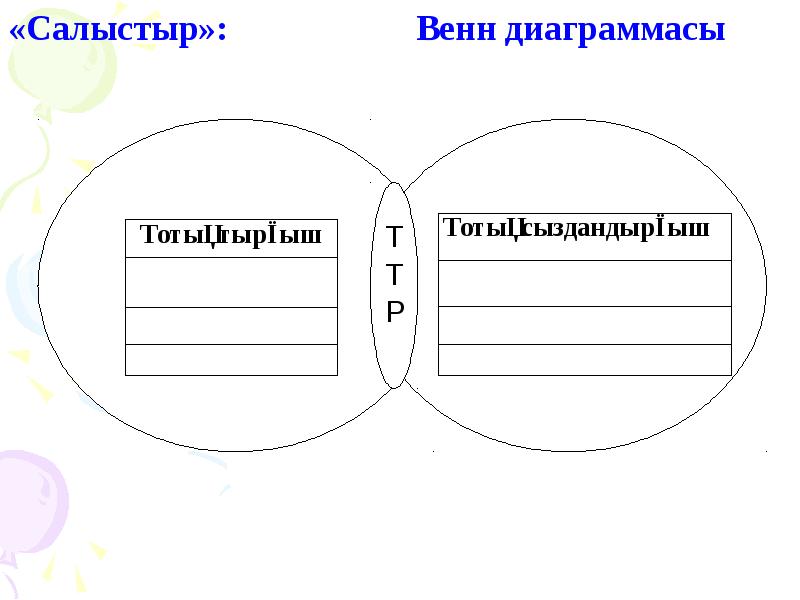
- 22. «Салыстыр»: Венн диаграммасы «Салыстыр»:
- 23. IV. Бекіту: “Кім тапқыр!” Төмендегі теңдеуде қандай элемент топтарының
- 24. Жауаптар: 1)б, 2)в, 3)а, 4)а, 5)ә Жауаптар: 1)б, 2)в, 3)а, 4)а,
- 25. Ойлан тап! (Химиялық терминдермен жұмыс) Тотығу – Тотықсыздану –
- 26. №5 жаттығу №5 жаттығу а) Алюминийдің оттекпен; б) Темірдің хлормен; в)
- 27. а) 4Al0+3O20 →2Al2+3O3-2 а) 4Al0+3O20 →2Al2+3O3-2 Al0 - 3e
- 28. VІ. Оқушыларды бағалау. VІ. Оқушыларды бағалау. V. Үйге тапсырма беру: §64
- 29. Скачать презентацию

























Слайды и текст этой презентации
Скачать презентацию на тему Тотығу-тотықсыздану реакциялары (1) можно ниже:
Похожие презентации





























