140 лет дому, который построил Д.И. Менделеев презентация
Содержание
- 2. Цели урока: Методическая цель: «Развитие познавательной деятельности и познавательной активности
- 3. Структура урока Тип урока - комбинированный. Принципы обучения - сознательности,
- 4. План-структура урока 1. Организационный момент 2. Актуализация опорных знаний 2.1. Написать
- 5. Актуализация опорных знаний Вариант 1 К + Н2О = СаО
- 6. Предпосылки создания периодического закона 1. К середине XIX века было
- 7. Антуан Лавуазье Французский химик, с 1772 г. член Парижской АН. Родился
- 8. Деберейнер Иоганн Вольфганг (1780-1849) Немецкий химик. Родился в Хофе. Учился самостоятельно.
- 9. Вариант И. Деберейнера (Закон триад) Натрий Na - 23,00 Калий K
- 10. УИЛЬЯМ ОДЛИНГ Английский химик, член Лондонского королевского общества. Основные работы посвящены
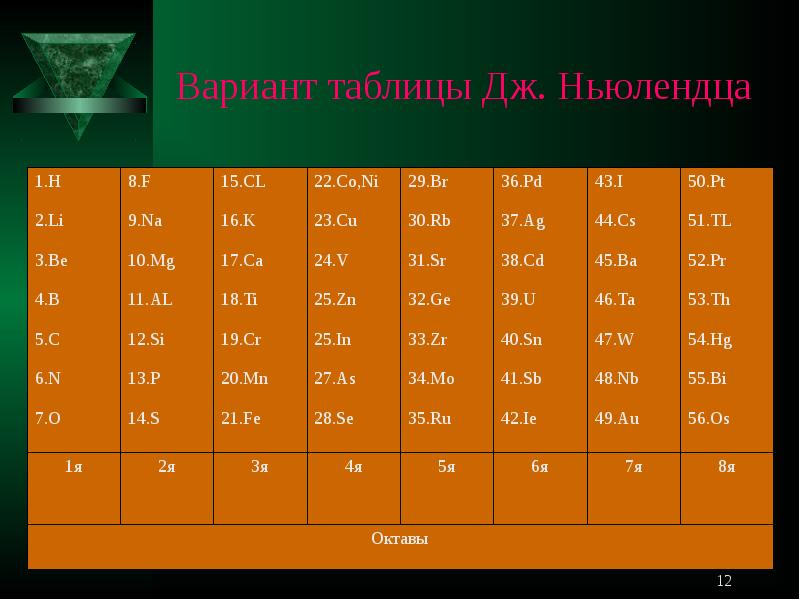
- 11. ДЖОН НЬЮЛЕНДС В статье, датированной 20 августа 1864 г., он отметил, что
- 12. Вариант таблицы Дж. Ньюлендца
- 13. Мейер Лотар Немецкий химик, с 1888 г. член - корреспондент Берлинской
- 14. Вариант Лотара Мейера
- 15. Менделеев Дмитрий Иванович (1834-1907) Русский ученый-энциклопедист, с 1876 г. член-корреспондент Петербургской
- 17. ЛЕКОК ДЕ БУОБОДРАН, ЛАРС ФРЕДЕРИК НИЛЬСОН, КЛИМЕНС ВИНКЛЕР– утвердители Периодического закона
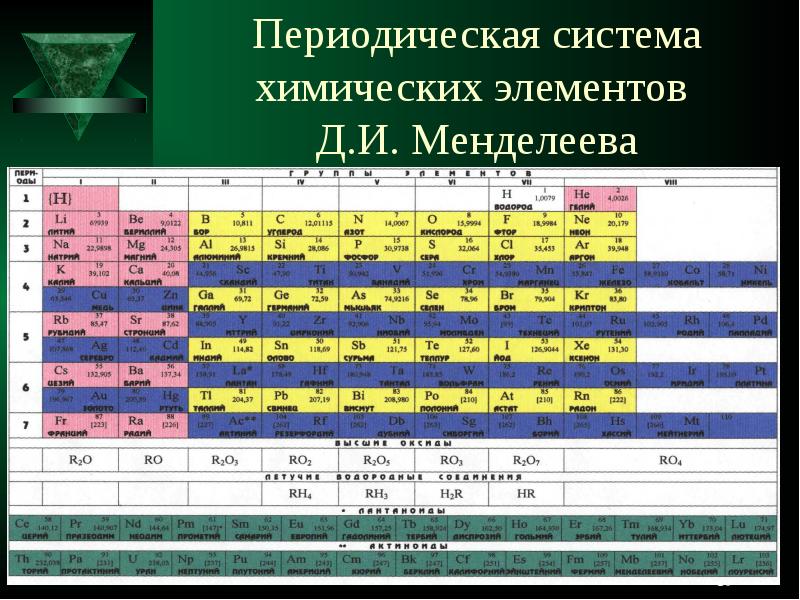
- 18. Периодическая система химических элементов Д.И. Менделеева
- 19. Структура периодической системы: Формулировка периодического закона «Свойства простых тел находятся
- 20. Структура периодической системы: Понятие группы А) Группа – это расположение элементов
- 21. Химическая викторина 1. Какой химический элемент сначала обнаружили на Солнце потом
- 22. Химический кроссворд
- 23. Александр Блок видел в Дмитрии Ивановиче воплощение гения России. Периодическая система
- 24. Заключительное слово преподавателя «Труд, работа не всякая, а осмысленная, сознательная,
- 25. Скачать презентацию






















Слайды и текст этой презентации
Скачать презентацию на тему 140 лет дому, который построил Д.И. Менделеев можно ниже:
Похожие презентации





























