Идеальные растворы. Законы Дальтона и Рауля презентация
Содержание
- 2. Модельная система: идеальный жидкий бинарный раствор в равновесии с собственным паром.
- 3. В идеальных растворах стремление к переходу в газовую фазу одинаково для
- 4. Если оба компонента идеального раствора летучи, то закон Рауля выполняется для
- 6. Предельно (бесконечно) разбавленные растворы. Закон Генри. В предельно разбавленных растворах к
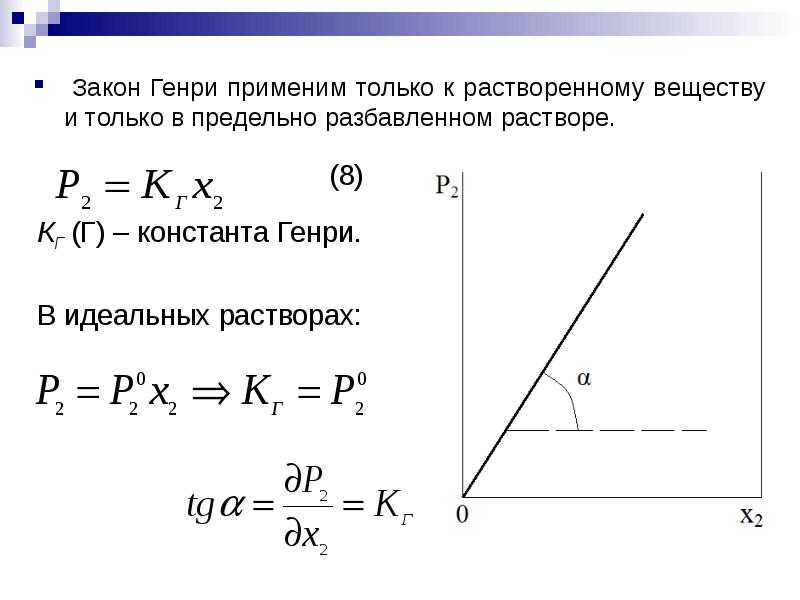
- 7. Закон Генри применим только к растворенному веществу и только в предельно
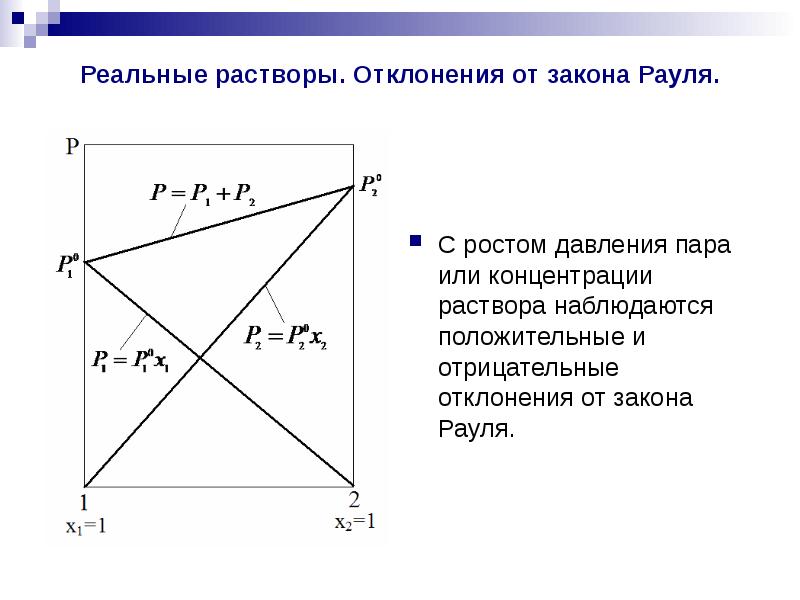
- 8. Реальные растворы. Отклонения от закона Рауля. С ростом давления пара или
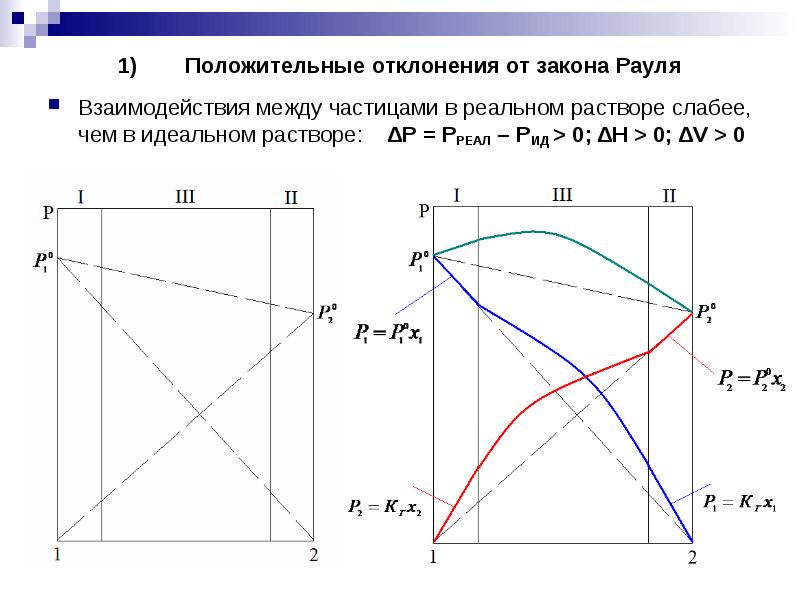
- 9. Положительные отклонения от закона Рауля Взаимодействия между частицами в реальном растворе
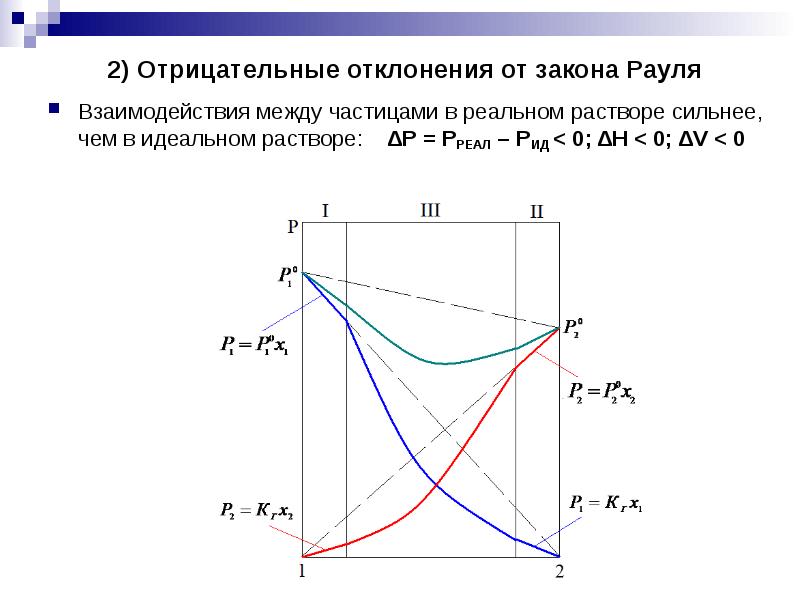
- 10. 2) Отрицательные отклонения от закона Рауля Взаимодействия между частицами в реальном
- 11. Термодинамика реальных растворов. Активность и коэффициент активности Для описания свойств реальных
- 12. Активность (аi) – эффективная или реально действующая концентрация компонента в растворе
- 13. Активность – гипотетическая величина, которая при подстановке вместо концентрации в уравнения
- 15. Скачать презентацию










Слайды и текст этой презентации
Скачать презентацию на тему Идеальные растворы. Законы Дальтона и Рауля можно ниже:
Похожие презентации





























