Карбоновые кислоты. (10 класс) презентация
Содержание
- 2. Карбоновые кислоты Карбоновые кислоты
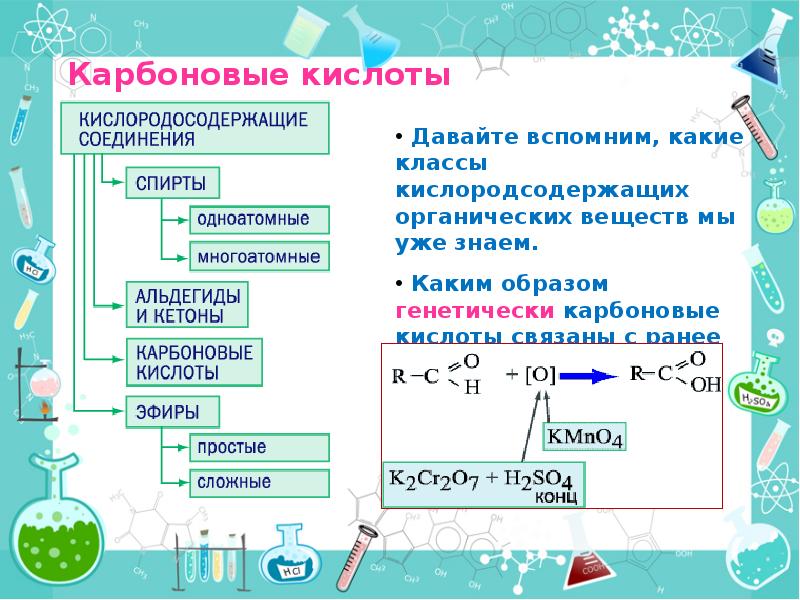
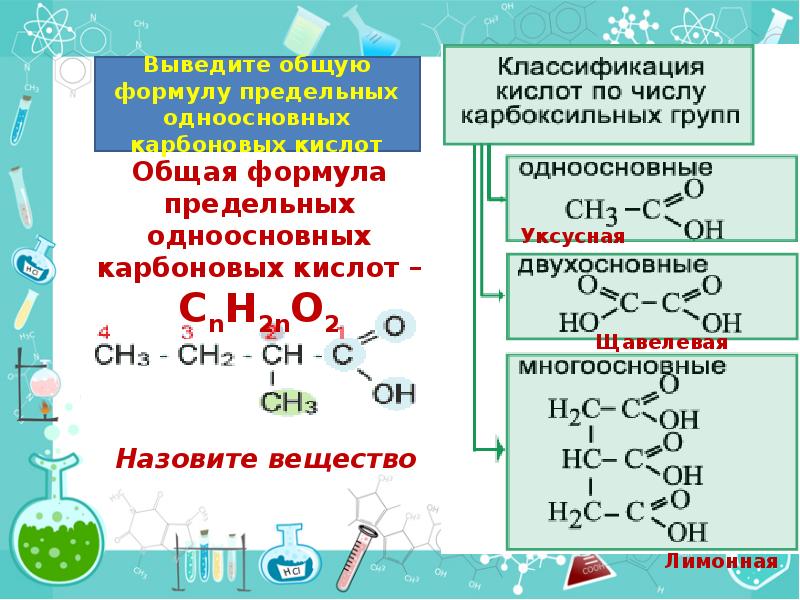
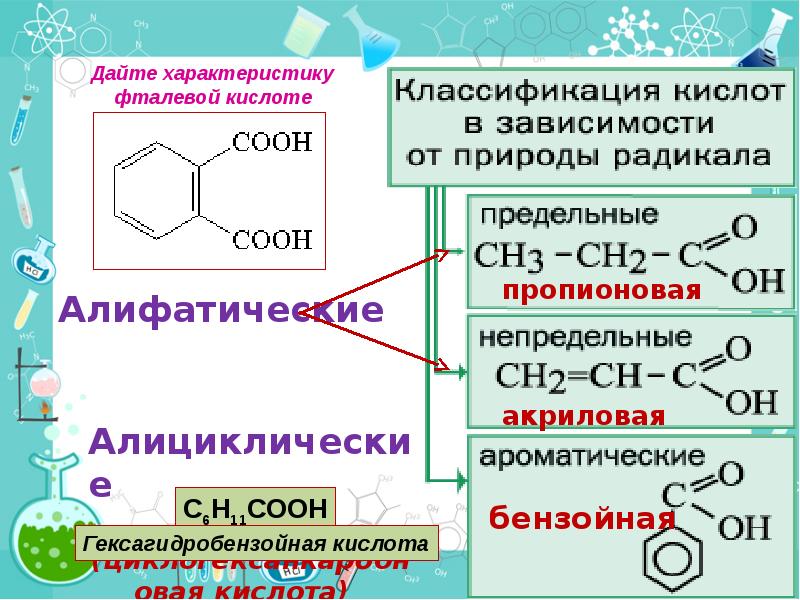
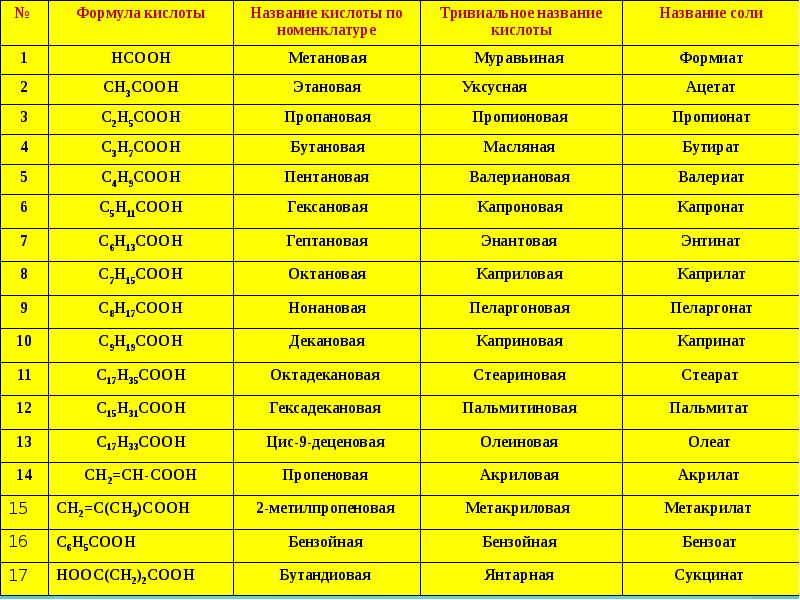
- 3. Что мы узнаем на этом уроке 1.Определение карбоновых кислот 2. Классификация
- 4. Историческая справка С древнейших времен использовали уксус, образующийся при скисании вина,
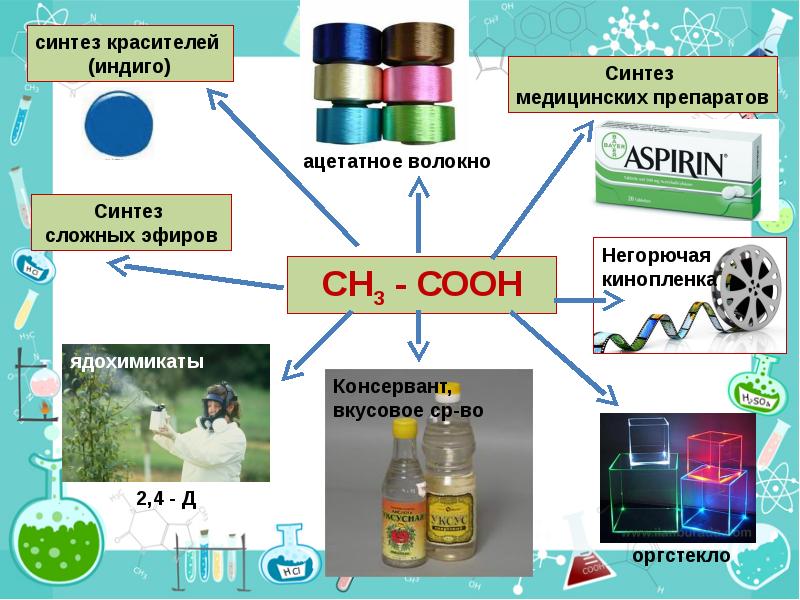
- 5. Кто получил кислоты? Уксусная кислота СН3СООН –
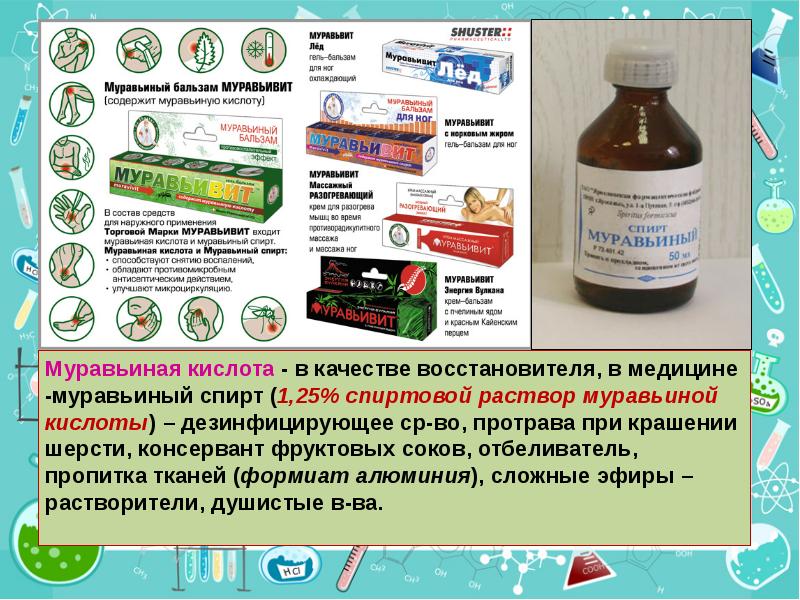
- 6. Муравьиная кислота 16 век – обнаружено, что «кислый пар» из муравейников
- 7. Карл Вильгельм Шееле Конец 18 века – выделил и описал лимонную,
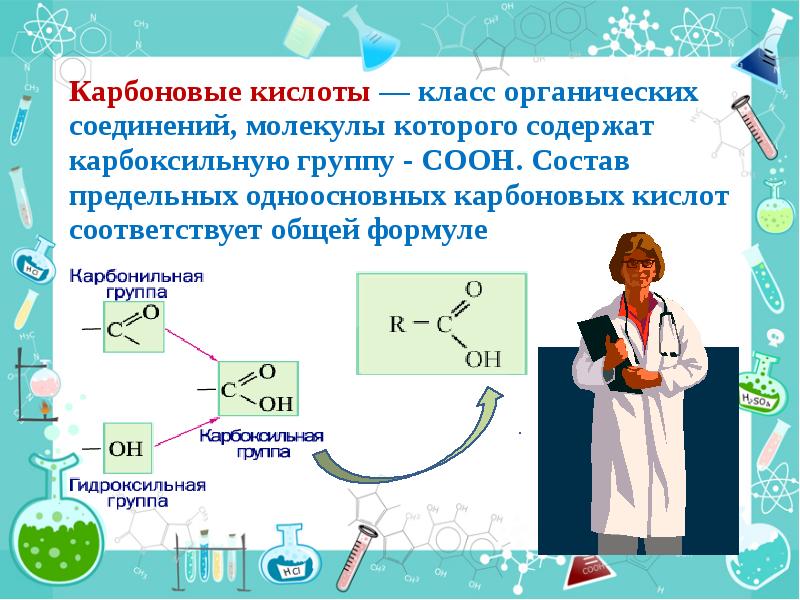
- 8. Карбоновые кислоты — класс органических соединений, молекулы которого содержат карбоксильную группу
- 15. Изомерия 1.Изомерия углеродной цепи Составьте изомеры по углеродному скелету для
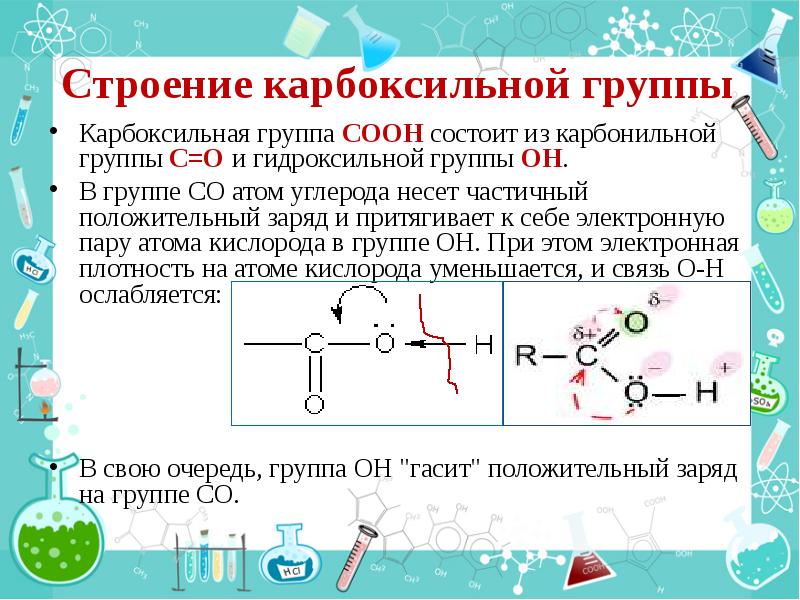
- 16. Строение карбоксильной группы Карбоксильная группа СООН состоит из карбонильной группы С=О
- 18. Физические свойства Низшие карбоновые кислоты — жидкости с острым запахом, хорошо
- 19. Возгонка – переход вещества из твердого состояния в газообразное, минуя жидкое
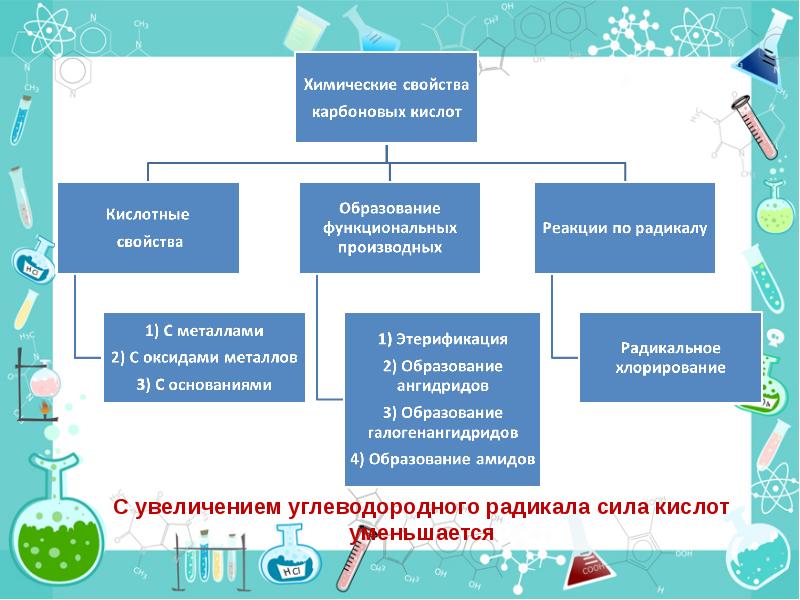
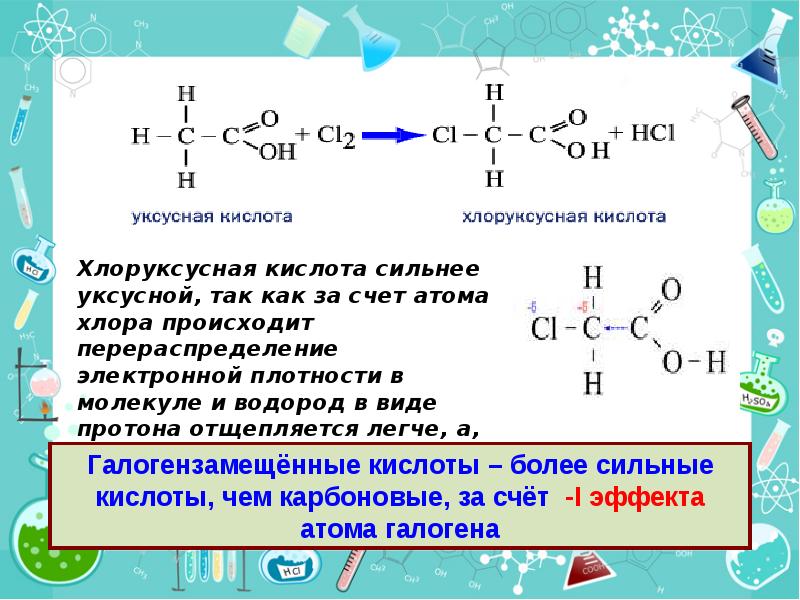
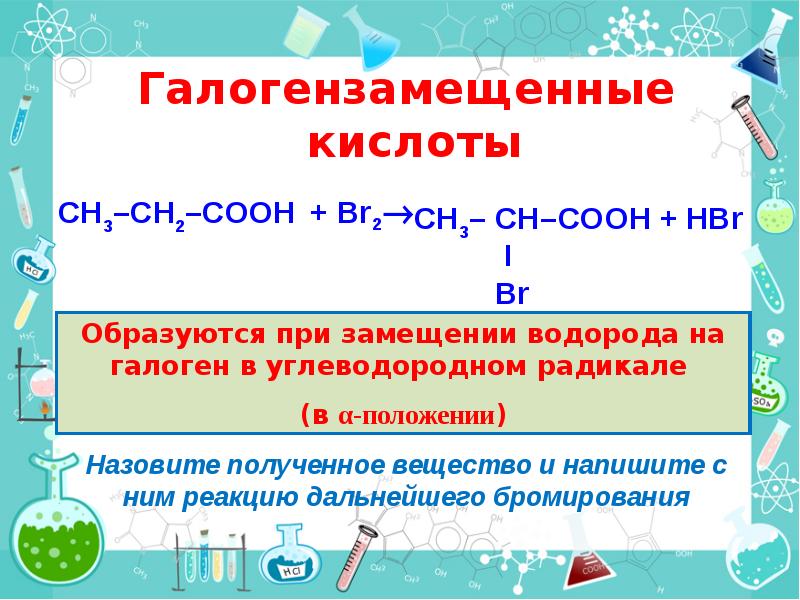
- 29. Галогензамещенные кислоты
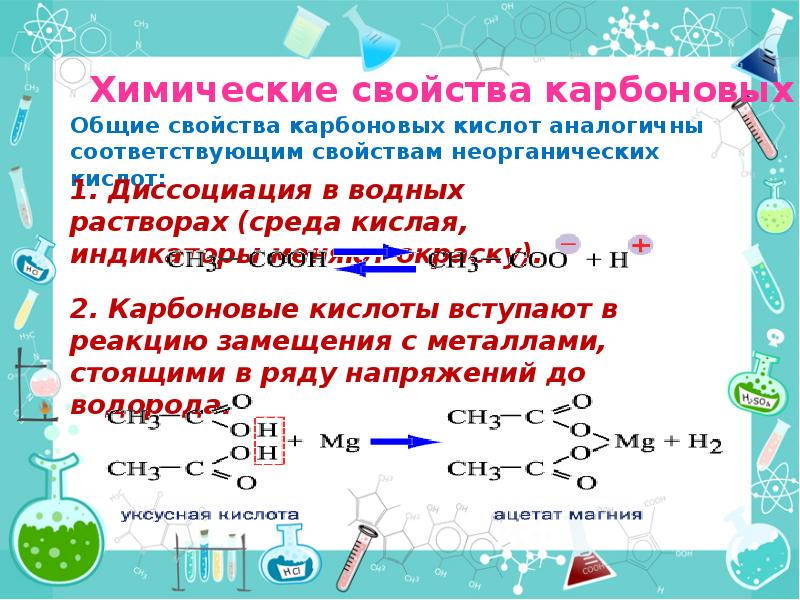
- 30. Примеры химических реакций для уксусной кислоты CH3COOH Zn + 2CH3COOH
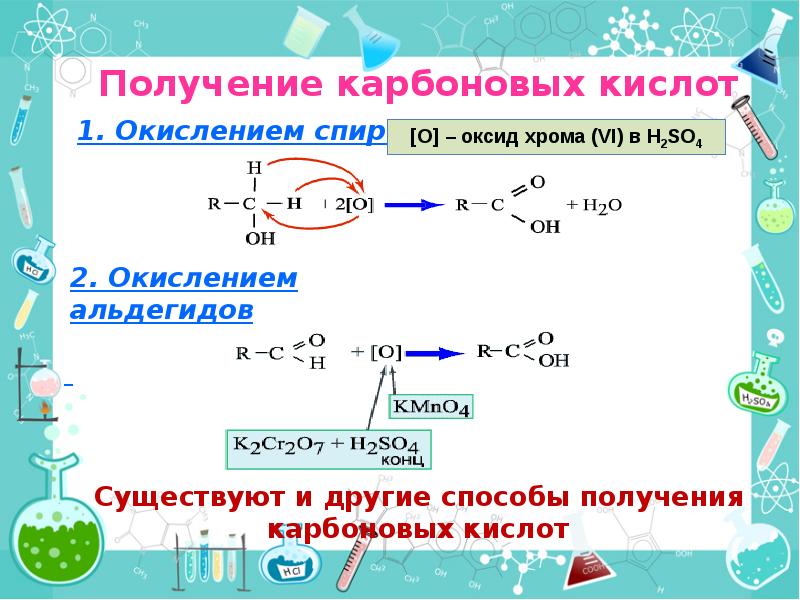
- 32. Получение карбоновых кислот 3. Окислением углеводородов Практическое значение
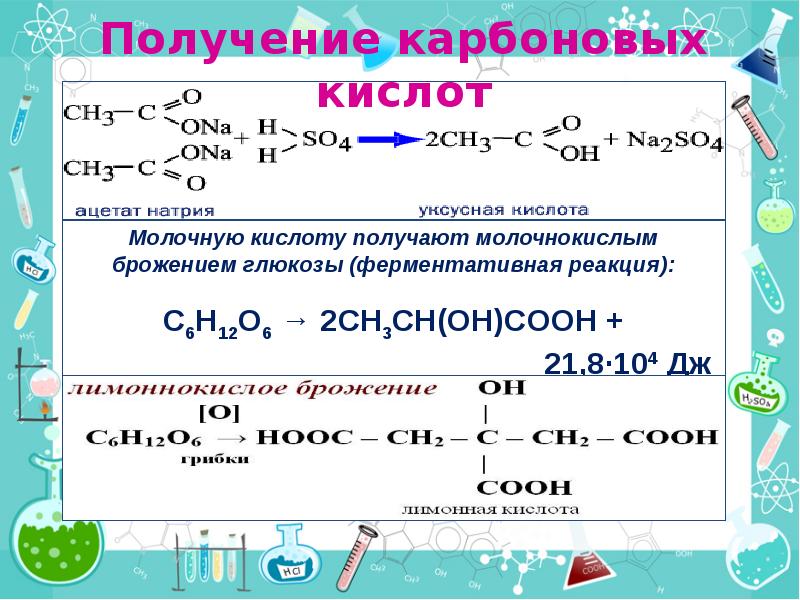
- 34. Специфические способы получения отдельных кислот
- 35. Получение карбоновых кислот
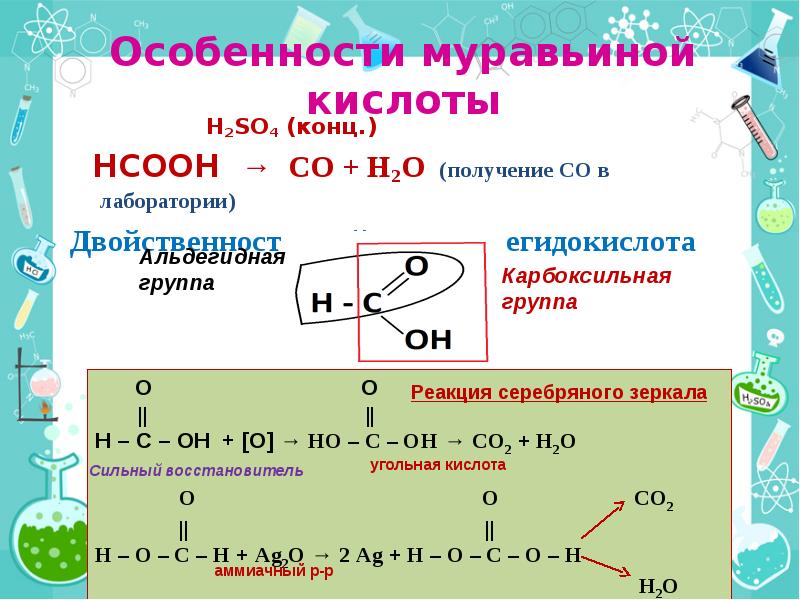
- 36. Особенности муравьиной кислоты H2SO4 (конц.) HCOOH → CO
- 39. Акриловая и метакриловая кислоты являются непредельными карбоновыми кислотами и проявляют свойства
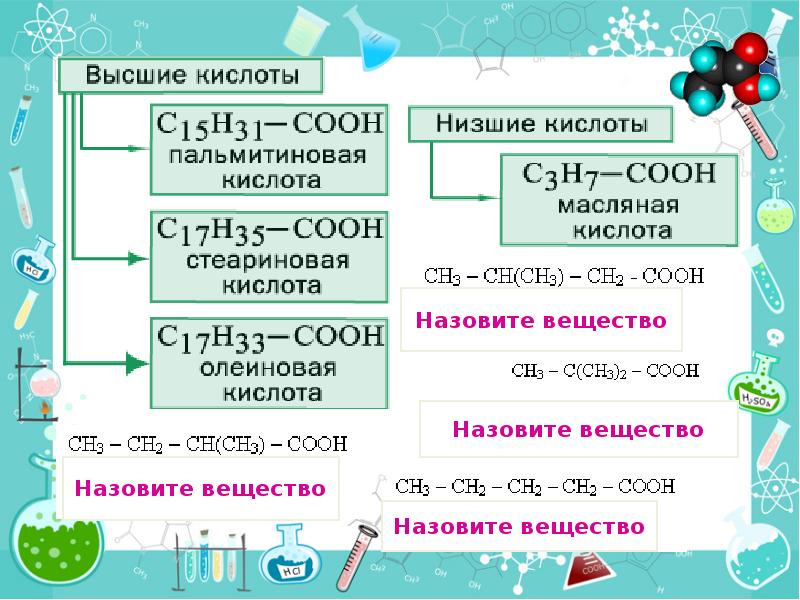
- 40. Высшие карбоновые кислоты Число атомов С – больше 10 Обычно имеют
- 41. Высшие карбоновые кислоты Высшие непредельные карбоновые кислоты: С17Н33СООН – олеиновая (1
- 42. Стеариновая кислота и ее соли стеараты С17Н35СООН относится к высшим карбоновым
- 43. Бензойная кислота С6Н5-СООН, в составе природных смол, в плодах, ягодах, сильнее
- 44. Щавелевая кислота НООС-СООН – двухосновная кислота, содержится в листьях щавеля, ревеня,
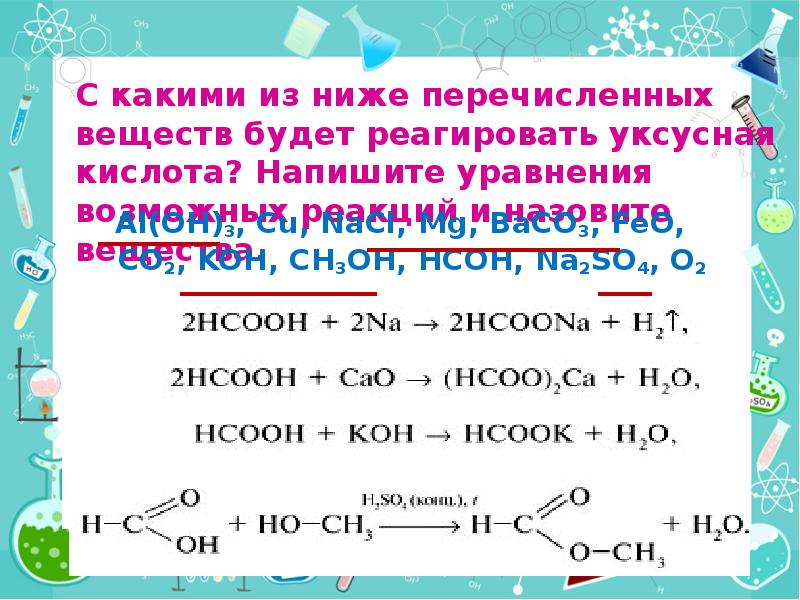
- 51. С какими из ниже перечисленных веществ будет реагировать уксусная кислота? Напишите
- 52. Задания Расположите в ряд по усилению кислотных свойств перечисленные кислоты
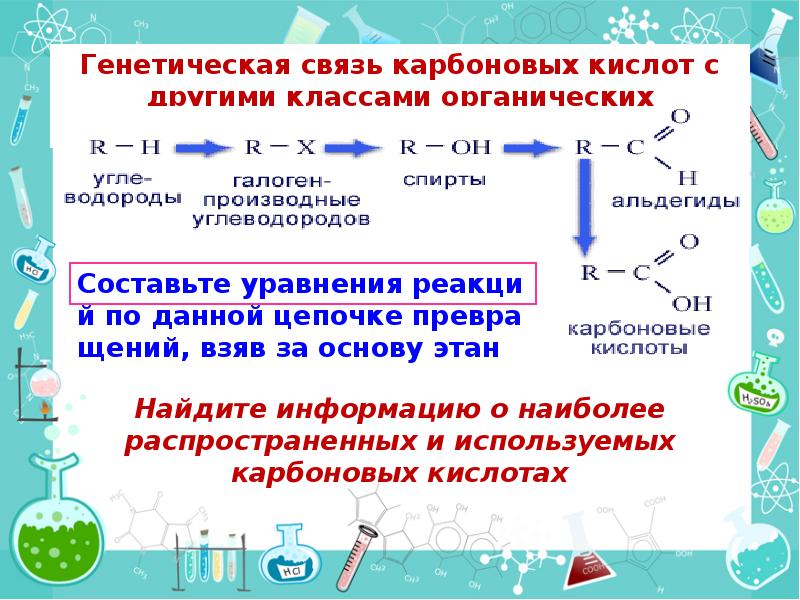
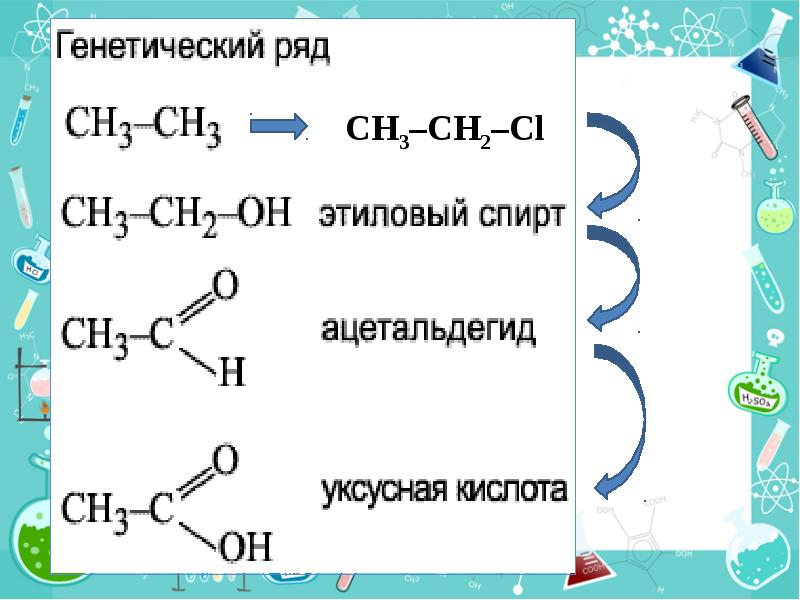
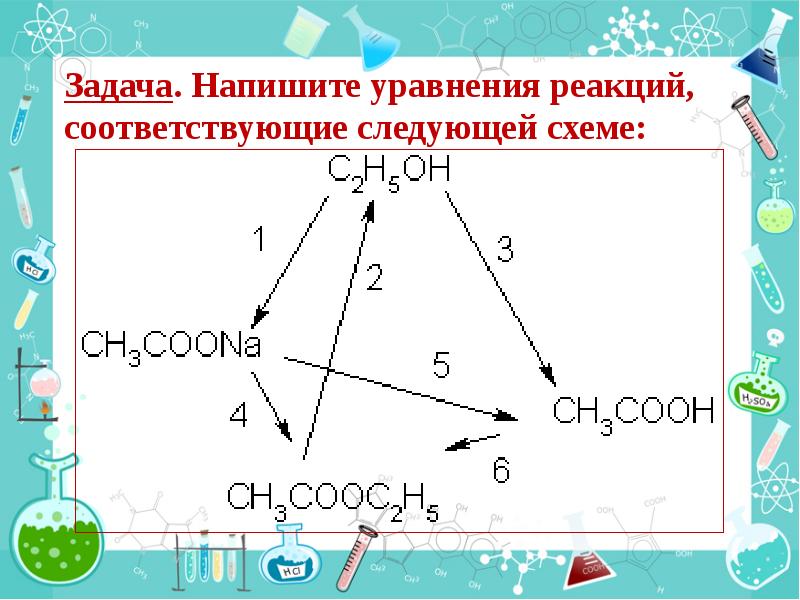
- 53. Задача. Напишите уравнения реакций, соответствующие следующей схеме:
- 59. Скачать презентацию


































Слайды и текст этой презентации
Похожие презентации





























