Органическая химия. Подготовка к контрольной работе № 2 презентация
Содержание
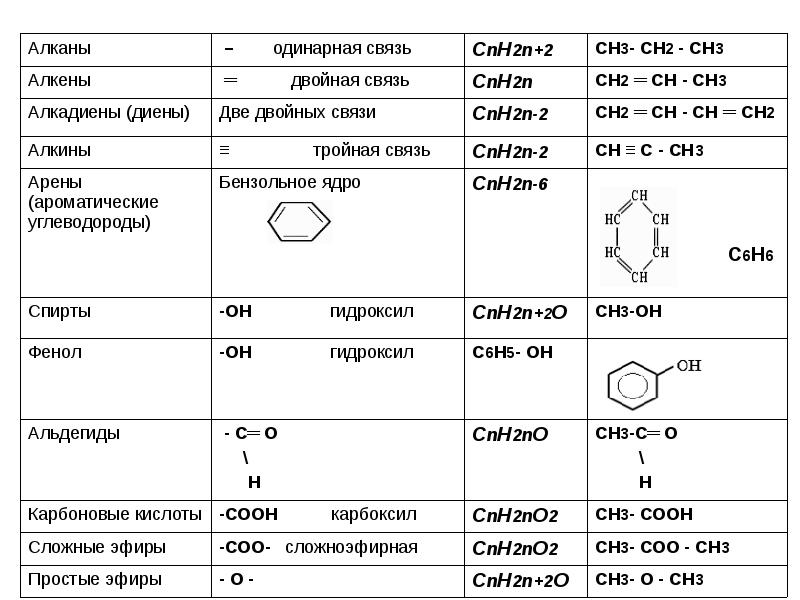
- 3. Гомологи – вещества одного класса (схожее строение и свойства), различающиеся по
- 4. Названия органических веществ строятся от названий алканов с тем же числом
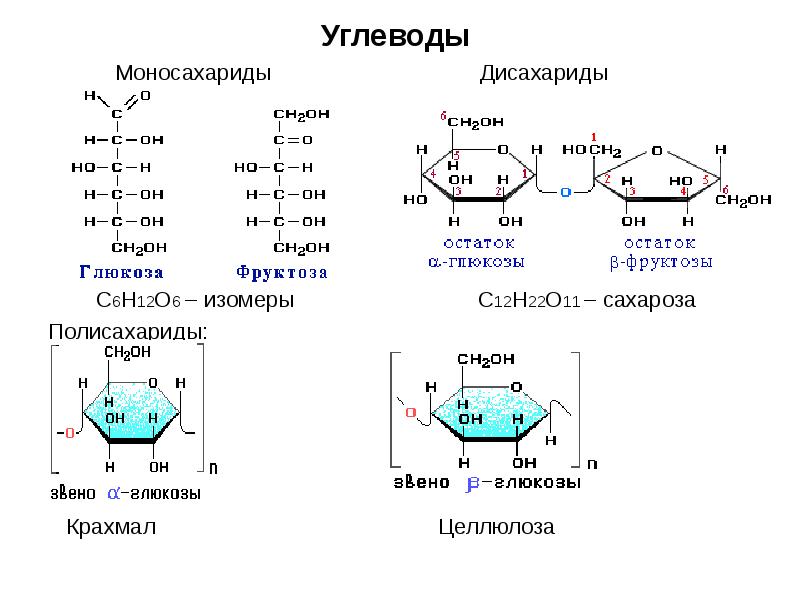
- 5. Углеводы Моносахариды
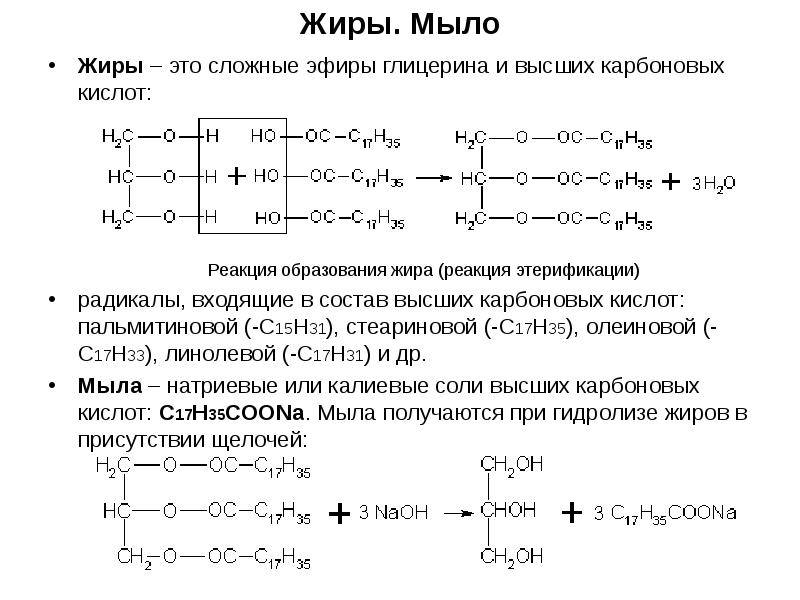
- 6. Жиры. Мыло Жиры – это сложные эфиры глицерина и высших карбоновых
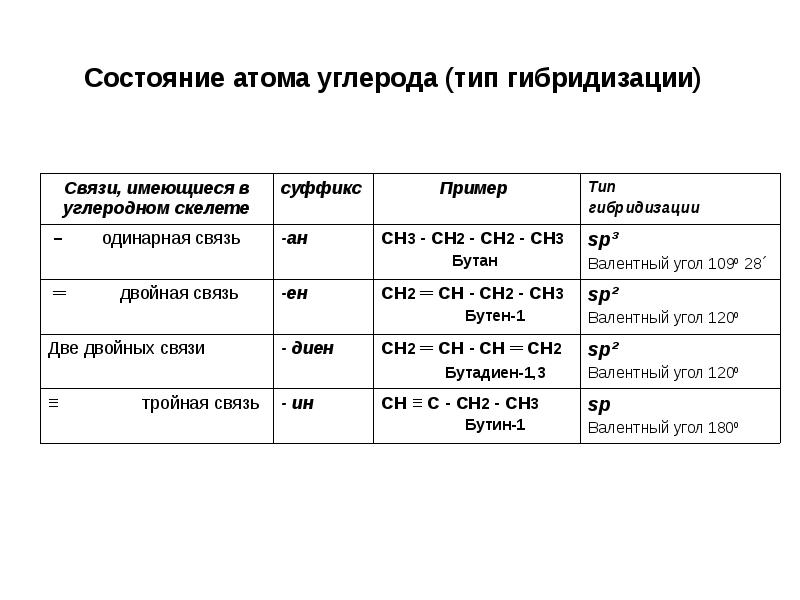
- 7. Состояние атома углерода (тип гибридизации)
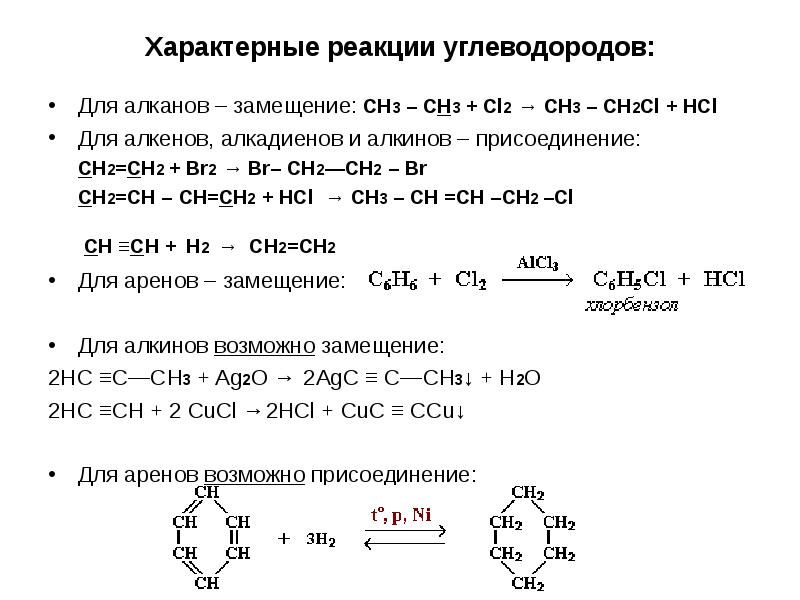
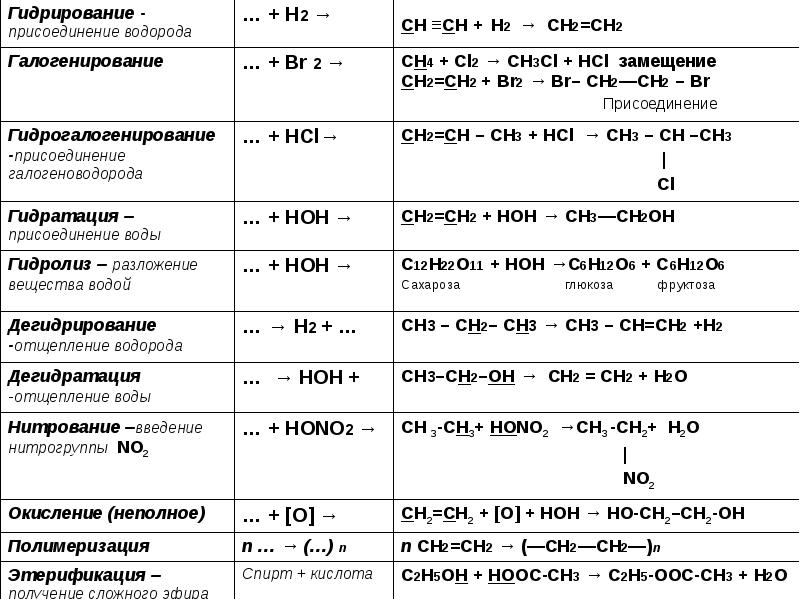
- 8. Характерные реакции углеводородов: Для алканов – замещение: CH3 – CH3 +
- 10. Качественные реакции На алкены, алкины, алкадиены – обесцвечивание бромной воды:
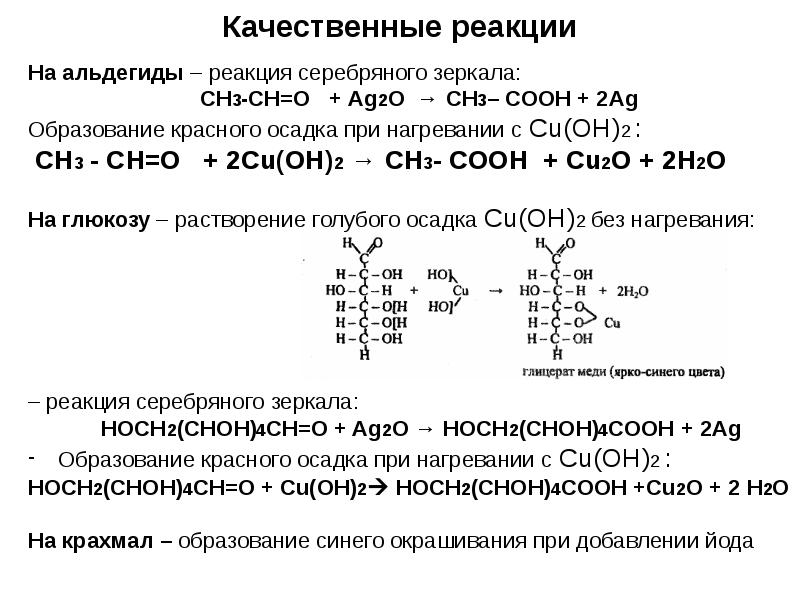
- 11. Качественные реакции На альдегиды – реакция серебряного зеркала:
- 12. Именные реакции: Именные реакции: Реакция Кучерова – получение уксусного альдегида (ацетальдегида)
- 13. Полимеры: Получение полиэтилена, полипропилена: n CH2=CH2 → (—CH2—CH2—)n полиэтилен
- 14. Скачать презентацию






Слайды и текст этой презентации
Скачать презентацию на тему Органическая химия. Подготовка к контрольной работе № 2 можно ниже:
Похожие презентации





























