Подготовка к итоговой контрольной работе. (9 класс) презентация
Содержание
- 2. Часть А. Тестовые задания. 1. Схема распределения электронов по энергетическим уровням
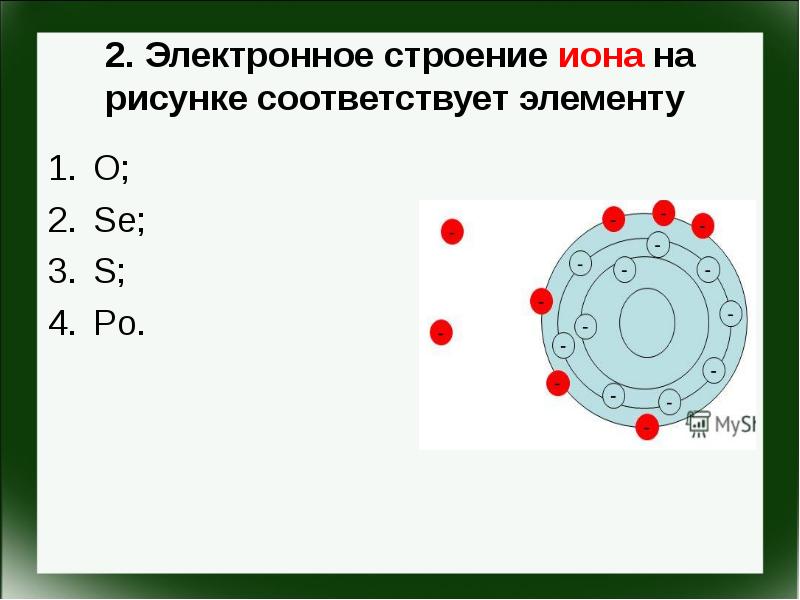
- 3. 2. Электронное строение иона на рисунке соответствует элементу O; Se;
- 4. 3. Ряд элементов расположенных в порядке увеличения электроотрицательности: F-Cl-Br; K-Na-Li; C-Si-Ge;
- 5. 4. Вещество имеющее кристаллическое строение это: NaCl; H2O; HCl; CH3COOH.
- 6. 5. Оксид углерода (II) является: Амфотерным; Кислотным; Несолеобразующим; Основным.
- 7. 6. Ряд формул веществ реагирующих с гидроксидом калия: Al, CO2, HCl;
- 8. 7. Необратимая химическая реакция произойдёт при сливании растворов веществ, формулы которых:
- 9. 8. Степень окисления серы S 2- в соединении формула которого: S;
- 10. 9. Уравнению реакции S+O2=SO2 соответствует схема превращения: S0→S-2; S+6→S0; S0→S-6; S0→S+4.
- 11. 10. Взаимодействию гидроксида бария и хлороводорода соответствует краткое ионное уравнение Ba2++2Cl-=BaCl2;
- 12. Часть Б. Задания со свободным ответом. 11. Составьте уравнения химических реакций
- 13. 12. По краткому ионному уравнению CO32-+2H+=H2O+CO2 составьте молекулярное уравнение.
- 14. 13. Дана схема превращений. Барий→Оксид бария→X→Карбонат бария Напишите молекулярные уравнения
- 15. 14. Задача ? Повторить! Строение атомов и ионов химических элементов; Изменение
- 16. Скачать презентацию














Слайды и текст этой презентации
Скачать презентацию на тему Подготовка к итоговой контрольной работе. (9 класс) можно ниже:
Похожие презентации





























