Растворы и растворимость. (8 класс) презентация
Содержание
- 2.
- 3. Утром встал я спозаранку. Чай налил, нашёл баранку.
- 4. ТЕМА: Растворение. Растворимость веществ в воде.
- 5. Растворы играют важную роль в природе, науке и технике. Особую роль
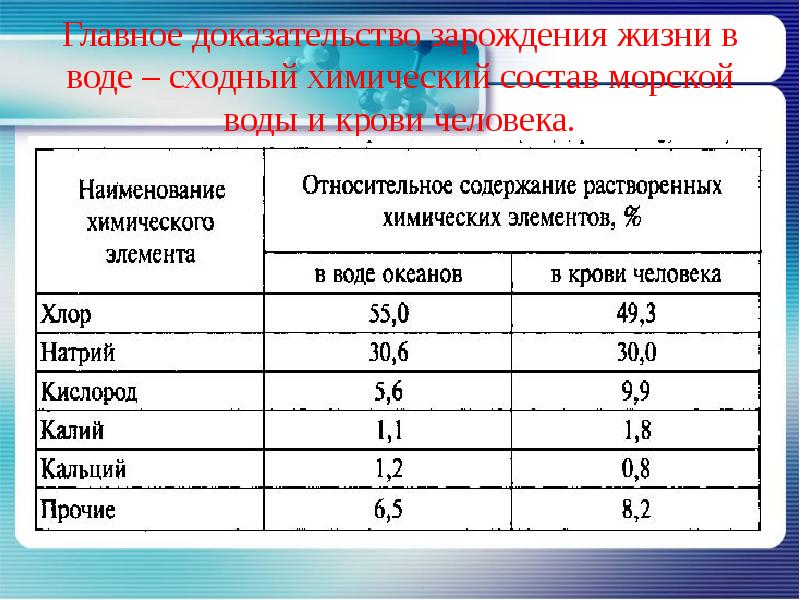
- 6. Главное доказательство зарождения жизни в воде – сходный химический состав морской
- 7. А знаете ли вы, что в 1м3 морской воды растворено 0,01мг золота.
- 8. Какие растворы Вам известны?
- 9. Растворы Вода
- 10. Что же такое раствор?
- 11. Раствор – однородная система, состоящая из частиц растворённого вещества, растворителя и
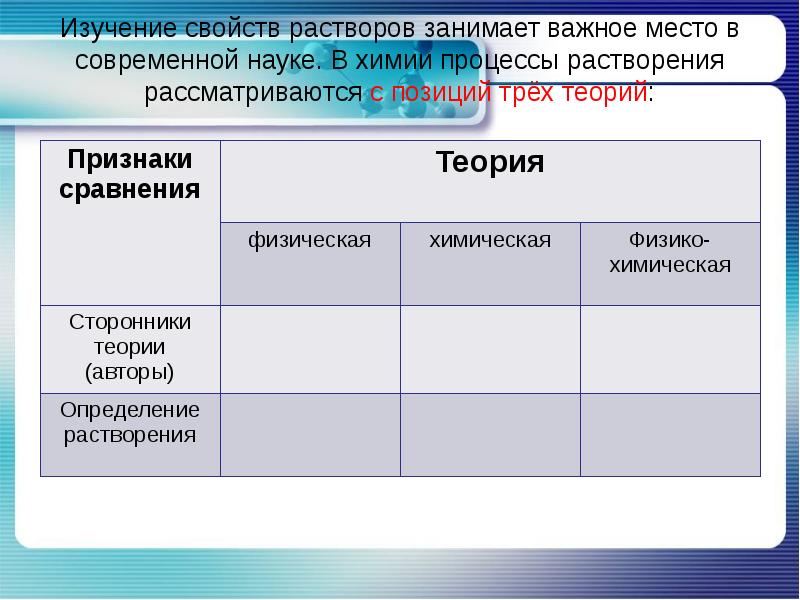
- 12. Изучение свойств растворов занимает важное место в современной науке. В химии
- 13. Изучение свойств растворов занимает важное место в современной науке. В химии
- 14. Гидраты – соединения, образованные взаимодействием вещества с водой. Кристаллогидраты – соли,
- 15. Какие признаки химических реакций Вы знаете?
- 16. Практическая часть 1опыт. Растворение сахара. 2 опыт. Растворение перманганата калия.
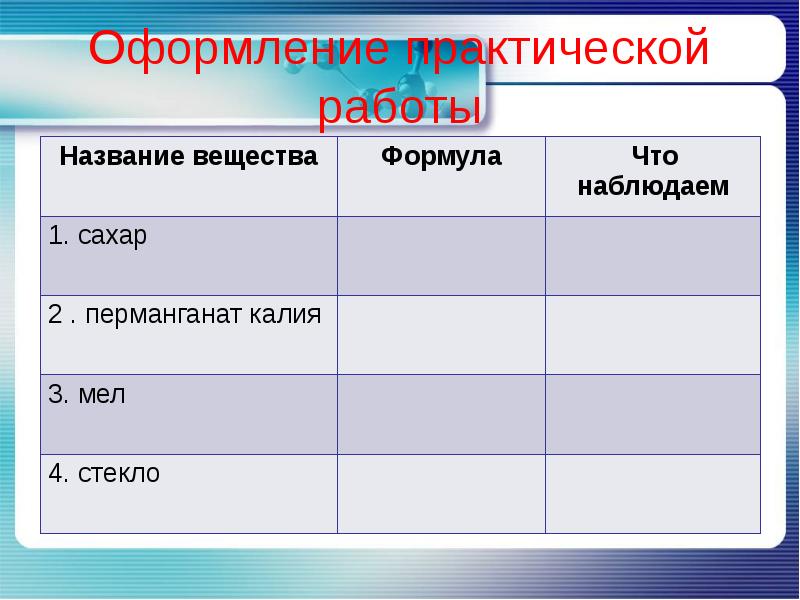
- 17. Оформление практической работы
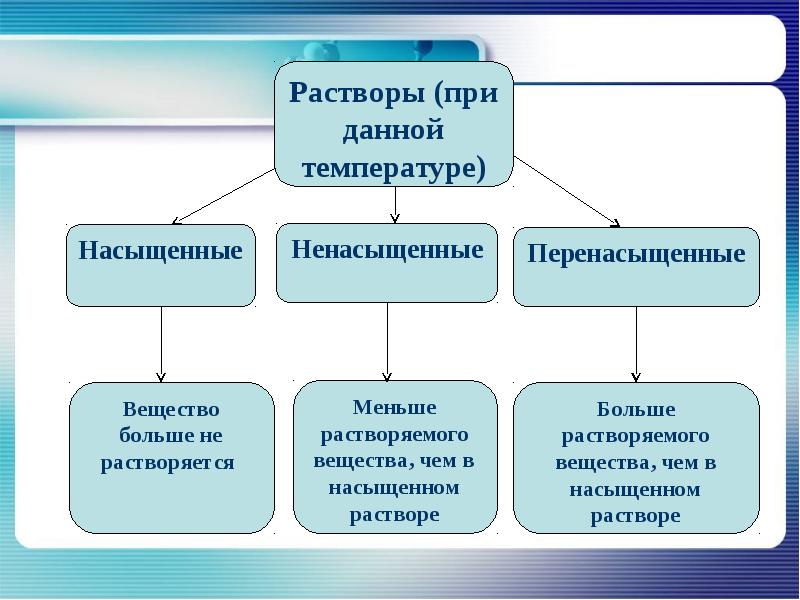
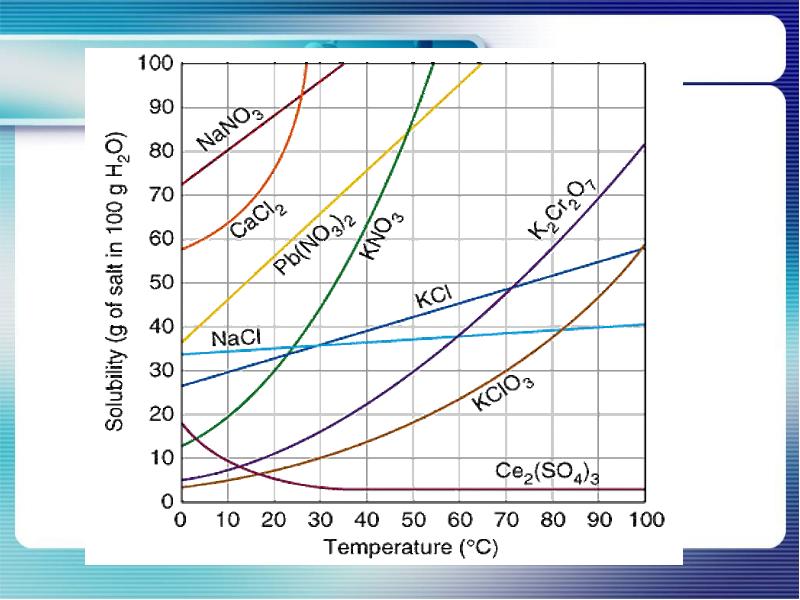
- 18. От чего зависит растворимость веществ?
- 19. Растворимость веществ зависит от: Природы вещества Природы растворителя Температуры
- 24. Решение задач Задача 1. Запишите химическое уравнение взаимодействия серной кислоты с
- 25. Тест на закрепление 1. Растворимость веществ не зависит от: А)
- 26. ответы 1. В 2. Б 3. А 4. Г 5.
- 27. Домашнее задание: §34, упр. 1, 3, 5, 6
- 29. СПАСИБО ЗА УРОК!
- 30. Скачать презентацию






















Слайды и текст этой презентации
Скачать презентацию на тему Растворы и растворимость. (8 класс) можно ниже:
Похожие презентации





























